Alles über atmosphärische Luft. Was ist Luft und woraus besteht sie?
Lesen Sie auch
Gaszusammensetzung der atmosphärischen Luft
Die Gaszusammensetzung der Luft, die wir atmen, sieht folgendermaßen aus: 78 % sind Stickstoff, 21 % sind Sauerstoff und 1 % sind andere Gase. Doch in der Atmosphäre großer Industriestädte wird dieses Verhältnis oft verletzt. Ein erheblicher Anteil besteht aus schädlichen Verunreinigungen, die durch Emissionen von Unternehmen und Fahrzeugen verursacht werden. Durch den Kraftverkehr gelangen viele Verunreinigungen in die Atmosphäre: Kohlenwasserstoffe unbekannter Zusammensetzung, Benzo(a)pyren, Kohlendioxid, Schwefel- und Stickstoffverbindungen, Blei, Kohlenmonoxid.
Die Atmosphäre besteht aus einer Mischung mehrerer Gase – Luft, in der kolloidale Verunreinigungen suspendiert sind – Staub, Tröpfchen, Kristalle usw. Die Zusammensetzung der atmosphärischen Luft ändert sich mit der Höhe kaum. Ab einer Höhe von etwa 100 km entsteht jedoch neben molekularem Sauerstoff und Stickstoff auch atomarer Sauerstoff durch die Dissoziation von Molekülen und die gravitative Trennung von Gasen beginnt. Oberhalb von 300 km überwiegt in der Atmosphäre atomarer Sauerstoff, über 1000 km Helium und dann atomarer Wasserstoff. Der Druck und die Dichte der Atmosphäre nehmen mit der Höhe ab; Etwa die Hälfte der Gesamtmasse der Atmosphäre konzentriert sich auf die unteren 5 km, 9/10 auf die unteren 20 km und 99,5 % auf die unteren 80 km. In Höhen von etwa 750 km sinkt die Luftdichte auf 10-10 g/m3 (während sie an der Erdoberfläche etwa 103 g/m3 beträgt), aber selbst eine so geringe Dichte reicht noch für das Auftreten von Polarlichtern aus. Die Atmosphäre hat keine scharfe obere Grenze; Dichte seiner Gasbestandteile
Die Zusammensetzung der atmosphärischen Luft, die jeder von uns atmet, umfasst mehrere Gase, von denen die wichtigsten sind: Stickstoff (78,09 %), Sauerstoff (20,95 %), Wasserstoff (0,01 %), Kohlendioxid (Kohlendioxid) (0,03 %) und Inertgase (0,93 %). Darüber hinaus befindet sich immer eine gewisse Menge Wasserdampf in der Luft, deren Menge sich bei Temperaturänderungen immer ändert: Je höher die Temperatur, desto größer der Dampfgehalt und umgekehrt. Aufgrund der schwankenden Menge an Wasserdampf in der Luft ist auch der Anteil der darin enthaltenen Gase nicht konstant. Alle Gase, aus denen Luft besteht, sind farb- und geruchlos. Das Gewicht der Luft ändert sich nicht nur abhängig von der Temperatur, sondern auch vom Wasserdampfgehalt darin. Bei gleicher Temperatur ist das Gewicht trockener Luft größer als das feuchter Luft, weil Wasserdampf ist viel leichter als Luftdampf.
Die Tabelle zeigt Gaszusammensetzung Atmosphäre im volumetrischen Massenverhältnis sowie die Lebensdauer der Hauptkomponenten:
| Komponente | % Volumen | % Masse |
| N 2 | 78,09 | 75,50 |
| O2 | 20,95 | 23,15 |
| Ar | 0,933 | 1,292 |
| CO2 | 0,03 | 0,046 |
| Ne | 1,8 10 -3 | 1,4 10 -3 |
| Er | 4,6 10 -4 | 6,4 10 -5 |
| CH 4 | 1,52 10 -4 | 8,4 10 -5 |
| Kr | 1,14 10 -4 | 3 10 -4 |
| H 2 | 5 10 -5 | 8 10 -5 |
| N2O | 5 10 -5 | 8 10 -5 |
| Xe | 8,6 10 -6 | 4 10 -5 |
| O 3 | 3 10 -7 - 3 10 -6 | 5 10 -7 - 5 10 -6 |
| Rn | 6 10 -18 | 4,5 10 -17 |
Die Eigenschaften der Gase, aus denen die atmosphärische Luft unter Druck besteht, ändern sich.
Zum Beispiel: Sauerstoff unter einem Druck von mehr als 2 Atmosphären hat eine toxische Wirkung auf den Körper.
Stickstoff unter einem Druck über 5 Atmosphären hat eine narkotische Wirkung (Stickstoffvergiftung). Ein schneller Aufstieg aus der Tiefe führt zu einer Dekompressionskrankheit, da Stickstoffbläschen schnell aus dem Blut freigesetzt werden, als würde es aufschäumen.
Ein Anstieg des Kohlendioxids im Atemgemisch um mehr als 3 % führt zum Tod.
Jeder Bestandteil der Luft wird bei einem Druckanstieg bis zu bestimmten Grenzen zu einem Gift, das den Körper vergiften kann.
Untersuchungen zur Gaszusammensetzung der Atmosphäre. Atmosphärenchemie
Für die Geschichte der rasanten Entwicklung eines relativ jungen Wissenschaftszweigs namens Atmosphärenchemie ist der im Hochgeschwindigkeitssport verwendete Begriff „Spurt“ (Wurf) am besten geeignet. Den Startschuss gaben vermutlich zwei Anfang der 1970er Jahre veröffentlichte Artikel. Sie sprachen über die mögliche Zerstörung des stratosphärischen Ozons durch Stickoxide – NO und NO 2. Der erste gehörte dem späteren Nobelpreisträger und damaligen Mitarbeiter der Universität Stockholm, P. Crutzen, der die wahrscheinliche Quelle von Stickoxiden in der Stratosphäre als natürlich vorkommendes Lachgas N 2 O ansah, das unter dem Einfluss von Sonnenlicht zerfällt. Der Autor des zweiten Artikels, der Chemiker G. Johnston von der University of California in Berkeley, vermutete, dass Stickoxide in der Stratosphäre als Folge menschlicher Aktivitäten auftreten, nämlich beim Ausstoß von Verbrennungsprodukten Strahltriebwerke Flugzeuge in großer Höhe.
Natürlich sind die oben genannten Hypothesen nicht aus dem Nichts entstanden. Das Verhältnis zumindest der Hauptbestandteile der atmosphärischen Luft – Stickstoff-, Sauerstoff-, Wasserdampfmoleküle usw. – war schon viel früher bekannt. Bereits in der zweiten Hälfte des 19. Jahrhunderts. In Europa wurden Messungen der Ozonkonzentration in der Oberflächenluft durchgeführt. In den 1930er Jahren entdeckte der englische Wissenschaftler S. Chapman den Mechanismus der Ozonbildung in einer reinen Sauerstoffatmosphäre und wies auf eine Reihe von Wechselwirkungen zwischen Sauerstoffatomen und -molekülen sowie Ozon in Abwesenheit anderer Luftbestandteile hin. Messungen mit Wetterraketen zeigten jedoch Ende der 50er Jahre, dass in der Stratosphäre viel weniger Ozon vorhanden war, als nach dem Chapman-Reaktionszyklus vorhanden sein sollte. Obwohl dieser Mechanismus bis heute von grundlegender Bedeutung ist, ist klar geworden, dass es noch einige andere Prozesse gibt, die ebenfalls aktiv an der Bildung von atmosphärischem Ozon beteiligt sind.
Es ist erwähnenswert, dass zu Beginn der 70er Jahre Kenntnisse auf dem Gebiet der Atmosphärenchemie hauptsächlich durch die Bemühungen einzelner Wissenschaftler erlangt wurden, deren Forschung durch kein gesellschaftlich bedeutsames Konzept verbunden war und meist rein akademischer Natur war. Johnstons Arbeit ist eine andere Sache: Nach seinen Berechnungen könnten 500 Flugzeuge, die sieben Stunden am Tag fliegen, die Menge an stratosphärischem Ozon um nicht weniger als 10 % reduzieren! Und wenn diese Einschätzungen fair wären, dann würde das Problem sofort zu einem sozioökonomischen Problem, da in diesem Fall alle Programme zur Entwicklung der Überschalltransportluftfahrt und der damit verbundenen Infrastruktur erheblich angepasst und möglicherweise sogar eingestellt werden müssten. Darüber hinaus stellte sich dann zum ersten Mal wirklich die Frage, dass anthropogene Aktivitäten keine lokale, sondern eine globale Katastrophe verursachen könnten. Natürlich erforderte die Theorie in der gegenwärtigen Situation eine sehr strenge und gleichzeitig praktische Überprüfung.
Erinnern wir uns daran, dass der Kern der oben genannten Hypothese darin bestand, dass Stickoxid mit Ozon NO + O 3 ® ® NO 2 + O 2 reagiert, dann reagiert das bei dieser Reaktion gebildete Stickstoffdioxid mit dem Sauerstoffatom NO 2 + O ® NO + O 2 , wodurch das Vorhandensein von NO in der Atmosphäre wiederhergestellt wird, während das Ozonmolekül für immer verloren geht. In diesem Fall wird ein solches Reaktionspaar, das den Stickstoff-Katalysezyklus der Ozonzerstörung ausmacht, wiederholt, bis irgendwelche chemischen oder physikalischen Prozesse zur Entfernung von Stickoxiden aus der Atmosphäre führen. Beispielsweise wird NO 2 zu oxidiert Salpetersäure HNO 3 ist gut wasserlöslich und wird daher durch Wolken und Niederschläge aus der Atmosphäre entfernt. Der katalytische Stickstoffkreislauf ist sehr effektiv: Ein Molekül NO schafft es während seines Aufenthalts in der Atmosphäre, Zehntausende Ozonmoleküle zu zerstören.
Aber wie Sie wissen, kommt Ärger nicht von alleine. Bald entdeckten Experten der US-Universitäten Michigan (R. Stolarski und R. Cicerone) und Harvard (S. Wofsey und M. McElroy), dass Ozon möglicherweise einen noch gnadenloseren Feind hat – Chlorverbindungen. Der Chlor-Katalysezyklus der Ozonzerstörung (Reaktionen Cl + O 3 ® ClO + O 2 und ClO + O ® Cl + O 2) war ihren Schätzungen zufolge um ein Vielfaches effizienter als der Stickstoff-Zyklus. Der einzige Grund für vorsichtigen Optimismus war, dass die Menge des natürlich vorkommenden Chlors in der Atmosphäre relativ gering ist, was bedeutet, dass die Gesamtwirkung seiner Auswirkungen auf das Ozon möglicherweise nicht allzu stark ist. Die Situation änderte sich jedoch dramatisch, als 1974 Mitarbeiter der University of California in Irvine, S. Rowland und M. Molina, feststellten, dass die Chlorquelle in der Stratosphäre Fluorch(FCKW) sind, die in weit verbreitet sind Kühlaggregate, Aerosolverpackungen usw. Da diese Stoffe nicht brennbar, ungiftig und chemisch passiv sind, werden sie durch aufsteigende Luftströme langsam von der Erdoberfläche in die Stratosphäre transportiert, wo ihre Moleküle durch Sonnenlicht zerstört werden, was zur Freisetzung freier Chloratome führt. Industrielle Produktion Die seit den 30er-Jahren einsetzende Verbreitung von FCKW und deren Emissionen in die Atmosphäre haben in allen Folgejahren, insbesondere in den 70er- und 80er-Jahren, stetig zugenommen. So haben Theoretiker innerhalb kürzester Zeit zwei Probleme in der Atmosphärenchemie identifiziert, die durch starke anthropogene Verschmutzung verursacht werden.
Um die Gültigkeit der aufgestellten Hypothesen zu testen, waren jedoch viele Aufgaben erforderlich.
Erstens, Erweiterung der Laborforschung, bei der es möglich wäre, die Geschwindigkeit photochemischer Reaktionen zwischen verschiedenen Bestandteilen der atmosphärischen Luft zu bestimmen oder zu klären. Es muss gesagt werden, dass die damals sehr dürftigen Daten zu diesen Geschwindigkeiten auch ziemlich viele Fehler aufwiesen (bis zu mehreren hundert Prozent). Darüber hinaus entsprachen die Bedingungen, unter denen die Messungen durchgeführt wurden, in der Regel nicht genau den Realitäten der Atmosphäre, was den Fehler erheblich verschärfte, da die Intensität der meisten Reaktionen von der Temperatur und manchmal vom Druck oder der Dichte der Atmosphäre abhing Luft.
Zweitens, untersuchen intensiv die strahlungsoptischen Eigenschaften einer Reihe kleiner atmosphärischer Gase unter Laborbedingungen. Durch die ultraviolette Strahlung der Sonne (in Photolysereaktionen) werden Moleküle einer erheblichen Anzahl von Bestandteilen der atmosphärischen Luft zerstört, darunter nicht nur die oben genannten FCKW, sondern auch molekularer Sauerstoff, Ozon, Stickoxide und viele andere. Daher waren Schätzungen der Parameter jeder Photolysereaktion gleichermaßen notwendig und wichtig für die korrekte Reproduktion der Atmosphäre Chemische Prozesse sowie die Reaktionsgeschwindigkeiten zwischen verschiedenen Molekülen.
LUFT
ein Gasgemisch, aus dem die Erdatmosphäre besteht und das sich bis zu einer Höhe von 1000–1200 km erstreckt. Bis zu einer Höhe von ca. 11 km bleibt die Zusammensetzung der Atmosphäre unverändert. Diese Schicht wird Troposphäre genannt. Es spielt die meisten meteorologischen Prozesse ab, die das Wetter bestimmen. Hier herrscht eine intensive Luftzirkulation, es entstehen Winde, Stürme und Hurrikane und die Turbulenzen sind hoch. Fast der gesamte Wasserdampf in der Atmosphäre und fast der gesamte Staub in der Luft konzentrieren sich in der Troposphäre, weshalb hier die meiste Wolkenbildung stattfindet. Oberhalb der Troposphäre befindet sich die Stratosphärenschicht, die sich über eine Länge von etwa 50 km erstreckt. Hier gibt es relativ große Ströme ruhige Luftüber große Entfernungen ohne nennenswerte Störungen zirkulieren. Im unteren Teil der Stratosphäre bilden sich seltene Wolken aus winzigen Eiskristallen. Oberhalb der Stratosphäre bis zu einer Höhe von ca. Die Mesosphäre erstreckt sich über 80 km – die Schicht, in der unter natürlichen Bedingungen die niedrigste Lufttemperatur erreicht wird, etwa -110 °C (160 K). Weiter bis zu einer Höhe von ca. 720 km folgen der Thermosphärenschicht. Hier bewegen sich Luftmoleküle so schnell, dass ihre Temperatur bei etwa 3000 °C liegen würde, wenn die Luftdichte die gleiche wie auf Meereshöhe wäre (und nicht milliardenfach kleiner). obere Schicht Atmosphäre - Exosphäre. Darin ist die Luft extrem verdünnt und Kollisionen von Molekülen untereinander sind so selten, dass sich die meisten von ihnen wie eine Kugel auf einfachen ballistischen Flugbahnen und einige von ihnen wie künstliche Erdsatelliten auf elliptischen Bahnen bewegen. Ein bestimmter Anteil der Moleküle, hauptsächlich Wasserstoff und Helium, erreicht Geschwindigkeiten, bei denen es möglich ist, die Wirkung der Schwerkraft zu überwinden, und wird im Raum zwischen Erde und Mond zerstreut (siehe auch ATMOSPHÄRE). Die wichtigste aller verschiedenen Eigenschaften der Luft ist, dass sie für das Leben auf der Erde notwendig ist. Ohne Sauerstoff wäre die Existenz von Mensch und Tier nicht möglich. Da zum Atmen verdünnter Sauerstoff erforderlich ist, ist auch das Vorhandensein anderer Gase in der Luft von entscheidender Bedeutung.
Verbindung. Auf Meereshöhe und innerhalb der Troposphäre ist die Gaszusammensetzung der Luft (in Vol.-%) wie folgt: Stickstoff – 78,08 %, Sauerstoff – 20,95 %, Argon – 0,93 %, Kohlendioxid (Kohlendioxid) – 0,034 %, Wasserstoff - 5 x 10-5 %; Darüber hinaus gibt es „Spuren“ der sogenannten Edelgase (oder inerten, seltenen Gase): Neon – 1,8 x 10-3 %, Helium – 5,24 x 10-4 %, Krypton – 1 x 10-4 % und Xenon - 8 x 10-6 %. Die Luft in der Troposphäre enthält auch unterschiedliche Mengen an Wasserdampf; Seine Luftfeuchtigkeit hängt davon ab Temperaturbedingungen und Höhen. In den unteren Schichten der Atmosphäre sind unterschiedliche Mengen an Staub und Asche in der Schwebe, die beispielsweise bei Verbrennungsprozessen und Vulkanausbrüchen entstehen. Das Vorhandensein solcher Aerosolpartikel in der Luft ist damit verbunden helle Farben Sonnenaufgänge und -untergänge aufgrund der Streuung der Sonnenstrahlen auf ihnen.
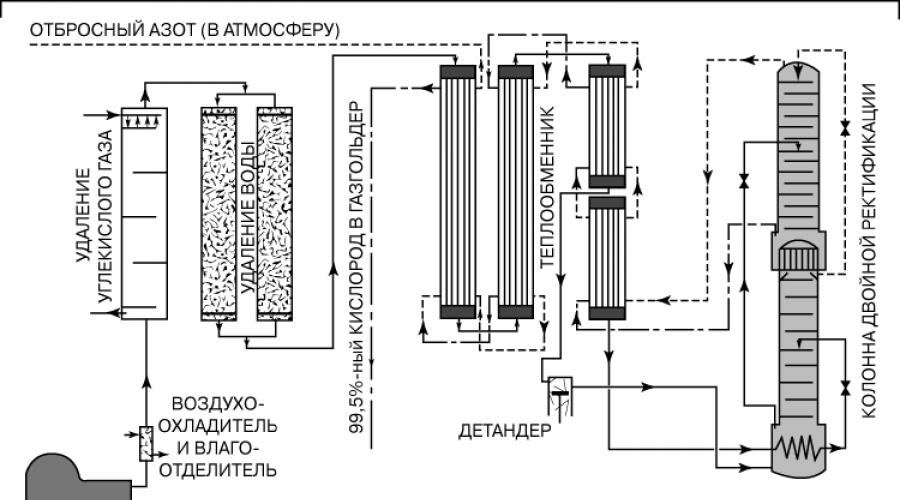
REKTIFIZIERUNG DER LUFTZERLEGUNG
Verschiedene Gase, aus denen die atmosphärische Luft besteht, können in einen flüssigen und sogar einen festen Zustand umgewandelt werden, wenn der Druck erhöht und die Temperatur entsprechend gesenkt wird. Der Mensch hat zahlreiche und vielfältige Einsatzmöglichkeiten für Luft gefunden. Der Anwendungsbereich von Gasbestandteilen der atmosphärischen Luft in Wissenschaft und Technik, Industrie und Alltag hat sich um ein Vielfaches erweitert, nachdem ein Verfahren zur Aufteilung des Luftgemisches in einzelne Komponenten entwickelt wurde. Bei dieser Methode wird Luft zunächst in einen flüssigen Zustand überführt und anschließend einer Destillation oder Rektifikation (Fraktionierung) unterzogen, ähnlich wie Rohöl in verschiedene Erdölprodukte getrennt wird. Die Luftverflüssigung wurde erstmals 1883 von Z. Wroblewski und K. Olszewski erfolgreich durchgeführt. Für die industrielle Anwendung der rektifizierenden Luftzerlegung sind zwei Umstände wichtig. Erstens bilden die Gase, aus denen Luft besteht, ein physikalisches Gemisch und keine chemische Verbindung, und zweitens unterscheiden sich die Siedepunkte verschiedener Luftbestandteile erheblich. Technische Mittel, die unter Berücksichtigung beider Faktoren geschaffen wurden, sorgen für eine nahezu vollständige Trennung der Hauptbestandteile der Luft und mit hochgradig Reinheit jeder Komponente. Der Prozess der Luftzerlegung erfolgt in drei Stufen: 1) Aufbereitung oder Reinigung von Luft, 2) Umwandlung der gereinigten Luft in die flüssige Phase (Verflüssigung) und 3) rektifizierende Trennung des Flüssigkeitsgemischs in einzelne Gase.

Entfernen von Verunreinigungen. Bevor die Luft in die Verflüssigungs- und Rektifikationsabschnitte der Luftzerlegungsanlage gelangt, werden alle Verunreinigungen entfernt, die entweder in Form von Feststoffpartikeln in der atmosphärischen Luft schweben oder bei sinkender Temperatur leicht zu Feststoffen werden können. Andernfalls ist eine schnelle Verstopfung enger Gerätekanäle unvermeidlich. Zu diesen Fremdverunreinigungen zählen Wasserdampf, Staub, Rauch und Dämpfe anderer Stoffe sowie Kohlendioxid. Der Großteil dieser Verunreinigungen wird von Öl- und Feuchtigkeitsabscheidern zurückgehalten, normalerweise nach der Verdichtung durch den Kompressor. In diesem Fall ist es vorzuziehen, die Luft nach der Kompression zu trocknen weniger Wasser muss als Dampf abgeführt werden, da es beim Komprimieren größtenteils in Flüssigkeit übergeht. Die weitere Trocknung der Luft erfolgt durch Durchleiten durch Adsorber mit aktiviertem Aluminiumoxid oder Kieselgel (teilweise dehydriertes Siliziumdioxid). Kohlendioxid kann entfernt werden chemisch durch Reaktion mit Kaliumhydroxid (Kalilauge) oder Natriumhydroxid (Natronlauge). Allerdings sind diese Chemikalien schnell aufgebraucht und müssen häufig nachgefüllt werden. Große Luftzerlegungsanlagen nutzen Wärmetauscher, die gleichzeitig Kohlendioxid und Wasserdampf entfernen und außerdem die in das System eintretende Luft kühlen. Leicht gefrierende Gase setzen sich in fester Form auf den Metalloberflächen von Wärmetauschern ab, die durch den Strom abgetrennter Gase, der durch ihre inneren Kanäle strömt, auf sehr niedrigen Temperaturen gehalten werden. Das System wird regelmäßig von angesammelten Verunreinigungen gereinigt, indem der Gasstrom im Wärmetauscher umgekehrt wird.
Verflüssigung. Die gereinigte Luft gelangt in den Verflüssigungsbereich und wird in einem mechanischen Kühlsystem gekühlt, bis der Großteil davon flüssig wird. Je nachdem, auf welchen Druck die Luft zunächst komprimiert wurde, sinkt ihre Temperatur dabei auf etwa 100 K. Die Zyklendrücke liegen zwischen 0,6 und 20 MPa. Bei der Kühlung wird die Kälte zuvor abgetrennter Gase aus dem Rektifikationsteil genutzt. In einem optimal ausgelegten Wärmetauscher wird die Kälte der abgeschiedenen Gase nahezu vollständig auf die einströmende Luft übertragen. In einigen Anlagen, insbesondere solchen, in denen ein Teil der abgeschiedenen Gase in flüssiger Form gesammelt wird, sind Wärmetauscher mit Freon oder Methylchlorid zur Vorkühlung auf etwa -40 °C (230 K) vorgesehen. Bei niedrigeren Temperaturen, die zur Luftverflüssigung erforderlich sind, ist das Kühlmedium entweder einströmende Luft oder abgetrennter Stickstoff. Dieses auf einen bestimmten Druck komprimierte Gas treibt eine Expansionsmaschine oder einen Expander (invertierter Kompressor) an. Durch die Ausdehnung bewegt das Gas den Kolben, der über die Kurbelwelle den elektrischen Generator dreht, der als „Bremse“ fungiert. Da das Gas bei der Expansion im Expander Arbeit verrichtet, sinken sein Wärmeinhalt und seine Temperatur. Wenn Sie das Gerät zum ersten Mal in Betrieb nehmen, müssen Sie es zunächst abkühlen Betriebstemperatur, und hierfür wird mehr Kälte benötigt als im stationären Betriebsmodus (Kühlung der Anlage). Kühlung kann auch durch die Expansion komprimierter Gase in der gasförmigen oder flüssigen Phase beim Durchströmen einer Absperrklappe erreicht werden. In diesem Fall ist der Temperaturabfall auf den Joule-Thomson-Effekt (Drosseleffekt) zurückzuführen. Diese Kühlmethoden basieren auf unterschiedlichen thermodynamischen Effekten, und wenn man sie in einen Kreislauf einführt richtige Reihenfolge, dann können Sie die Vorteile jedes einzelnen davon nutzen
(siehe auch
HITZE ;
THERMODYNAMIK;
PHYSIK NIEDRIGER TEMPERATUREN).
Verflüssigungs- und Rektifikationsabschnitte, die bei kryogenen Temperaturen betrieben werden, erfordern gute äußere Wärmedämmung. Daher sind die Geräte der genannten Abschnitte mit Gehäusen ausgestattet, die mit wärmeisolierenden Materialien gefüllt sind Mineralwolle, Glaswolle und poröse Vulkanasche. Die Baumaterialien von Wärmetauschern, Destillationskolonnen und Verbindungsleitungen werden sehr sorgfältig ausgewählt. Kohlenstoffstähle werden bei kryogenen Temperaturen spröde. Daher werden Materialien wie Kupfer, Bronze, Messing, Edelstahl und Aluminium bevorzugt, die unter kryogenen Bedingungen hervorragende Festigkeitseigenschaften aufweisen.
Berichtigung. Die Zerlegung der verflüssigten Luft in ihre Bestandteile erfolgt in vertikalen zylindrischen Vorrichtungen, sogenannten Rektifikationskolonnen. Im Inneren einer solchen Kolonne befindet sich eine vertikale Reihe horizontaler „Platten“ mit Löchern, durch die Flüssigkeit nach unten fließt und Gas vom Boden der Kolonne aufsteigt und mit der Flüssigkeit auf den Böden in Kontakt kommt. In Anlagen zur Abtrennung aller Luftbestandteile ist ein hoher Reinheitsgrad vorgesehen ganze Zeile solche Spalten. In den oberen Teil jeder Kolonne wird eine Flüssigkeit entsprechender Zusammensetzung eingeleitet und im unteren Teil werden die für eine ausreichend intensive Verdampfung notwendigen Bedingungen geschaffen, so dass es in der Kolonne zu einer allmählichen Trennung des Gemisches kommt. Unter normalem Atmosphärendruck verflüssigt sich Luft bei einer Temperatur von etwa 80 K (-190 °C); die Zusammensetzung der Mischung verändert sich im Vergleich zum Original. Wenn die ursprüngliche Luft etwa 79 % Stickstoff und 21 % Sauerstoff enthält, besteht die Flüssigkeit aufgrund der natürlichen kinetischen Umverteilung aus 65 % Stickstoff und 35 % Sauerstoff und das Gas über der Flüssigkeit besteht aus 87 % Stickstoff und 13 % Sauerstoff . Die anderen Gasbestandteile verhalten sich unabhängig vom Verhältnis zwischen Sauerstoff und Stickstoff genau gleich. Typischerweise ist der Dampf über der Flüssigkeit mit der Komponente mit dem niedrigeren Siedepunkt angereichert. Das Verhältnis zwischen den Phasen hängt natürlich vom Druck ab. Während die Flüssigkeit absinkt und der Dampf aufsteigt Destillationskolonne, die Konzentrationen der darin freigesetzten Bestandteile nehmen zu; Am Ende der Kolonne wird am Ende Sauerstoff „handelsüblicher“ Reinheit, am Kopf hochwertiger Stickstoff und an anderen Stellen Argon und eine Mischung „seltener“ Gase ausgewählt. Da die Temperatur in Luftzerlegungsanlagen in der Regel nicht unter den Siedepunkt von Stickstoff sinkt, bleiben Neon und Helium unverflüssigt und können im Gemisch mit Stickstoff unkondensiert aus der Hauptleitung entnommen werden Destillationskolonne. Gemische aus Sauerstoff und Argon sind schwieriger zu trennen als Gasgemische mit großer Unterschied bei Siedetemperaturen. In großen Luftzerlegungsanlagen wird der Kondensations-Verdampfungsprozess durch einen chemischen Prozess ergänzt, um die Ausbeute an hochreinem Argon zu erhöhen. Dem aus dem kryogenen Teil des Systems entnommenen Gemisch aus Sauerstoff, Stickstoff und Argon wird eine dosierte Menge Wasserstoffgas zugesetzt. Sauerstoff reagiert mit Wasserstoff in Gegenwart eines Palladiumkatalysators zu Wasser, das in Trocknern entfernt wird. Das verbleibende Gasgemisch aus Argon und Stickstoff wird erneut abgekühlt und einer erneuten Rektifikation zugeführt. Die endgültige Trennung der Edelgase (Helium, Neon, Krypton und Xenon) erfolgt in kombinierten Anlagen, in denen das Kondensations-Verdampfungsverfahren mit dem selektiven Adsorptionsverfahren kombiniert wird. Wird oft als Adsorptionsmittel verwendet Aktivkohle, auf die Temperatur von flüssigem Stickstoff abgekühlt.
Transport und Lagerung. Sauerstoff, Stickstoff und Argon werden sowohl in flüssiger als auch gasförmiger Form transportiert und gespeichert. Für kryogene Flüssigkeiten werden spezielle wärmeisolierte Behälter verwendet. Tieftemperaturgase werden unter einem Druck von bis zu 17 MPa in Stahlflaschen gelagert. Edelgase werden freigesetzt Glasgefäße Dewar mit einem Fassungsvermögen von 1-2 Litern; Es werden auch Thermoskannen aus Stahl verwendet.
INDUSTRIELLE ANWENDUNGEN VON ABGESETZTEN GASEN
Es gibt kaum eine Industrietätigkeit, bei der nicht das eine oder andere der abgeschiedenen Gase der Luft eine wesentliche Rolle spielt. Im Folgenden werden nur die wichtigsten Anwendungen aufgeführt.
Sauerstoff. Bei der Metallbearbeitung wird Sauerstoff mit verschiedenen Brenngasen (Acetylen, Propan, Erdgas) wird zum Schneiden und Schweißen von Hochtemperatur-Flammstahl verwendet. Zum Strippen wird eine Sauerstoff-Acetylen-Flamme verwendet Metalloberflächen zum Entfernen von Rost und Zunder sowie zum Hartlöten vieler Metalle. In der Metallurgie wird neuer Stahl unter Verwendung von mit Brenngasen vermischtem Sauerstoff feuergereinigt, um Mängel zu beseitigen. Um die Prozesse der Stahlherstellung zu beschleunigen, wird Sauerstoff in großen Mengen als Entkohlungs- und Oxidationsmittel verbraucht. Aufgrund der zunehmenden Verbreitung feuerfester Gläser wird Sauerstoff zunehmend in der Technologie zur Formung von Glasprodukten eingesetzt. IN Weltraumraketen Als Brennstoffkomponente wird Sauerstoff verwendet. Aufgrund des Platzmangels in solchen Flugzeugen wird es in flüssiger Form gespeichert, aber vor der Zufuhr zum Triebwerk in Gas umgewandelt.
siehe auch RAKETE; Weltraumforschung und -nutzung.
Stickstoff. Aufgrund seiner relativen Inertheit eignet sich Stickstoff besonders zum Schutz von Lebensmitteln, die unter Einwirkung von Sauerstoff verderben (oxidieren). In der Lebensmittelindustrie wird häufig eine Stickstoffatmosphäre eingesetzt, um die Belastung durch Luftsauerstoff zu verhindern, der zum Verderb führen kann. Lebensmittelprodukt oder Verlust des natürlichen Geruchs. In der Chemie-, Erdöl- und Farbenindustrie wird eine Stickstoffgasdecke verwendet, um die Reinheit des Produkts aufrechtzuerhalten und Feuer und Explosionen während der Verarbeitung zu verhindern. In der Elektronikindustrie wird Stickstoffgas gespült, um die Luft in Vakuumröhrenzylindern und Gehäusen von Halbleiterbauelementen zu verdrängen, bevor diese verschweißt und versiegelt werden. Stickstoff wird verwendet, um während des Glühens und der Wärmebehandlung eine kontrollierte Atmosphäre zu schaffen, um geschmolzenes Aluminium zu spülen, um gelösten Wasserstoff zu entfernen, und um Sekundäraluminium (Schrott) zu reinigen. In der Elektrotechnik wird häufig eine Hochdruck-Stickstoffatmosphäre eingesetzt, um einen hohen Isolationswiderstand aufrechtzuerhalten und die Lebensdauer von Isoliermaterialien zu erhöhen. Der Expansionsraum in ölgefüllten Transformatoren ist üblicherweise mit Stickstoff gefüllt. Flüssiger Stickstoff wird sowohl in der Industrie als auch in der Industrie häufig zur Kühlung eingesetzt wissenschaftliche Forschung, insbesondere bei Umwelttests.
Siehe auch STICKSTOFF.
Argon. Im Gegensatz zu Stickstoff, der bei erhöhten Temperaturen mit einigen Metallen reagieren kann, ist Argon unter allen Bedingungen völlig inert. Daher wird es zur Schaffung einer Schutzatmosphäre bei der Herstellung reaktiver Metalle wie Titan und Zirkonium eingesetzt. Es dient auch als Schutzmedium beim Lichtbogenschweißen schwer schweißbarer Metalle und Legierungen – Aluminium, Bronze, Kupfer, Monel-Metall und rostfreie Stähle. Argon eignet sich gut zum Befüllen (unter Zusatz von Stickstoff) von Glühlampen. Aufgrund seiner geringen Wärmeleitfähigkeit ermöglicht Argon höhere Glühfadentemperaturen, was die Lichtausbeute der Lampe erhöht, und sein hohes Molekulargewicht macht es schwierig, Metall aus einem heißen Wolframfaden zu verdampfen. Das Ergebnis ist eine längere Lampenlebensdauer. Argon, rein oder gemischt mit anderen Gasen, wird auch zum Füllen von Leuchtstofflampen verwendet, sowohl für die Beleuchtung (mit einer heißen Kathode) als auch für die Werbung (mit einer kalten Kathode). Darüber hinaus wird es bei der Herstellung hochreiner Halbleitermaterialien (Germanium und Silizium) für die Herstellung von Transistoren eingesetzt. Siehe auch TRANSISTOR.
Neon, Krypton und Xenon. Alle drei dieser Gase haben eine erhöhte Fähigkeit zur Ionisierung, d. h. Sie werden bei deutlich geringeren Spannungen elektrisch leitfähig als die meisten anderen Gase. Wenn sie ionisiert werden, strahlen diese Gase wie Argon und Helium helles Licht mit jeweils eigener Farbe aus und werden daher in Lampen für die Werbebeleuchtung verwendet. In der Elektronikindustrie werden diese Edelgase zum Befüllen spezieller Arten elektronischer Lampen verwendet – Zenerdioden, Starter, Fotozellen, Thyratrons, UV-Sterilisationslampen und Geigerzähler. In der Nuklearindustrie werden sie zum Füllen von Ionisations- und Blasenkammern sowie anderen Geräten zur Untersuchung subatomarer Teilchen und zur Messung der Intensität durchdringender Strahlung verwendet.
Wasserstoff, Helium und Kohlendioxid. Diese Gase werden in größeren Mengen durch andere Methoden hergestellt, deren Herstellung kostengünstiger ist. Daher werden sie nach der Luftzerlegung bei der Rektifikationstrennung üblicherweise in die Atmosphäre freigesetzt. Siehe auch WASSERSTOFF.
DRUCKLUFT
Die Energie der Druckluft kann genutzt werden, um mechanische Arbeit zu verrichten, einen Luftstrom oder ein Luftpolster zu erzeugen. Druckluft lässt sich leicht durch Rohre und Schläuche transportieren, sodass sie in beträchtlicher Entfernung von der Quelle (Kompressor oder Tank) verwendet werden kann hoher Druck) ohne große Energieverluste in der Übertragungsleitung.
Anwendung. Druckluft wird in pneumatischen Motoren verwendet, die Bohrmaschinen, Handschleifmaschinen und andere Geräte antreiben pneumatische Werkzeuge, in Bohr- und Presslufthämmern und in Torpedoluftturbinen. Der durch Druckluft erzeugte Luftstrom wird zum Transport von Getreide, Kohlenstaub und anderen pulverförmigen Materialien über Luftrutschen verwendet. Mithilfe von Druckluft belüften sie Minen, Gebäude und andere geschlossene Räume, mischen Flüssigkeiten durch Sprudeln in Bottichen und erzeugen einen Zwangszug in Hochöfen und anderen Öfen. Druckluft wird zum Ausgleich des Wasserdrucks in Tauchanzügen, zum Aufpumpen von Luftreifen, zum Betätigen von Bremsen in Zügen und zur Fernbeeinflussung von Steuergeräten für Prozessanlagen verwendet. Insgesamt sind es mehr als 200 verschiedene Arten Verwendung von Druckluft. Die groß angelegte Nutzung von Druckluftenergie begann im Jahr 1861, als M. Sommeyer einen Wasserkolbenkompressor entwarf, der von einem Wasserrad angetrieben wurde. Beim Bau des Mont-Cenis-Tunnels in den Alpen wurden Bohrhämmer mit Druckluft versorgt. Früher wurde stattdessen Dampf verwendet, doch der Abgasdampf führte zu unerträglichen Bedingungen für die Tunnelarbeiter. Die Vorteile des pneumatischen Antriebs, insbesondere im Untertagebergbau, wurden deutlich und die rasante Entwicklung der pneumatischen Technologie begann.
Kompressoren. Um Luft unter Druck zu liefern, wurde ein Kolbenkompressor entwickelt. Der Kolben in einem solchen Kompressor wird von einer Antriebsmaschine angetrieben. Beim Saughub wird Luft durch das Einlassventil angesaugt, beim Rückhub des Kolbens wird diese komprimiert und durch ein weiteres Ventil herausgedrückt. Federbelastete Sitzventile funktionieren ohne externen Steuermechanismus. Ein einfachwirkender Kompressor nutzt nur eine Seite des Kolbens zum Komprimieren, während ein doppeltwirkender Kompressor beide Enden des Zylinders zum Komprimieren nutzt. Wenn Luft komprimiert wird, steigt ihre Temperatur. Eine solche Erwärmung ist unerwünscht, da sich die Betriebsbedingungen des Kolbens verschlechtern. Wenn außerdem die beim Komprimieren entstehende Wärme abgeführt wird, ist dies erforderlich weniger Arbeit zur Komprimierung. Daher sind Kompressoren in der Regel wasser- oder luftgekühlt. Bei Einspritzdrücken über 0,4 MPa erfolgt die Verdichtung stufenweise. Zwei oder mehr Zylinder werden so verbunden, dass die Luft vom Auslass einer Stufe in den Einlass der anderen gelangt und der volle Auslassdruck erst am Auslass der letzteren erreicht wird. Zur Reduzierung der Lufttemperatur sind zwischen den Stufen Wärmetauscher vorgesehen. Sechsstufige Kompressoren dieses Typs sind in der Lage, Druckluft mit Drücken von bis zu 100 MPa zu liefern. Es gibt zwei Arten von Rotationskompressoren mit positiver Verdrängung: Flügelzellen- und Zweirotorkompressoren. Ein Flügelzellenkompressor ist genauso aufgebaut wie ein Flügelzellen-Luftmotor (siehe unten), nur dass sich der Rotor in die entgegengesetzte Richtung dreht. Bei einem Zwei-Rotor-Kompressor wird Luft im Raum zwischen den Rotoren und der Gehäusewand eingeschlossen und durch das Ineinandergreifen der Rotoren herausgedrückt. Radialgebläse und -kompressoren sind Rotationsmaschinen, die Kreiselpumpen ähneln. Die Energie der Luft wird durch die Zentrifugalwirkung der rotierenden Laufräder erhöht. Gebläse sind Maschinen, die Luft auf einen Druck von nicht mehr als 0,3 MPa (g) verdichten, und Kompressoren – auf Drücke, die diesen Wert überschreiten. Zur Druckerhöhung sind beide mehrstufig ausgeführt. Auf einer Welle sind mehrere Laufräder angebracht, und die Luft wird beim Übergang von einer Stufe zur nächsten nacheinander komprimiert.
Luftmotoren. Ein pneumatischer Motor ist eine Maschine, die umwandelt mechanische Arbeit Druckluftenergie. Luftmotoren sind Kolben-, Drehschieber- und Turbinenmotoren. Die Luftverdichtung erfolgt außerhalb des Motors, beispielsweise in einem Kompressor.

Kolbenluftmotoren. Eine Kolbenluftmaschine ähnelt einer Dampfmaschine. Druckluft gelangt in den Ventilkasten, und wenn das Ventil aktiviert ist, lässt es einen Teil der Luft in den Zylinder ein. Unter Luftdruck verrichtet der Kolben über eine Kurbel oder einen anderen Mechanismus nützliche Arbeit, wonach die Abluft in die Atmosphäre abgegeben wird. Der pneumatische Zyklus kann ohne Expansion oder mit Expansion sein.
Flügelrotations-Luftmotoren. Der Rotor eines solchen Motors ist relativ zur Mittellinie des festen Gehäuses versetzt. In den radialen Schlitzen des Rotors eingebaute rechteckige Platten (oder Schaufeln) werden gegen die Innenwand des Gehäuses gedrückt. Durch eine Öffnung in der Wand gelangt Druckluft in das zylindrische Gehäuse und füllt die „Kammer“, die aus der Rotorwand, der Gehäusewand und einer der Platten besteht. Unter Luftdruck dreht sich die Platte zusammen mit dem Rotor, und die nächste Platte, die an dem Loch vorbeigeht, unterbricht den Luftstrom in diese Kammer und ermöglicht den Zugang zur nächsten. Die eingeschlossene Luft dehnt sich unter Abgabe eines Teils ihrer Energie aus, bis das volle Volumen der Kammer erreicht ist. Danach öffnet sich die Abluftöffnung und ein Teil der Abluft tritt aus.
Turbinenluftmotoren. In einer Luftturbine wird die Druckenergie der Druckluft in die kinetische Energie ihrer gerichteten Bewegung umgewandelt, wenn die Luft in den Düsen expandiert. Ein Luftstrahl mit hoher Geschwindigkeit trifft auf die Rotorblätter, wirkt mit einer tangentialen Kraft auf sie und zwingt sie in Rotation (Luftturbinen ähneln Dampfturbinen).
Luft ist für alle lebenden Organismen notwendig: Tiere zum Atmen und Pflanzen für die Ernährung. Darüber hinaus schützt die Luft die Erde vor schädlichen Einflüssen UV-Strahlung Sonne. Die Hauptbestandteile der Luft sind Stickstoff und Sauerstoff. Die Luft enthält außerdem geringe Beimengungen von Edelgasen, Kohlendioxid und eine gewisse Menge an Feststoffpartikeln – Ruß und Staub. Alle Tiere brauchen Luft zum Atmen. Etwa 21 % der Luft besteht aus Sauerstoff. Ein Sauerstoffmolekül (O2) besteht aus zwei gebundenen Sauerstoffatomen.
Luftzusammensetzung
Der Anteil verschiedener Gase in der Luft schwankt je nach Standort, Jahreszeit und Tag leicht. Stickstoff und Sauerstoff sind die Hauptbestandteile der Luft. Ein Prozent der Luft besteht aus Edelgasen, Kohlendioxid, Wasserdampf und Schadstoffen wie Stickstoffdioxid. In der Luft enthaltene Gase können durch abgetrennt werden fraktionierte Destillation. Die Luft wird abgekühlt, bis die Gase in einen flüssigen Zustand übergehen (siehe Artikel „“). Anschließend wird die flüssige Mischung erhitzt. Jede Flüssigkeit hat ihren eigenen Siedepunkt und die beim Sieden entstehenden Gase können separat gesammelt werden. Sauerstoff, Stickstoff und Kohlendioxid gelangen ständig aus der Luft in die Luft und kehren wieder zurück, d. h. es entsteht ein Kreislauf. Tiere atmen Sauerstoff aus der Luft ein und Kohlendioxid aus.
Sauerstoff
Stickstoff
Mehr als 78 % der Luft besteht aus Stickstoff. Auch Proteine, aus denen lebende Organismen aufgebaut sind, enthalten Stickstoff. Hauptsächlich Industrielle Anwendung Stickstoff - Ammoniakproduktion für Düngemittel benötigt. Zu diesem Zweck wird Stickstoff mit kombiniert. Stickstoff wird in Verpackungen für Fleisch oder Fisch gepumpt, weil... Bei Kontakt mit normaler Luft oxidieren und zerfallen die Produkte. Zur Transplantation bestimmte menschliche Organe werden in flüssigem Stickstoff gelagert, da dieser kalt und chemisch inert ist. Ein Stickstoffmolekül (N2) besteht aus zwei verbundenen Stickstoffatomen.
Edelgase
Die Edelgase sind 6 der 8. Gruppe. Sie sind chemisch äußerst inert. Nur sie existieren in Form einzelner Atome, die keine Moleküle bilden. Aufgrund ihrer Passivität werden einige von ihnen zum Füllen von Lampen verwendet. Xenon wird vom Menschen praktisch nicht verwendet, Argon wird jedoch in Glühbirnen gepumpt und Leuchtstofflampen sind mit Krypton gefüllt. Neon blinkt bei elektrischer Ladung rot-orange. Es wird in Natrium-Straßenlaternen und Neonlampen verwendet. Radon ist radioaktiv. Es entsteht durch den Zerfall des Metalls Radium. Der Wissenschaft sind keine Heliumverbindungen bekannt und Helium gilt als völlig inert. Seine Dichte ist siebenmal geringer als die von Luft, weshalb Luftschiffe damit gefüllt sind. Mit Helium gefüllt Luftballons mit wissenschaftlicher Ausrüstung ausgestattet und in die obere Atmosphäre geschossen.
Treibhauseffekt
 Dies ist die Bezeichnung für den derzeit beobachteten Anstieg des Kohlendioxidgehalts in der Atmosphäre und die daraus resultierenden Folgen globale Erwärmung
, d.h. Anstieg der durchschnittlichen Jahrestemperaturen weltweit. Kohlendioxid verhindert, dass Wärme die Erde verlässt, so wie Glas in einem Gewächshaus hohe Temperaturen aufrechterhält. Je mehr Kohlendioxid in der Luft vorhanden ist, desto mehr Wärme wird in der Atmosphäre gespeichert. Schon eine leichte Erwärmung führt dazu, dass der Meeresspiegel steigt, sich die Winde ändern und ein Teil des Eises an den Polen schmilzt. Wissenschaftler gehen davon aus, dass die Durchschnittstemperatur in 50 Jahren um 1,5 °C bis 4 °C ansteigen könnte, wenn der Kohlendioxidgehalt so schnell ansteigt.
Dies ist die Bezeichnung für den derzeit beobachteten Anstieg des Kohlendioxidgehalts in der Atmosphäre und die daraus resultierenden Folgen globale Erwärmung
, d.h. Anstieg der durchschnittlichen Jahrestemperaturen weltweit. Kohlendioxid verhindert, dass Wärme die Erde verlässt, so wie Glas in einem Gewächshaus hohe Temperaturen aufrechterhält. Je mehr Kohlendioxid in der Luft vorhanden ist, desto mehr Wärme wird in der Atmosphäre gespeichert. Schon eine leichte Erwärmung führt dazu, dass der Meeresspiegel steigt, sich die Winde ändern und ein Teil des Eises an den Polen schmilzt. Wissenschaftler gehen davon aus, dass die Durchschnittstemperatur in 50 Jahren um 1,5 °C bis 4 °C ansteigen könnte, wenn der Kohlendioxidgehalt so schnell ansteigt.
Luft ist der wichtigste Stoff, ohne Zugang zu dem ein Mensch nicht einmal ein paar Minuten leben kann. Wir alle wissen, wie wichtig Luft für uns ist, aber wissen wir, wie sie ist?
Leider haben die meisten von uns nur sehr begrenzte Kenntnisse zu diesem Thema. Bringen wir die Situation in Ordnung.
Luft auf wissenschaftliche Weise
Streng genommen ist Luft ein natürliches Gasgemisch, das die Erdatmosphäre bildet. Der Hauptbestandteil der Luft, der sie bestimmt entscheidende Rolle im Leben lebender Organismen ist Sauerstoff. Sauerstoff wird in oxidativen Prozessen genutzt, die die lebensnotwendige Energie freisetzen.
Chemische Zusammensetzung der Luft
Der schottische Wissenschaftler Joseph Black zeigte 1754 durch eine Reihe von Experimenten, dass Luft keine homogene Substanz, sondern ein Gasgemisch ist. Die chemische Zusammensetzung der Luft wurde vom französischen Wissenschaftler Antoine Lavoisier bestimmt. Und daraus besteht unsere Erdenhülle:
- Stickstoff - 78 %;
- Sauerstoff - 21 %;
- andere Gase (Kohlendioxid, Argon, Neon, Methan, Helium, Krypton, Wasserstoff, Xenon) – 1 %.
Übrigens war die Luft nicht immer so – vor 4 Milliarden Jahren, zu Beginn der Entstehung unseres Planeten, bestand die Luft hauptsächlich aus Kohlendioxid. Es versteht sich von selbst, dass sich unter solchen Bedingungen einfach kein Leben entwickeln konnte. Allmählich ging Kohlendioxid verschiedene Reaktionen ein (in Wasser gelöst, mit Gesteinen reagiert) und sein Gehalt in der Luft nahm ab.
Als grüne Pflanzen auftauchten, die bekanntermaßen aktiv Kohlendioxid absorbieren und es im Lebensprozess nutzen, begann sein Gehalt in der Atmosphäre viel schneller zu sinken, bis schließlich die endgültige Zusammensetzung gebildet wurde.
Fairerweise ist anzumerken, dass diese endgültige Zusammensetzung von 78 %/21 %/1 % je nach Standort variiert: In Wäldern gibt es eine minimale Zusammensetzung an Verunreinigungen, und in Großstädte, im Gegenteil, ist maximal. Außerdem in verschiedene Teile Licht kann der Gehalt eines bestimmten Gases jeweils innerhalb von 3 % variieren.
Physikalische Eigenschaften
Zur Hauptsache physikalische Eigenschaften Zur Luft gehören Temperatur, Luftfeuchtigkeit und atmosphärischer Druck. Jede dieser Eigenschaften hat einen besonderen Einfluss auf den Zustand der Umwelt und des Menschen.
Lufttemperatur
Die Lufttemperatur bestimmt den thermischen Zustand Außenumgebung, also Wärmeübertragung. Höhere und niedrigere Temperaturen wirken sich negativ auf die Wärmeübertragung aus.
Bei erhöhten Temperaturen (mehr als 35 Grad Celsius) leitet der Körper überschüssige Wärme hauptsächlich durch Schwitzen ab. Zusammen mit dem Schweiß werden dem Körper Salze und wasserlösliche Vitamine entzogen, was zu vielen negativen Auswirkungen führt, insbesondere zu einer erhöhten Blutviskosität, Herzbeschwerden usw. Eine übermäßige Überhitzung des Körpers kann zu einem Hitzschlag führen.
Bei niedrigen Temperaturen kommt es im Körper zu einem Wärmemangel. Die allgemeine Abkühlung geht mit einer Schwächung der Muskelaktivität einher, lokale Abkühlung trägt zur Entstehung von Erkältungen bei.
Luftfeuchtigkeit
Die Luftfeuchtigkeit charakterisiert den Wasserdampfgehalt der Luft. Zu trockene Luft wirkt sich negativ auf die Schleimhaut der oberen Atemwege aus und führt zu Entzündungen und Rissen.
Atmosphärendruck
Änderungen des Luftdrucks sind im Erwachsenenalter besonders akut, und plötzliche Druckänderungen haben negative Folgen für einen jungen Körper.
Niedriger Luftdruck führt zu Hypoxie (Sauerstoffmangel), was wiederum Kopfschmerzen, beeinträchtigte Bewegungskoordination, Schläfrigkeit usw. hervorruft.
Zu den negativen Folgen eines erhöhten Luftdrucks zählen eine erhöhte Herzfrequenz, Atmung, ein erhöhter maximaler und verringerter minimaler Blutdruck usw.
Wichtiges Ergebnis
Wie Sie sehen, spielt die Luft und ihre Beschaffenheit – trocken oder feucht, heiß oder kalt – eine entscheidende Rolle. Somit ist Luft nicht nur für das Leben lebender Organismen notwendig, sie bestimmt auch die Qualität dieses Lebens.
Lesen Sie in den Artikeln mehr über den für uns wichtigsten Stoff.
Der Teil der Atmosphäre, der an die Erde angrenzt und den der Mensch entsprechend atmet, wird Troposphäre genannt. Die Troposphäre hat eine Höhe von neun bis elf Kilometern und ist ein mechanisches Gemisch verschiedener Gase.
Die Zusammensetzung der Luft ist nicht konstant. Abhängig von geografische Position, Gelände, Wetterverhältnisse, Luft kann unterschiedliche Zusammensetzung haben und verschiedene Eigenschaften. Die Luft kann verschmutzt oder verdünnt, frisch oder schwer sein – all das bedeutet, dass sie bestimmte Verunreinigungen enthält.
Stickstoff – 78,9 Prozent;
Sauerstoff – 20,95 Prozent;
Kohlendioxid - 0,3 Prozent.
Darüber hinaus sind in der Atmosphäre weitere Gase vorhanden (Helium, Argon, Neon, Xenon, Krypton, Wasserstoff, Radon, Ozon), deren Gesamtmenge etwas weniger als ein Prozent beträgt.
Es ist auch darauf hinzuweisen, dass in der Luft einige permanente Verunreinigungen natürlichen Ursprungs vorhanden sind, insbesondere einige gasförmige Produkte, die durch biologische und chemische Prozesse entstehen. Unter ihnen verdient Ammoniak eine besondere Erwähnung (die Zusammensetzung der Luft fernab von besiedelten Gebieten umfasst etwa drei bis fünf Tausendstel Milligramm pro Jahr). Kubikmeter), Methan (sein Gehalt beträgt durchschnittlich zwei Zehntausendstel Milligramm pro Kubikmeter), Stickoxide (in der Atmosphäre erreicht ihre Konzentration etwa fünfzehn Zehntausendstel Milligramm pro Kubikmeter), Schwefelwasserstoff und andere gasförmige Produkte.
Die chemische Zusammensetzung der Luft umfasst neben dampfförmigen und gasförmigen Verunreinigungen meist Staub kosmischen Ursprungs, der im Laufe des Jahres in einer Menge von siebenhunderttausendstel Tonnen pro Quadratkilometer auf die Erdoberfläche fällt, sowie Staubpartikel, die stammen aus Vulkanausbrüchen.
Was jedoch die Zusammensetzung der Luft am meisten verändert (und nicht zum Besseren) und die Troposphäre verschmutzt, ist der sogenannte Bodenstaub (Pflanzen-, Bodenstaub) und der Rauch von Waldbränden. Besonders viel Staub kommt in kontinentalen Luftmassen vor, die ihren Ursprung in den Wüsten Zentralasiens und Afrikas haben. Deshalb können wir mit Sicherheit sagen, dass eine ideal saubere Luftumgebung einfach nicht existiert und dass es sich um ein Konzept handelt, das nur theoretisch existiert.
Die Zusammensetzung der Luft neigt dazu, sich ständig zu verändern, und ihre natürlichen Veränderungen spielen in der Regel eine relativ geringe Rolle, insbesondere im Vergleich zu mögliche Konsequenzen seine künstlichen Verstöße. Solche Störungen werden hauptsächlich mit verbunden Produktionsaktivitäten Menschlichkeit, die Nutzung von Geräten für Verbraucherdienste sowie Fahrzeuge. Diese Störungen können unter anderem zur Denaturierung der Luft führen, also zu deutlichen Unterschieden in ihrer Zusammensetzung und ihren Eigenschaften gegenüber den entsprechenden Indikatoren der Atmosphäre.
Diese und viele andere Arten menschlicher Aktivitäten haben dazu geführt, dass die Grundzusammensetzung der Luft langsame und unbedeutende, aber dennoch absolut irreversible Veränderungen zu erfahren begann. Wissenschaftler haben beispielsweise berechnet, dass die Menschheit in den letzten fünfzig Jahren ungefähr die gleiche Menge an Sauerstoff verbraucht hat wie in den Millionen Jahren davor, und zwar in Prozentsatz- zwei Zehntel Prozent seiner gesamten Reserve in der Atmosphäre. Gleichzeitig nehmen die Emissionen in die Luft entsprechend zu. Nach neuesten Daten beliefen sich die Emissionen in den letzten hundert Jahren auf fast vierhundert Milliarden Tonnen.
Dadurch verändert sich die Zusammensetzung der Luft zum Schlechteren, und es ist schwer vorstellbar, wie sie in einigen Jahrzehnten aussehen wird.