Метан основной компонент. Природный газ - сн4 (Метан)
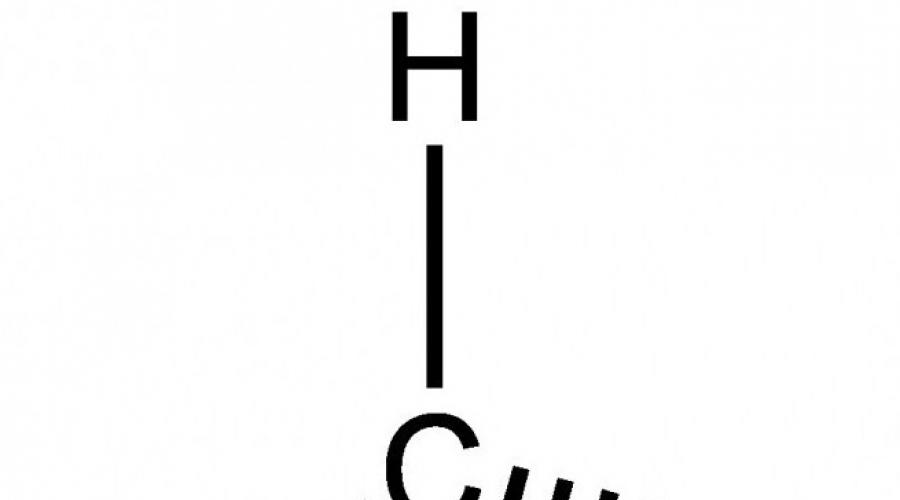
Читайте также
В воде
вспышки
самовозгорание
Пропан
Хлорметан
2. Строение молекулы
Молекулярная формула СН 4. Структурная и электронная формулы:
Н | Н-С-Н | H
3. Химические свойства
Первый член гомологического ряда насыщенных (метановых) углеводородов . Метан представляет собой малоактивные в химическом отношении вещество. При обычных условиях он довольно устойчив к действию кислот, щелочей и окислителей. Так, при пропускании метана через раствор KMnO 4, который является довольно сильным окислителем, он не окисляется и фиолетовая окраска раствора не исчезает. В реакции присоединения (сообщения) метан не вступает, поскольку в его молекуле все четыре валентности атома углерода полностью насыщены. Для метана, как и других предельных углеводородов, типичны реакции замещения, при которых атомы водорода замещаются атомами других элементов или атомными группами. Характерная для метана также реакция с хлором, которая происходит при обычной температуре под влиянием рассеянного света (при прямом солнечном свете может произойти взрыв). При этом атомы водорода в молекуле метана последовательно замещаются атомами хлора
- CH 4 + Cl 2 = CH 3 Cl + HCl
- CH 3 Cl + Cl 2 = CH 2 Cl 2 + HCl
- CH 2 Cl 2 + Cl 2 = CHCl 3 + HCl
- CHCl 3 + Cl 2 = CCl 4 + HCl
В результате реакции образуется смесь хлоропохидних метана.
В атмосфере воздуха метан горит бесцветным пламенем с выделением значительного количества тепла:
- CH 4 + 2O 2 = СО 2 + 2Н 2 О
С воздухом метан образует горючие взрывную смесь. При нагревании метана без доступа воздуха до температуры выше 1000 C он разлагается на элементы - на углерод (сажу) и водород:
- CH 4 = С + 2Н 2
4. Распространение в природе
Метан является основным компонентом:
- газов природных горючих (до 99,5%),
- нефтяных попутных (39-91%),
- болотных (99%) и рудничных (34-48%) газов;
- присутствует в газах грязевых вулканов (более 95%),
- спорадически встречается в вулканических газах и в газах магматических и метаморфических пород.
Большое количество метана растворено в водах океанов, морей, озер. Среднее содержание метана в водах Мирового океана около 10 -2 см 3 / л, общее количество - 14.10 12 м 3. Количество метана, растворенного в пластовых водах, на несколько порядков выше его промышленных запасов.
Метан присутствует также в атмосферах Земли , Юпитера , Сатурна , Урана ; в газах поверхностного грунта Луны . Основная масса метана лето-и гидросферы Земли образовалась при биохимической и термокаталитический деструкции рассеянного органического вещества, уголь и нефть. Метан образуется при анаэробном разложении органических веществ, в частности целлюлозы (метановое брожение).
В природе Земли метан довольно распространен. Горючие природные газы состоят на 90-97% из метана. Он образует много месторождений, из которых добывается и по газопроводам подается к месту использования. На дне болот и прудов метан образуется в результате разложения остатков растений без доступа воздуха. Поэтому его называют еще болотным газом. Под названием "рудничный газ" метан накапливается в угольных шахтах, в результате выделения из пластов угля и сопутствующих пород, в которых находится в свободном и связанном виде. На действующих шахтах наблюдается выделение метана из угольных пластов в объеме до 70-80 м / т с. б. м. (т с. б. м. - тонна сухого беззольной массы), что делает экономически целесообразным его самостоятельно или сопутствующее (дегазация) извлечения из угольных месторождений.
Рудничный газ очень опасен, поскольку с воздухом может образовывать взрывчатую смесь. Наиболее взрывоопасные концентрации метана в воздухе - 9-14%.
При низких температурах метан образует соединения включения - газовые гидраты , широко распространенные в природе.
Биотопливо ВВВС Генераторные газы Кокс Моторные топлива
Энергетическая биосырье
Большие количества метана используются как удобное и дешевое топливо. Неполное сжигание метана дает сажу, которая идет на изготовление печатной краски и как наполнитель каучука, а при термическом разложении (выше 1000 C) получают сажу и водород, который используется для синтеза аммиака. Продукт полного хлорирования метана - тетрахлорид углерода CCl 4 - является хорошим растворителем жиров и применяется для извлечения жиров из зерен масличных растений. Метан служит также исходным веществом для получения ацетилена , метилового спирта и многих других химических продуктов.
7. Метан как фактор угледобычи
С воздухом М. образует взрывчатые смеси. При содержании в воздухе до 5-6% М. горит около источника тепла (т-ра воспаление 650-750 С), при содержании 5-15,2 (16)% - взрывается, свыше 16% - может гореть при притоке кислорода, снижение при этом концентрации М. взрывоопасное. М. имеет слабое наркотическое действие. ПДК 300 мг / м 3. Выделение М. в выработки шахт создает особую опасность при добыче угля. Различают три формы выделения М. в горные выработки: обычное, суфлярным и внезапное. По метанообильность, согласно "Правил безопасности в угольных и сланцевых шахтах", шахты подразделяют на пять категорий. Критерием такого деления является относительная метанообильность, т.е. количество метана в кубометрах, выделяемой за сутки на 1 т среднесуточной добычи: с выделением метана до 5 м 3 / т, 5 - 10 м 3 / т, 10 - 15 м 3 / т; сверхкатегорийные - более 15 м 3 / т; опасные по суфлярным выделениями. Шахты, разрабатывающих пласты, опасные или угрожающие по внезапным выбросам угля, газа и породы, относятся к особой категории - опасных по внезапным выбросам. Перспективным считается добыча метана из угольных пластов (см. метаноноснисть угольного пласта , метан угольных месторождений). В конце ХХ в. этой проблемой только в США занимались ученые ок. 40 университетов, задействовано ок. 100 фирм. Первые промышленные попытки использовать попутный метан (при угледобыче) производятся и в Украине, в Донбассе. В промышленности М. применяют для получения синтезгаз, ацетилена, хлороформа, четыреххлористого углерода, технического углерода и др.. Продукты неполного окисления метана являются исходными для изготовления пластмасс, используемых в органическом синтезе.
См.. также
Источники
Метан (болотный газ; СН 4) - это простейший предельный углеводород. Бесцветный, не имеющий запаха газ, t° плавления -182,48°. Метан легко загорается; смесь метана с воздухом взрывоопасна.
Метан является основным компонентом природного газа (60-99%), рудничного газа (35-40%), а также различных продуктов анаэробного разложения органических веществ, например болотного газа, газов полей орошения. В больших количествах метан образуется при коксовании каменного угля, гидрировании угля и в других промышленных производствах.
Метан используется как топливо при газификации, а также для промышленного синтеза углеводородов большого мол. веса. При неполном сгорании или каталитическом окислении метана образует метанол (см. Метиловый спирт), (см.), ацетилен (см.). Метан используют также в производстве сажи, хлористого метила, хлорбромбензола, нитрометана, и других продуктов.
Метан обнаруживается в кишечных газах (в результате метанового брожения), в крови животных и человека.
Метан является наиболее инертным соединением из группы парафиновых углеводородов. Физиологический метан индифферентен и может вызывать отравления лишь в очень высокой концентрации (из-за малой растворимости метана в воде и крови). Вместе с тем токсическое действие метана проявляется и при более низких концентрациях метана в воздухе. Так, при содержании в воздухе 25-30% метана появляются первые признаки (учащение пульса, увеличение объема дыхания, нарушение координации тонких мышечных движений и т. д.). Более высокие концентрации метана в воздухе вызывают у человека головную боль. В полной мере токсическое действие метана проявляется лишь при повышенном давлении (2-3 атм).
Первая помощь при остром отравлении: удаление пострадавшего из вредной атмосферы. Грелки. При отсутствии дыхания немедленно (до прихода врача) искусственное дыхание, которое прекращается только после появления признаков трупного окоченения.
Хроническое действие метана. У работающих на или производствах, где в воздухе присутствуют метан и другие углеводороды ряда метана, описаны заметные сдвиги со стороны (положительный глазо-сердечный рефлекс, резко выраженная атропиновая проба, ). Тем не менее хроническое действие метана не вызывает тяжелых органических изменений, хотя некоторые исследователи связывают возникновение у шахтеров нистагма с длительным воздействием метана.
Профилактика отравлений метаном. В подземных выработках не допускается содержание метана выше 0,75 об.%. При повышении содержания метана рабочие должны быть непременно удалены, а помещения - проветрены. Главной мерой предупреждения скоплений метана в шахтах является наличие хорошей вентиляции. При индивидуальной защите необходимо применение шлемов с принудительной подачей воздуха или дыхательных аппаратов, снабженных запасом воздуха.
Молекулярная, структурная и электронная формула метана составляются на основе теории строения органических веществ Бутлерова. Прежде чем приступать к написанию таких формул, начнем с краткой характеристики данного углеводорода.
Особенности метана
Данное вещество является взрывоопасным, его еще именуют «болотным» газом. Специфический запах этого предельного углеводорода известен всем. В процессе сгорания от него не остается химических компонентов, оказывающих негативное воздействие на организм человека. Именно метан является активным участником образования парникового эффекта.
Физические свойства
Первый представитель гомологического ряда алканов был обнаружен учеными в атмосфере Титана и Марса. Учитывая тот факт, что метан связан с существованием живых организмов, появилась гипотеза о существовании жизни на этих планетах. На Сатурне, Юпитере, Нептуне, Уране, метан появился в качестве продукта химической переработки веществ неорганического происхождения. На поверхности нашей планеты его содержание незначительное.

Общая характеристика
Метан не имеет цвета, он легче воздуха почти в два раза, плохо растворяется в воде. В составе природного газа его количество достигает 98 процентов. В содержится от 30 до 90 процентов метана. В большей степени метан имеет биологическое происхождение.
Копытные травоядные козы и коровы испускают при переработке в желудках бактерий довольно существенное количество метана. Среди важных источников гомологического ряда алканов выделим болота, термитов, фильтрацию естественного газа, процесс фотосинтеза растений. При обнаружении на планете следов метана, можно говорить о существовании на ней биологической жизни.

Способы получения
Развернутая структурная формула метана является подтверждением того, что в его молекуле только насыщенные одинарные связи, образованные гибридными облаками. Среди лабораторных вариантов получения данного углеводорода отметим сплавление ацетата натрия с твердой щелочью, а также взаимодействие карбида алюминия с водой.
Горит метан голубоватым пламенем, выделяя при этом порядка 39 МДж на кубический метр. Взрывоопасные смеси данное вещество образует с воздухом. Наиболее опасен метан, который выделяется во время проведения подземных разработок месторождений полезных ископаемых в горных шахтах. Высок риск взрыва метана и на обогатительных угольных и брикетных фабриках, а также на сортировочных производствах.
Физиологическое действие
Если процентное содержание метана в воздухе составляет от 5 до 16 процентов, при попадании кислорода возможно воспламенение метана. В случае существенного возрастания в смеси данного химического вещества повышается вероятность взрыва.
Если в воздухе концентрация данного алкана составляет 43 процента, он является причиной удушья.
При взрыве скорость распространения составляет от 500 до 700 метров в секунду. После того как метан контактирует с источником тепла, процесс воспламенения алкана происходит с некоторым запаздыванием.
Именно на этом свойстве базируется производство взрывобезопасного электрического оборудования и предохранительных взрывчатых компонентов.
Так как именно метан является самым термически устойчивым он имеет широкое применение в виде промышленного и бытового топлива, а также используется в качестве ценного сырья для химического синтеза. Структурная формула три-этил-метана характеризует особенности строения представителей данного класса углеводородов.
В процессе его химического взаимодействия с хлором при воздействии ультрафиолетового облучения возможно образование нескольких продуктов реакции. В зависимости от количества исходного вещества, можно в ходе замещения получить хлорметан, хлороформ, четыреххлористый углерод.
В случае неполного сгорания метана образуется сажа. В случае каталитического окисления образуется формальдегид. Конечным продуктом взаимодействия с серой является сероуглерод.

Особенности структуры метана
Какова его структурная формула? Метан относится к предельным углеводородам, имеющим общую формулу С n Н 2n+2 . Рассмотрим особенности образования молекулы, чтобы пояснить, как образуется структурная формула.
Метан состоит из одного атома углерода и четырех атомов водорода, связанных между собой ковалентной полярной химической связью. Поясним на основе строения атома углерода структурные формулы.
Вид гибридизации
Пространственное строение метана характеризуется тетраэдрической структурой. Так как на внешнем уровне у углерода четыре валентных электрона, при нагревании атома происходит переход электрона со второй s-орбитали на p. В итоге на последнем энергетическом уровне у углерода располагается четыре неспаренных («свободных») электрона. Полная структурная формула метана основывается на том, что происходит образование четырех гибридных облаков, которые ориентируются в пространстве под углом 109 градусов 28 минут, формируя структуру тетраэдра. Далее происходит перекрывание вершин гибридных облаков с негибридными облаками атомов водорода.
Полная и сокращенная структурная формула метана в полной мере отвечает теории Бутлерова. Между углеродом и водородами образуется простая (одинарная) связь, поэтому для данного химического вещества не характерны реакции присоединения.
Ниже представлена конечная структурная формула. Метан - это первый представитель класса насыщенных углеводородов, он обладает типичными свойствами предельного алкана. Структурная и электронная формула метана подтверждают тип гибридизации атома углерода в данном органическом веществе.

Из школьного курса химии
Данный класс углеводородов, представителем которого является «болотный газ», изучается в курсе 10 класса средней школы. Например, ребятам предлагается задание следующего характера: «Напишите структурные формулы метана». Необходимо понимать, что для этого вещества можно расписать по теории Бутлерова только развернутую структурную конфигурацию.
Его сокращенная формула будет совпадать с молекулярной, записываться в виде СН4. По новым федеральным образовательным стандартам, которые введены в связи с реорганизацией российского образования, в базовом курсе химии все вопросы, касающиеся характеристики классов органических веществ, разбираются обзорно.
Промышленный синтез
На основе метана были разработаны промышленные способы такого важного химического компонента, как ацетилен. Основой термического и электрического крекинга стала именно его структурная формула. Метан при каталитическом окислении с аммиаком образует синильную кислоту.
Применяют данное органическое вещество для производства синтез-газа. При взаимодействии с водяным паром получается смесь угарного газа и водорода, являющаяся сырьем для производства предельных карбонильных соединений.
Особое значение имеет взаимодействие с азотной кислотой, в результате получается нитрометан.

Применение в виде автомобильного топлива
В связи с нехваткой природных источников углеводородов, а также оскудением сырьевой базы, особую актуальность приобретает вопрос, связанный с поиском новых (альтернативных) источников для получения топлива. Одним из таких вариантов является в составе которого есть и метан.
Учитывая разницу в плотности между бензиновым топливом и первым представителем класса алканов, существуют определенные особенности применения его в качестве источника энергии для автомобильных двигателей. Для того чтобы не было необходимости перевозить с собой огромное количества метана, путем сжатия его плотность увеличивают (при давлении порядка 250 атмосфер). Хранят метан в сжиженном состоянии в баллонах, устанавливаемых в автомобилях.
Воздействие на атмосферу
Выше уже шла речь о том, что метан оказывает воздействие на парниковый эффект. Если степень действия оксида углерода (4) на климат берется условно за единицу, то в нем доля «болотного газа» составляет 23 единицы. На протяжении двух последних столетий ученые наблюдают повышение количественного содержания метана в земной атмосфере.
На данный момент примерное количество СН 4 оценивается в 1,8 части на миллион. Несмотря на то что данный показатель в 200 раз меньше, чем наличие углекислого газа, идет разговор между учеными о возможном риске удержания тепла, излучаемого планетой.
В связи с отличной теплотворной способностью «болотного газа», его применяют не только в качестве исходного сырья при осуществлении химического синтеза, но и в качестве источника энергии.
Например, на метане функционируют разнообразные газовые котлы, колонки, предназначенные для индивидуальной отопительной системы в частных домах и загородных коттеджах.
Такой автономный вариант отопления весьма выгоден для собственников жилья, не связан с авариями, систематически происходящими на централизованных отопительных системах. Благодаря газовому котлу, функционирующему на данном виде топлива, достаточно 15-20 минут для того, чтобы полностью обогреть двухэтажный коттедж.

Заключение
Метан, структурные и молекулярные формулы которого были приведены выше, является природным источником энергии. Благодаря тому, что в его составе есть только атом углерода и атомы водорода, экологи признают экологическую безопасность данного насыщенного углеводорода.
При стандартных условиях (температуре воздуха 20 градусов по Цельсию, давлении 101325 Па) это вещество является газообразным, нетоксичным, нерастворимым в воде.
В случае понижения температуры воздуха до -161 градуса, происходит сжатие метана, что широко применяют в промышленности.
Метан оказывает воздействие на здоровье человека. Он не является отравляющим веществом, но считается удушающим газом. Существуют даже предельные нормы (ПДК) по содержанию данного химического вещества в атмосфере.
Например, работы в шахтах разрешены только в тех случаях, когда его количество не превышает на метр кубический 300 миллиграммов. Анализируя особенности строения данного органического вещества, можно сделать вывод о его сходстве по химическим и физическим свойствам со всеми другими представителями класса насыщенных (предельных) углеводородов.
Мы проанализировали структурные формулы, пространственное строение метана. который начинает "болотный газ", имеет общую молекулярную формулу С n Н 2n+2 .
Атом углерода в молекуле метана находится в состоянии sp3- гибридизации.В результате перекрывания четырёх гибридных орбиталей атома углерода с s-орбиталями атомов водоорда образуется весьма прочная молекула метана.
Метан-газ без цвета и запаха,легче воздуха,малорастворим в воде.Предельные углеводороды способны гореть,образуя оксид углерода (IV) и воду.Метан горит бледным синеватым пламенем: CH4+2O2=2H2O
В смеси с воздухом (или с кислородом,особенно в соотношении по объему 1:2, что видно из уравнения реакции) метан образует взрывчатые смеси.Поэтому он опасен как в быту (утечка газа через краны),так и в шахтах.При неполном сгорании метана образуется сажа.Так её получают в промышленных условиях.В присутствии катализаторов при окислении метана получают метиловый спирт и формальдегид
При сильном нагревании метан распадается по уравнению:CH4=C+2H2
В печах специальной конструкции распад метана может быть осуществлён до промежуточного продукта-ацителена:
2CH4=C2H 2+3H2
Для метана характерны реакции замещения.На свету или обычной температуре галогены-хлор и бром-постепенно (по стадиям) вытесняют из молекулы метана водород,образуя так называемые галогенопроизводные.Атомы хлора замещяют атомы водорода в ней с образованием смеси различных соединенний:
CH3Cl-хлорметана (хлористого метила),CH2Cl2-дихлорметана,CHCl3-трихлорметана,CCl4-тетрахлорметана
Из этой смеси каждое соединение может быть выделено.Важное значение имеют хлороформ итетрахлорметан как растворители смол,жиров,каучука и других органических веществ.
Образование галогенопроизводных метана протекают по цепному свободнорадикальному механизму.Под действием света молекулы хлора распадаются на неорганические радикалы:Cl2=2Cl
Неорганический радикал Cl отрывает от молекулы метана атом водорода с одним электроном,образуя HCl и свободный радикал CH3 H H
H:C_| H+Cl=H:C +HCl
H| H
Cвободный радикал взаимодействует с молекулой хлора Cl2 ,образуя галогенопроизводное и радикал хлора:
CH3+Cl_| Cl=CH3-Cl+Cl
Метан при обычной температуре обладает большей стойкостью к кислотам,щелочам и многим окислителям.Однако он вступает в реакцию с азотной кислотой:
CH4+HNO3=CH3NO2 +H2O
нитрометан
Метан не способен к реакциям присоединения,поскольку в его молекуле все валентности насыщены.
Приведенные реакции замещения сопровождаются разрывом связей C-H.Однако известны процессы,при которых происходит не только расщепление связей C-H,но и разрыв цепи углеродных атомов (у гомологов метана).Эти реакции протекают при высоких температурах и в присутствии катализаторов.Например:
C4H10+H2 -процесс дегидрогенизации
C4H10-|
C2H6 + C2H4-крекинг
Получение метана.
Метан широко распространён в природе.Он является главной составной частью многих горючих газов как природных (90-98%),так и искусственных,выделяющихся при сухой перегонке дерева,торфа,каменного угля,а также при крекинге нефти
Метан выделяется со дна болот и из каменноугольных пластов в рудниках,где он образуется при медленном разложении растительных остатков без доступа воздуха,Поэтому метан часто называют болотным газом или рудничным газом
В лабороторных условиях метан получают при нагревании смесси ацетата натрия с гидроксидом натрия:
200 *C
CH3|COONa +NaO|H=Na2CO3 + CH4|
или при взаимодействии карбида алюминия с водой:
Al4C3 +12H2O=4Al(OH)3 +3CH4|
В последнем случае метан получается весьма чистым.
Метан может быть получен из простых веществ при нагревании в присутствии катализатора: Ni
C+2H2=CH4
А также синтезом на основе водяного газа
Ni
CO+3H2 =CH4 +H2O
Гомологи метана,как и метан,в лабораторных условиях получают прокаливанием солей соответствующих органических кислот с щелочами.Другой способ-реакция Вюрца, т.е. нагревание моногалогенопроизводных с металлическим натрием,например
C2H5 |Br+2Na+Br|C2H5= C2H5-C2H5+2NaBr
В технике для получения синтетического бензина (смесь углеводородов,содержащих 6-10 атомов углерода) применяют синтез из оксида углерода (II) и водорода в присутствии катализатора (соединения кобальта) и при повышенном давлении.Процесс можно выразить уравнением:
200*С
nCO+(2n+1)H2=CnH2n+2+nH2O
Применение алканов
Благодаря большой теплотворной способности метан в больших количествах расходуется в качестве топлива (в быту-бытовой газ и в промешленности.Широко применяются получаемые из него вещества:водород,ацителен,сажа.Он служит исходным сырьём для получения формальдегида,метилового спирта,а также различных синтетических продуктов
Большое промышленное значение имеет окисление высших предельных углеводородов-парафинов с числом углеродных атомов 20-25.Этим путём получают синтетические жирные кислоты с различной длиной цепи,которые используются для производства мыл,различных моющих средств,смазочных материалов,лаков и эмалей.
Жидкие углеводороды используются как горючее (они входят в состав бензина и керосина).Алканы широко используются в органическом синтезе.
Физико-химические свойства метана.
Опасные примеси в рудничном воздухе
К ядовитым примесям рудничного воздуха относятся окись углерода, окислы азота, сернистый газ и сероводород.
Окись углерода (СО) – газ без цвета, вкуса и запаха с удельным весом 0,97. Горит и взрывается при концентрации от 12,5 до 75%. Температура воспламенения, при концентрации 30%, 630-810 0 С. Очень ядовит. Смертельная концентрация – 0,4%. Допустимая концентрация в горных выработках - 0,0017%. Основная помощь при отравлении – искусственное дыхание в выработке со свежим воздухом.
Источниками окиси углерода являются взрывные работы, работы двигателей внутреннего сгорания, рудничные пожары и взрывы метана и угольной пыли.
Окислы азота (NO) - имеют бурый цвет и характерный резкий запах. Очень ядовиты, вызывают раздражение слизистых оболочек дыхательных путей и глаз, отеки легких. Смертельная концентрация, при кратковременном вдыхании, - 0,025%. Предельное содержание оксидов азота в рудничном воздухе не должно превышать 0,00025% (в пересчете на двуокись – NO 2). Для диоксида азота – 0,0001%.
Сернистый газ (SO 2) – бесцветен, с сильным раздражающим запахом и кислым вкусом. Тяжелее воздуха в 2,3 раза. Очень ядовит: раздражает слизистые оболочки дыхательных путей и глаз, вызывает воспаление бронхов, отек гортани и бронхов.
Сернистый газ образуется при взрывных работах (в сернистых породах), пожарах, выделяется из горных пород.
Предельное содержание в рудничном воздухе – 0,00038%. Концентрация 0,05% - опасна для жизни.
Сероводород (H 2 S) – газ без цвета, со сладковатым вкусом и запахом тухлых яиц. Удельный вес – 1,19. Сероводород горит, а при концентрации 6% взрывается. Очень ядовит, раздражает слизистые оболочки дыхательных путей и глаз. Смертельная концентрация – 0,1%. Первая помощь при отравлении – искусственное дыхание на свежей струе, вдыхание хлора (с помощью платка, смоченного хлорной известью).
Сероводород выделяется из горных пород и минеральных источников. Образуется при гниении органических веществ, рудничных пожарах и взрывных работах.
Сероводород хорошо растворяется в воде. Это необходимо учитывать при передвижении людей по заброшенным выработкам.
Допустимое содержание H 2 S в рудничном воздухе не должно превышать 0,00071%.
Лекция 2
Метан и его свойства
Метан является основной, наиболее распространенной частью рудничного газа. В литературе и на практике, метан, чаще всего отождествляется с рудничным газом. В рудничной вентиляции этому газу уделяется наибольшее внимание из-за его взрывчатых свойств.
Физико-химические свойства метана.
Метан (СН 4) – газ без цвета, вкуса и запаха. Плотность – 0,0057. Метан инертен, но, вытесняя кислород (вытеснение происходит в следующей пропорции: 5 единиц объема метана замещают 1 единицу объема кислорода, т.е. 5:1), может представлять опасность для людей. Воспламеняется при температуре 650-750 0 С. С воздухом метан образует горючие и взрывчатые смеси. При содержании в воздухе до 5-6% горит у источника тепла, от 5-6% до 14-16% - взрывается, свыше 14-16% - не взрывается. Наибольшая сила взрыва при концентрации 9,5%.
Одно из свойств метана – запаздывание вспышки, после контакта с источником воспламенения. Время запаздывания вспышки называется идукционным периодом. Наличие этого периода создает условия для предупреждения вспышки при взрывных работах, применяя предохранительные взрывчатые вещества (ВВ).
Давление газа в месте взрыва примерно в 9 раз выше начального давления газо-воздушной смеси до взрыва. При этом может возникать давление до 30 ат и выше. Различные препятствия в выработках (сужения, выступы и т.д.) способствуют повышению давления и увеличивают скорость распространения взрывной волны в горных выработках.