Какие органические вещества. Классы органических соединений
Читайте также
Органические вещества, органические соединения - класс соединений, в состав которых входит углерод (за исключением карбидов, угольной кислоты, карбонатов, оксидов углерода и цианидов). Органические соединения обычно построены из цепочек атомов углерода, связанных между собой ковалентными связями, и различных заместителей, присоединенных к этим углеродным атомам
Органическая химия- это наука, изучающая состав, строение, физические и химические свойства органических веществ.
Органическими называют вещества, молекулы которых состоят из атомов углерода, водорода, кислорода, азота, серы и некоторых других элементов и содержат в своем составе С-С и С-Н связи. Причем наличие последних обязательно.
Органические вещества были известны человечеству с глубокой древности. Как самостоятельная наука, органическая химия возникла лишь в начале XIX века. В 1827г. шведский ученый Й.Я.Берцелиус опубликовал первое руководство по органическим веществам. Он был приверженцем модной в то время теории витализма, утверждавшей, что органические вещества образуются лишь в живых организмах под влиянием особой "жизненной силы".
Однако не все ученые-химики придерживались виталистических взглядов. Так еще в 1782г. К.В.Шееле, нагревая смесь аммиака, углекислого газа и угля, получил синильную кислоту, весьма распространенную в мире растений. В 1824-28гг. Ф.Велер путем химического синтеза получил щавелевую кислоту и мочевину.
Особое значение для окончательного развенчания теории витализма имели проведенные к началу 60-х годов синтезы различных органических веществ. В 1842г. Н.И.Зинин получил анилин, в 1845г. А.Кольбе - уксусную кислоту, в 1854г. М.Бертло разработал метод получения синтетического жира, а в 1861г. А.М.Бутлеров синтезировал сахаристое вещество.
С крахом теории витализма была стерта грань, отделяющая органические вещества от неорганических. И все же, для органических веществ характерен ряд специфических особенностей. К таковым в первую очередь следует отнести их многочисленность. В настоящее время человечеству известно более 10 млн. веществ, из них около 70% относятся к органическим.
Основными причинами многочисленности органических веществ считаются явления гомологии и изомерии.
Гомология - это явление существования ряда веществ, имеющих одинаковый качественный состав, сходное строение, а по количественному составу различающиеся на одну или несколько групп CH2, называемыхгомологической разностью.
Изомерия - это явление существования ряда веществ, имеющих одинаковый качественный и количественный состав, но различное строение молекул, проявляющих различные физические свойства и химическую активность.
Молекулы органических веществ состоят в основном из атомов неметаллов, связанных слабополярными ковалентными связями. Поэтому в зависимости от числа атомов углерода в молекуле они представляют собой газообразные, жидкие или низкоплавкие твердые вещества. Кроме того, молекулы органических веществ обычно содержат атомы углерода и водорода в неокисленной или малоокисленной форме, поэтому они легко окисляются с выделением большого количества теплоты, что приводит к воспламенению.
Видеоурок:
Лекция: Классификация органических веществ. Номенклатура органических веществ (тривиальная и международная)
Классификация органических веществ
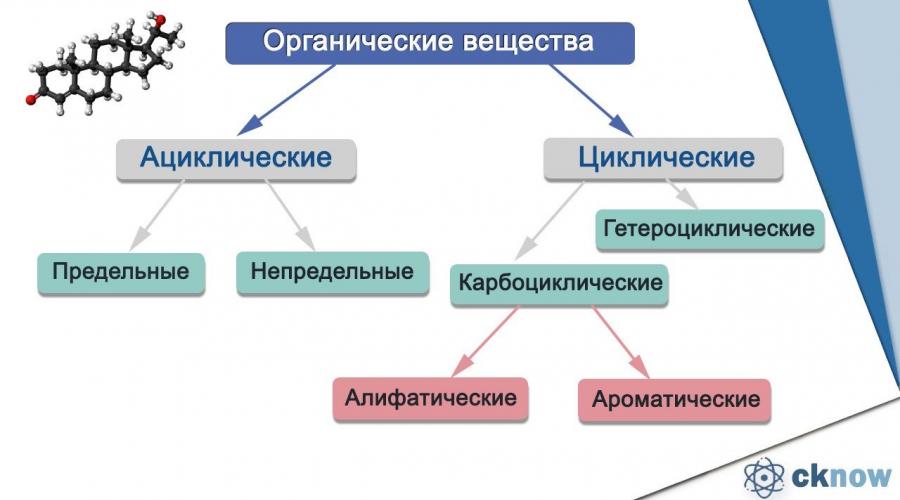
В основе классификации органических веществ лежит теория А.М. Бутлерова. В таблице показана классификация органических веществ в зависимости от типа строения углеродной цепи, т.е. по типу углеродного скелета:

Ациклические соединения - это органические вещества, в молекулах которых атомы углерода соединены друг с другом в прямые, а так же разветвленные открытые цепи.
К ациклическим, например, относится этан:

или ацетилен:

Иначе подобные соединения называются алифатическими или соединениями жирного ряда, потому что первые соединения данного ряда органических веществ были получены из растительных или животных жиров. Из ациклических соединений выделяются:
Предельные (или насыщенные) - данные соединения содержат в углеродном скелете одинарные ковалентные неполярные углерод-углеродные С-С и слабополярные С-Н связи, это алканы .
Общая молекулярная формула алканов - C n H 2n+2 , где n - количество атомов углерода в молекуле углеводорода. К ним относятся открытые цепи, а также замкнутые (циклические) углеводороды. Все атомы углерода в алканах имеют sp 3 - гибридизацию . Запомните следующие алканы:
Метан - СH 4
Этан - C 2 H 6: CH 3 -CH 3
Пропан - C 3 H 8: CH 3 -CH 2 -CH 3
Бутан - C 4 H 10: CH 3 -(CH 2) 2 -CH 3
Пентан - C 5 H 12: CH 3 -(CH 2) 3 -CH 3
Гексан - C 6 H 14: CH 3 -(CH 2) 4 -CH 3
Гептан - C 7 H 16: CH 3 -(CH 2) 5 -CH 3
Октан - C 8 H 18: CH 3 -(CH 2) 6 -CH 3
Нонан - C 9 H 20: CH 3 -(CH 2) 7 -CH 3
Декан - C 10 H 22: CH 3 -(CH 2) 8 -CH 3
Непредельные (или ненасыщенные) - содержат кратные - двойные (С=С) или тройные (С≡С) связи, это алкены, алкины и алкадиены:
1) А лкены - содержат одну углерод-углеродную связь, которая является двойной C=C. Общая формула - C n H 2n . Атомы углерода в данных соединениях имеют sp 2 - гибридизацию . Связь C=C имеет π-связь и σ-связь, поэтому алкены более химически активны, чем алканы. Запомните следующие алкены:
Этен (этилен) - C 2 H 4: CH 2 =CH 2
Пропен (пропилен) - C 3 H 6: СН 2 =СН-СН 3
Бутен - С 4 Н 8: бутен-1 СН 3 -СН 2 -СН=СН, бутен-2 СН 3 -СН=СН-СН 3 , изобутен [СН 3 ] 2 С=СН 2
Пентен - C 5 H 10: 1-пентен CH 3 -CH 2 -CH 2 -CH=CH 2 , 2-пентен C 2 H 5 CH=CHCH 3
Гексен - C 6 H 12: 1-гексен CH 2 =CH-CH 2 -CH 2 -CH 2 -CH 3 , цис- гексен-2 CH 3 -CH=CH-CH 2 -CH 2 -CH 3 и другие изомеры.
Гептен - C 7 H 14: 1-гептен СН 2 =СН-СН 2 -СН-СН 2 -СН 2 -СН 3 , 2-гептен СН 3 -СН=СН-СН 2 -СН 2 -СН 2 -СН 3 и др.
Октен - C 8 H 16: 1-октен СН 2 =СН-СН 2 -СН 2 -СН 2 -СН 2 -СН 2 -СН 3 , 2-октен СН 3 -СН=СН-СН 2 -СН 2 -СН 2 -СН 2 -СН 3 и др.
Нонен - C 9 H 18: 3-нонен CH 3 -CH 2 -CH=CH-CH 2 -CH 2 -CH 2 -CH 2 -CH 3 , 5-нонен CH 3 -CH 2 -CH 2 -CH 2 -CH=CH-CH 2 -CH 2 -CH 3 и др.
Децен - C 10 H 20: 2-децен СН 3 -СН 2 -СН 2 -СН 2 -СН 2 -СН 2 -СН 2 -СН=СН-СН 3 и др.
Как вы заметили, названия алкенов схожи с названиями алканов, с разницей суффикса. Названия алканов имеют суффикс -ан , а алкенов суффикс -ен . Кроме того среди перечисленных алкенов отсутствует метен. Запомните, метена не существует, потому что метан имеет только один углерод. А для образования алкенов, обязательно образование двойных связей.
Местоположение двойной связи обозначается цифрой, например, 1-бутен: СН 2 =СН–СН 2 –СН 3 или 1-гексен: СН 3 –СН 2 –СН 2 –СН 2 –СН=СН 2 . Обратите внимание на данное правило: нумерация углеводородных цепей должна производиться так, чтобы двойные связи находились под наименьшим номером, например, 2-гексен:
2) А лкины – в молекулах присутствует одна тройная С≡С связь. Общая формула - C n H 2n-2 . В названиях алкинов суффикс -ан заменен на -ин. Например, 3-гептин: СН 3 –СН 2 –СН 2 –С≡С–СН 2 –СН 3 . Для этина НС≡СН возможно и тривиальное название ацетилен. Указание положения тройной связи производится также как в предыдущем случае с алкенами. Если в соединении тройных связей больше одной, то к названию прибавляется суффикс -диин или -триин . Если же в соединении присутствуют и двойные, и тройные связи, то их нумерацию определяет двойная связь, следовательно, называют сначала двойную, затем тройную связи. Например, гексадиен-1,3-ин-5: СН 2 =СН–СН 2 =СН 2 –С≡СН.
3) А л кадиены – в молекулах присутствуют две двойные С=С связи. Общая формула - C n H 2n-2, такая же, как и у алкинов. Алкины и алкадиены относятся к межклассовым изомерам. К примеру, 1,3-бутадиен или дивинил C 4 H 6: СН 2 =СН-СН=СН 2 .
Циклические соединения - это органические вещества , в молекулах которых содержится три или более связанных в замкнутое кольцо атомов, образующих циклы.

Предельные циклические углеводороды называются циклоалканами. Их о бщая формула - C n H 2n . В молекулах имеется замкнутая цепь или кольца. К примеру, циклопропан (C 3 H 6):

и циклобутан (C 4 H 8):

В зависимости от того, какими атомами были образованы циклы, данный вид соединений подразделяется на карбоциклические и гетероциклические.
Карбоциклические , которые иначе называются гомоциклическими, содержат в циклах только атомы углерода. В свою очередь, они делятся на алифатические и ароматические.
Алициклические (алифатические) соединения отличаются тем, что атомы углерода могут соединяться между собой в прямые, разветвлённые цепочки или кольца одинарными, двойными или тройными связями.
Типичным алифатическим соединением является циклогексен:

Ароматические соединения получили свое название благодаря ароматному запаху вещества. Иначе называются аренами. Они отличаются наличием в соединении бензольного кольца:
Таких колец в составе может быть несколько. Например, нафталин:

Также данная группа соединений имеет в составе ароматическую систему, что характеризует высокую устойчивость и стабильность соединения. Ароматичная система, содержит в кольце 4n+2 электронов (где n = 0, 1, 2, …). Данной группе органических веществ свойственно вступать в реакции замещения, а не присоединения.
Ароматические соединения могут иметь функциональную группу, прикрепленную непосредственно к кольцу. Например, толуол:
Гетероциклические соединения всегда содержат в составе углеводородного цикла один или несколько гетероатомов, которыми являются атомы кислорода, азота или серы. Если гетероатомов пять, то соединения называются пятичленными, если шесть, соответственно шестичленными. Примером гетероциклического соединения является пиридин:

Классификация производных углеводорода
Другие органические вещества рассматривают исключительно как производные углеводородов, которые образуются при введении в молекулы углеводородов функциональных групп, включающих в себя другие химические элементы. Формулу соединений, имеющих одну функциональную группу, можно записать как R - X . Где R – углеводородный радикал (фрагмент молекулы углеводорода без одного или нескольких атомов водорода; Х – функциональная группа. По наличию функциональных групп углеводороды подразделяются на:
Галогенпроизводные - судя из названия ясно, что в данных соединениях атомы водорода замещены на атомы какого-либо галогена.
Спирты и фенолы. В спиртах атомы водорода замещены на гидроксильную группу -OH. По количеству таких групп, спирты подразделяются на одноатомные и многоатомные, среди которых двухатомные, трехатомные и т.д.
Формула одноатомных спиртов: C n H 2n +1OH или C n H 2n +2O .
Формула многоатомных спиртов: C n H 2n +2O x ; x – атомность спирта.
Спирты могут быть и ароматическими. Формула одноатомных ароматических спиртов: C n H 2n -6O .
Следует помнить, что производные ароматических углеводородов, в которых на гидроксильные группы заменены один/несколько атомов водорода не относятся к спиртам. Данный тип относят к классу фенолов. Причина, по которой фенолы не относят к спиртам, содержится в их специфических химических свойствах. Одноатомные фенолы изомерны одноатомным ароматическим спиртам. То есть они так же имеют общую молекулярную формулу C n H 2n -6O .
Амины - производные аммиака, в которых один, два или три атома водорода заменены на углеводородный радикал. Амины, в которых только один атом водорода замещен на углеводородный радикал, то есть имеющие общую формулу R-NH 2 , именуют первичными аминами. Амины, в которых, два атома водорода заменены на углеводородные радикалы, именуют вторичными. Их формула - R-NH-R’ . Следует помнить, что радикалы R и R’ могут быть как одинаковые, так и разные. Если все три атома водорода молекулы аммиака замещены на углеводородный радикал, то амины являются третичными. При этом R, R’, R’’ могут быть как полностью одинаковыми, так и разными. Общая формула первичных, вторичных и третичных предельных аминов - C n H 2n +3N . Ароматические амины с одним непредельным заместителем имеют формулу C n H 2n -5N.
Альдегиды и кетоны. У альдегидов при первичном атоме углерода два атома водорода замещены на один атом кислорода. То есть в их структуре имеется альдегидная группа – СН=О. Общая формула - R-CH=O . У кетонов при вторичном атоме углерода два атома водорода замещены на атом кислорода. То есть это соединения, в структуре которых есть карбонильная группа –C(O)-. Общая формула кетонов: R-C(O)-R ’. При этом радикалы R, R’ могут быть как одинаковыми, так и разными. Альдегиды и кетоны достаточно схожи по строению, но их все-таки различают как классы, так как они имеют существенные различия в химических свойствах. Общая формула предельных кетонов и альдегидов имеет вид: C n H 2n O .
Карбоновые кислоты содержат карбоксильную группу –COOH. В случае, когда кислота содержит две карбоксильные группы, такую кислоту именуют дикарбоновой кислотой. Предельные монокарбоновые кислоты (с одной группой -COOH) имеют общую формулу - C n H 2n O 2 . Ароматические монокарбоновые кислоты имеют общую формулу C n H 2n -8O 2 .
Простые эфиры – органические соединения, в которых два углеводородных радикала опосредованно соединены через атом кислорода. То есть, имеют формулу вида: R-O-R’ . При этом радикалы R и R’ способны быть как одинаковыми, так и разными. Формула предельных простых эфиров - C n H 2n +1OH или C n H 2n +2О .
Сложные эфиры – класс соединений на основе органических карбоновых кислот, у которых атом водорода в гидроксильной группе заменен на углеводородный радикал R.
Нитросоединения – производные углеводородов, в которых один или несколько атомов водорода замещены на нитрогруппу –NO 2 . Предельные нитросоединения с одной нитрогруппой имеют формулу C n H 2n +1NO 2 .
Аминокислоты имеют в структуре одновременно две функциональные группы – амино NH 2 и карбоксильную – COOH. Например: NH 2 -CH 2 -COOH. Предельные аминокислоты, имеющие одну карбоксильную и одну аминогруппу изомерны соответствующим предельными нитросоединениям то есть, имеют общую формулу C n H 2n +1NO 2 .
Номенклатура органических соединений
Номенклатура соединения делится на 2 типа:
тривиальную и
систематическую.
Тривиальная - это исторически первая номенклатура, возникшая в самом начале развития органической химии. Названия веществ носили ассоциативный характер, например, щавелевая кислота, мочевина, индиго.
Создание систематической, т.е. международной номенклатуры началось с 1892 года. Тогда была начата Женевская номенклатура, которую с 1947 и по сегодняшний день продолжает ИЮПАК (IUPAC - международная единая химическая номенклатура). Согласно систематической номенклатуре названия органических соединений составляются из корня, обозначающего длину основной цепи, т.е. соединенных в неразветвленную цепь атомов углеродов, а также приставок и суффиксов, обозначающих наличие и расположение заместителей, функциональных групп и кратных связей.
Систематическая номенклатура алкановСистематическая номенклатура алкенов
В настоящее время известно более 10 млн органических соединений. Такое громадное количество соединений требует строгой классификации и единых международных номенклатурных правил. Этому вопросу уделяется особое внимание в связи с использованием компьютерных технологий для создания разнообразных баз данных.
1.1. Классификация
Строение органических соединений описывается с помощью структурных формул.
Структурной формулой называют изображение последовательности связывания атомов в молекуле при помощи химических символов.
С понятием последовательности соединения атомов в молекуле непосредственно связано явление изомерии, т. е. существования соединений одинакового состава, но различного химического стро- ения, называемых структурными изомерами (изомеры строения). Важнейшей характеристикой большинства неорганических соединений служит состав, выражаемый молекулярной формулой, например хлороводородная кислота HC1, серная кислота H 2 SO 4. Для органи- ческих соединений состав и соответственно молекулярная формула не являются однозначными характеристиками, так как одному и тому же составу может соответствовать много реально существующих соединений. Например, структурные изомеры бутан и изобутан, имея одинаковую молекулярную формулу С 4 Н 10, различаются последовательностью связывания атомов и имеют разные физико-химические характеристики.

Первым классификационным критерием служит деление органических соединений на группы с учетом строения углеродного скелета (схема 1.1).
Схема 1.1. Классификация органических соединений по строению углеродного скелета

Ациклические соединения - это соединения с незамкнутой цепью атомов углерода.
Алифатические (от греч. a leiphar - жир) углеводороды - простейшие представители ациклических соединений - содержат только атомы углерода и водорода и могут быть насыщенными (алканы) и ненасыщенными (алкены, алкадиены, алкины). Их структурные формулы часто записывают в сокращенном (сжатом) виде, как показано на примере н -пентана и 2,3-диметилбутана. При этом обозначение одинарных связей опускают, а одинаковые группы заключают в скобки и указывают число этих групп.
Углеродная цепь может быть неразветвленной (например, в н-пентане) и разветвленной (например, в 2,3-диметилбутане и изопрене).

Циклические соединения - это соединения с замкнутой цепью атомов.
В зависимости от природы атомов, составляющих цикл, различают карбоциклические и гетероциклические соединения.
Карбоциклические соединения содержат в цикле только атомы углерода и делятся на ароматические и алициклические (циклические неароматические). Число атомов углерода в циклах может быть различным. Известны большие циклы (макроциклы), состоящие из 30 атомов углерода и более.
Для изображения циклических структур удобны скелетные формулы, в которых опускают символы атомов углерода и водорода, но символы остальных элементов (N, O, S и др.) указывают. В таких

формулах каждый угол многоугольника означает атом углерода с необходимым числом атомов водорода (с учетом четырехвалентности атома углерода).
Родоначальником ароматических углеводородов (аренов) является бензол. Нафталин, антрацен и фенантрен относятся к полициклическим аренам. Они содержат конденсированные бензольные кольца.

Гетероциклические соединения содержат в цикле, кроме атомов углерода, один или несколько атомов других элементов - гетероатомов (от греч. heteros - другой, иной): азот, кислород, серу и др.

Большое многообразие органических соединений можно рассматривать в целом как углеводороды или их производные, полученные путем введения в структуру углеводородов функциональных групп.
Функциональная группа - это гетероатом или группа атомов неуглеводородного характера, определяющие принадлежность соеди- нения к определенному классу и ответственных за его химические свойства.
Вторым, более существенным классификационным критерием, служит деление органических соединений на классы в зависимости от природы функциональных групп. Общие формулы и названия важнейших классов приведены в табл. 1.1.
Соединения с одной функциональной группой называют монофункциональными (например, этанол), с несколькими одинаковыми функциональными группами - полифункциональными (например,
Таблица 1.1. Важнейшие классы органических соединений

* К функциональным группам иногда причисляют двойную и тройную связи.
** Применяемое иногда название тиоэфиры использовать не следует, так как оно
относится к серосодержащим сложным эфирам (см. 6.4.2).
глицерин), с несколькими разными функциональными группами - гетерофункциональными (например, коламин).
Соединения каждого класса составляют гомологический ряд, т. е. группу родственных соединений с однотипной структурой, каждый последующий член которого отличается от предыдущего на гомологическую разность СН 2 в составе углеводородного радикала. Например, ближайшими гомологами являются этан С 2 Н 6 и пропан С з Н 8 , метанол
СН 3 ОН и этанол СН 3 СН 2 ОН, пропановая СН 3 СН 2 СООН и бутановая СН 3 СН 2 СН 2 СООН кислоты. Гомологи обладают близкими химическими свойствами и закономерно изменяющимися физическими свойствами.
1.2. Номенклатура
Номенклатура представляет собой систему правил, позволяющих дать однозначное название каждому индивидуальному соединению. Для медицины знание общих правил номенклатуры имеет особенно большое значение, так как в соответствии с ними строятся названия многочисленных лекарственных средств.
В настоящее время общепринята систематическая номенклатура ИЮПАК (IUPAC - Международный союз теоретической и прикладной химии)*.
Однако до сих пор сохраняются и широко применяются (особенно в медицине) тривиальные (обыденные) и полутривиальные названия, использовавшиеся еще до того, как становилось известным строение вещества. В этих названиях могут отражаться природные источники и способы получения, особо заметные свойства и области применения. Например, лактоза (молочный сахар) выделена из молока (от лат. lactum - молоко), пальмитиновая кислота - из пальмового масла, пировиноградная кислота получена при пиролизе виноградной кислоты, в названии глицерина отражен его сладкий вкус (от греч. glykys - сладкий).
Тривиальные названия особенно часто имеют природные соединения - аминокислоты, углеводы, алкалоиды, стероиды. Употребление некоторых укоренившихся тривиальных и полутривиальных названий разрешается правилами ИЮПАК. К таким названиям относятся, например, «глицерин» и названия многих широко известных ароматических углеводородов и их производных.
* Номенклатурные правила ИЮПАК по химии. Т. 2. - Органическая химия/пер. с англ. - М.: ВИНИТИ, 1979. - 896 с.; Хлебников А.Ф., Новиков М.С. Современная номенклатура органических соединений, или Как правильно называть органические вещества. - СПб.: НПО «Профессионал», 2004. - 431 с.
В тривиальных названиях дизамещенных производных бензола взаимное расположение заместителей в кольце обозначается префиксами орто- (о-) - для групп, находящихся рядом, мета- (м-) - через один атом углерода и пара- (п-) - напротив. Например:
Для использования систематической номенклатуры ИЮПАК необходимо знать содержание следующих номенклатурных терминов:
Органический радикал;
Родоначальная структура;
Характеристическая группа;
Заместитель;
Локант.
Органический радикал* - остаток молекулы, из которой удаляются один или несколько атомов водорода и при этом остаются свободными одна или несколько валентностей.
Углеводородные радикалы алифатического ряда имеют общее название - алкилы (в общих формулах обозначаются R), радикалы ароматического ряда - арилы (Ar). Два первых представителя алканов - метан и этан - образуют одновалентные радикалы метил СН 3 - и этил СН 3 СН 2 -. Названия одновалентных радикалов обычно образуются при замене суффикса -ан суффиксом -ил.
Атом углерода, связанный только с одним атомом углерода (т. е. концевой), называют первичным, с двумя - вторичным, с тремя - третичным, с четырьмя - четвертичным.

* Этот термин не следует путать с термином «свободный радикал», который характеризует атом или группу атомов с неспаренным электроном.
Каждый последующий гомолог из-за неравноценности атомов углерода образует несколько радикалов. При удалении атома водорода от концевого атома углерода пропана получают радикал н -пропил (нормальный пропил), а от вторичного атома углерода - радикал изопропил. Бутан и изобутан каждый образуют по два радикала. Буква н- (которую разрешается опускать) перед названием радикала указывает, что свободная валентность находится на конце неразветвленной цепи. Префикс втор- (вторичный) означает, что свободная валентность находится у вторичного атома углерода, а префикс трет- (третичный) - у третичного.

Родоначальная структура - химическая структура, составляющая основу называемого соединения. В ациклических соединениях в качестве родоначальной структуры рассматривается главная цепь атомов углерода, в карбоциклических и гетероциклических соединениях - цикл.
Характеристическая группа - функциональная группа, связанная с родоначальной структурой или частично входящая в ее состав.
Заместитель - любой атом или группа атомов, замещающие в ор- ганическом соединении атом водорода.

Локант (от лат. locus - место) цифра или буква, указывающая положение заместителя или кратной связи.
Наиболее широко применяются два вида номенклатуры: заместительная и радикально-функциональная.
1.2.1. Заместительная номенклатура
Общая конструкция названия по заместительной номенклатуре представлена на схеме 1.2.
Схема 1.2. Общая конструкция названия соединения по заместительной номенклатуре

Название органического соединения представляет собой сложное слово, включающее название родоначальной структуры (корень) и названия разного типа заместителей (в виде префиксов и суффиксов), отражающих их природу, местонахождение и число. Отсюда и название этой номенклатуры - заместительная.
Заместители подразделяются на два типа:
Углеводородные радикалы и характеристические группы, обозначаемые только префиксами (табл. 1.2);
Характеристические группы, обозначаемые как префиксами, так и суффиксами в зависимости от старшинства (табл. 1.3).
Для составления названия органического соединения по заместительной номенклатуре используют приводимую ниже последовательность правил.
Таблица 1.2. Некоторые характеристические группы, обозначаемые только префиксами

Таблица 1.3. Префиксы и суффиксы, применяемые для обозначения важнейших характеристических групп

* Атом углерода, отмеченный цветом, включается в состав родоначальной структуры.
** Большинство фенолов имеет тривиальные названия.
Правило 1. Выбор старшей характеристической группы. Выявляют все имеющиеся заместители. Среди характеристических групп определяют старшую группу (если она присутствует), используя шкалу старшинства (см. табл. 1.3).
Правило 2. Определение родоначальной структуры. В качестве родо- начальной структуры в ациклических соединениях используют главную цепь атомов углерода, а в карбоциклических и гетероциклических соединениях - основную циклическую структуру.
Главную цепь атомов углерода в ациклических соединениях выбирают по приведенным ниже критериям, причем каждый последую- щий критерий используют, если предыдущий не приводит к однозначному результату:
Максимальное число характеристических групп, обозначаемых как префиксами, так и суффиксами;
Максимальное число кратных связей;
Максимальная длина цепи атомов углерода;
Максимальное число характеристических групп, обозначаемых только префиксами.
Правило 3. Нумерация родоначальной структуры. Родоначальную структуру нумеруют так, чтобы старшая характеристическая группа получила наименьший локант. Если выбор нумерации неоднозначен, то применяют правило наименьших локантов, т. е. нумеруют так, чтобы заместители получили наименьшие номера.
Правило 4. Название блока родоначальной структуры со старшей характеристической группой. В названии родоначальной структуры степень насыщенности отражают суффиксами: -ан в случае насыщенного углеродного скелета, -ен - при наличии двойной и -ин - тройной связи. К названию родоначальной структуры присоединяют суффикс, обозначающий старшую характеристическую группу.
Правило 5. Названия заместителей (кроме старшей характеристической группы). Дают название заместителям, обозначаемым префиксами в алфавитном порядке. Положение каждого заместителя и каждой кратной связи указывают цифрами, соответствующими номеру атома углерода, с которым связан заместитель (для кратной связи указывают только наименьший номер).
В русской терминологии цифры ставят перед префиксами и после суффиксов, например, 2-аминоэтанол H 2 NCH 2 CH 2 OH, бутадиен-1,3
СН 2 =СН-СН=СН 2 , пропанол-1 СН 3 СН 2 СН 2 ОН.
Для иллюстрации этих правил ниже приведены примеры построения названий ряда соединений в соответствии с общей схемой 1.2. В каждом случае отмечены особенности строения и способ их отражения в названии.
Схема 1.3. Построение систематического названия фторотана

2- бромо-1,1,1-трифторо-2-хлороэтан (средство для ингаляционного наркоза)
При наличии в соединении нескольких одинаковых заместителей при одном и том же атоме углерода локант повторяют столько раз, сколько имеется заместителей, с добавлением соответствующего умножающего префикса (схема 1.3). Заместители перечисляют по алфавиту, причем умножающий префикс (в данном примере - три-) в алфавитном порядке не учитывают. Схема 1.4. Построение систематического названия цитраля

После суффикса -аль, как и для сочетания -овая кислота, можно не указывать положение характеристических групп, так как они всегда находятся в начале цепи (схема 1.4). Двойные связи отражают суффиксом -диен с соответствующими локантами в названии родоначальной структуры.
Суффиксом обозначают старшую из трех характеристических групп (схема 1.5); остальные заместители, включая нестаршие характеристические группы, перечисляют по алфавиту как префиксы.
Схема 1.5. Построение систематического названия пеницилламина

Схема 1.6. Построение систематического названия щавелевоуксусной кислоты

оксобутандиовая кислота (продукт углеводного обмена)
Умножающий префикс ди- перед сочетанием -овая кислота указывает на наличие двух старших характеристических групп (схема 1.6). Локант перед оксо- опущен, так как иное положение оксогруппы соответствует той же структуре.
Схема 1.7. Построение систематического названия ментола

Нумерацию в цикле ведут от атома углерода, с которым связана старшая характеристическая группа (ОН) (схема 1.7), несмотря на то, что наименьший набор локантов всех заместителей в кольце может быть 1,2,4-, а не 1,2,5- (как в рассматриваемом примере).
Схема 1.8. Построение систематического названия пиридоксаля
I Заместители: ГВДРОКСИМЕТИЛ,ГИДРОКСИ, МЕТИЛ I

Альдегидную группу, атом углерода которой не включен в родоначальную структуру (схема 1.8), обозначают суффиксом -карбаль- дегид (см. табл. 1.3). Группу -СН 2 ОН рассматривают как составной заместитель и называют «гидроксиметил», т. е. метил, в котором в свою очередь произведено замещение атома водорода гидроксильной группой. Другие примеры составных заместителей: диметиламино- (CH 3) 2 N-, этокси- (сокращение от этилокси) С 2 Н 5 О-.
1.2.2. Радикально-функциональная номенклатура
Радикально-функциональная номенклатура используется реже, чем заместительная. В основном она применяется для таких классов органических соединений, как спирты, амины, простые эфиры, сульфиды и некоторых других.
Для соединений с одной функциональной группой общее название включает название углеводородного радикала, а наличие функцио- нальной группы отражают опосредованно через название соответствующего класса соединений, принятого в этом виде номенклатуры (табл. 1.4).
Таблица 1.4. Названия классов соединений, используемые в радикальнофункциональной номенклатуре*

1.2.3. Построение структуры по систематическому названию
Изображение структуры по систематическому названию представляется обычно более легкой задачей. Сначала записывают родо- начальную структуру - открытую цепь или цикл, затем нумеруют атомы углерода и расставляют заместители. В заключение дописывают атомы водорода с условием, чтобы каждый атом углерода оказался четырехвалентным.
В качестве примера приводится построение структур лекарственного средства ПАСК (сокращение от пара-аминосалициловой кислоты, систематическое название - 4-амино-2-гидроксибензойная кислота) и лимонной (2-гидроксипропан-1,2,3-трикарбоновой) кислоты.
4-Амино-2-гидроксибензойная кислота
Родоначальная структура - тривиальное название цикла со старшей характеристической
группой (СООН):

Расстановка заместителей - группа у атома С-4 и группа ОН у атома С-2:
2-Гидроксипропан-1,2,3-трикарбоновая кислота
Главная углеродная цепь и нумерация:
Расстановка заместителей - три группы СООН (-трикарбоновая кислота) и группа ОН у атома С-2:
Дополнение атомами водорода:


Следует заметить, что в систематическом названии лимонной кислоты в качестве родоначальной структуры выбран пропан, а не более длинная цепь - пентан, так как в пятиуглеродную цепь невозможно включить атомы углерода всех карбоксильных групп.
В прошлом ученые разделяли все вещества в природе на условно неживые и живые, включая в число последних царство животных и растений. Вещества первой группы получили название минеральных. А те, что вошли во вторую, стали называть органическими веществами.
Что под этим подразумевается? Класс органических веществ наиболее обширный среди всех химических соединений, известных современным ученым. На вопрос, какие вещества органические, можно ответить так – это химические соединения, в состав которых входит углерод.
Обратите внимание, что не все углеродсодержащие соединения относятся к органическим. Например, корбиды и карбонаты, угольная кислота и цианиды, оксиды углерода не входят в их число.
Почему органических веществ так много?
Ответ на этот вопрос кроется в свойствах углерода. Этот элемент любопытен тем, что способен образовывать цепочки из своих атомов. И при этом углеродная связь очень стабильная.
Кроме того, в органических соединениях он проявляет высокую валентность (IV), т.е. способность образовывать химические связи с другими веществами. И не только одинарные, но также двойные и даже тройные (иначе – кратные). По мере возрастания кратности связи цепочка атомов становится короче, а стабильность связи повышается.
А еще углерод наделен способностью образовывать линейные, плоские и объемные структуры.
Именно поэтому органические вещества в природе так разнообразны. Вы легко проверите это сами: встаньте перед зеркалом и внимательно посмотрите на свое отражение. Каждый из нас – ходячее пособие по органической химии. Вдумайтесь: не меньше 30% массы каждой вашей клетки – это органические соединения. Белки, которые построили ваше тело. Углеводы, которые служат «топливом» и источником энергии. Жиры, которые хранят запасы энергии. Гормоны, которые управляют работой органов и даже вашим поведением. Ферменты, запускающие химические реакции внутри вас. И даже «исходный код», цепочки ДНК – все это органические соединения на основе углерода.
Состав органических веществ
Как мы уже говорили в самом начале, основной строительный материал для органических веществ – это углерод. И практические любые элементы, соединяясь с углеродом, могут образовывать органические соединения.
В природе чаще всего в составе органических веществ присутствуют водород, кислород, азот, сера и фосфор.
Строение органических веществ
Многообразие органических веществ на планете и разнообразие их строения можно объяснить характерными особенностями атомов углерода.
Вы помните, что атомы углерода способны образовывать очень прочные связи друг с другом, соединяясь в цепочки. В результате получаются устойчивые молекулы. То, как именно атомы углерода соединяются в цепь (располагаются зигзагом), является одной из ключевых особенностей ее строения. Углерод может объединяться как в открытые цепи, так и в замкнутые (циклические) цепочки.
Важно и то, что строение химических веществ прямо влияет на их химические свойства. Значительную роль играет и то, как атомы и группы атомов в молекуле влияют друг на друга.
Благодаря особенностям строения, счет однотипным соединениям углерода идет на десятки и сотни. Для примера можно рассмотреть водородные соединения углерода: метан, этан, пропан, бутан и т.п.
Например, метан – СН 4 . Такое соединение водорода с углеродом в нормальных условиях пребывает в газообразном агрегатном состоянии. Когда же в составе появляется кислород, образуется жидкость – метиловый спирт СН 3 ОН.
Не только вещества с разным качественным составом (как в примере выше) проявляют разные свойства, но и вещества одинакового качественного состава тоже на такое способны. Примером могут служить различная способность метана СН 4 и этилена С 2 Н 4 реагировать с бромом и хлором. Метан способен на такие реакции только при нагревании или под ультрафиолетом. А этилен реагирует даже без освещения и нагревания.
Рассмотрим и такой вариант: качественный состав химических соединений одинаков, количественный – отличается. Тогда и химические свойства соединений различны. Как в случае с ацетиленом С 2 Н 2 и бензолом С 6 Н 6 .
Не последнюю роль в этом многообразии играют такие свойства органических веществ, «завязанные» на их строении, как изомерия и гомология.
Представьте, что у вас есть два на первый взгляд идентичных вещества – одинаковый состав и одна и та же молекулярная формула, чтобы описать их. Но строение этих веществ принципиально различно, откуда вытекает и различие химических и физических свойств. К примеру, молекулярной формулой С 4 Н 10 можно записать два различных вещества: бутан и изобутан.

Речь идет об изомерах – соединениях, которые имеют одинаковый состав и молекулярную массу. Но атомы в их молекулах расположены в различном порядке (разветвленное и неразветвленное строение).
Что касается гомологии – это характеристика такой углеродной цепи, в которой каждый следующий член может быть получен прибавлением к предыдущему одной группы СН 2 . Каждый гомологический ряд можно выразить одной общей формулой. А зная формулу, несложно определить состав любого из членов ряда. Например, гомологи метана описываются формулой C n H 2n+2 .
По мере прибавления «гомологической разницы» СН 2 , усиливается связь между атомами вещества. Возьмем гомологический ряд метана: четыре первых его члена – газы (метан, этан, пропан, бутан), следующие шесть – жидкости (пентан, гексан, гептан, октан, нонан, декан), а дальше следуют вещества в твердом агрегатном состоянии (пентадекан, эйкозан и т.д.). И чем прочнее связь между атомами углерода, тем выше молекулярный вес, температуры кипения и плавления веществ.
Какие классы органических веществ существуют?
К органическим веществам биологического происхождения относятся:
- белки;
- углеводы;
- нуклеиновые кислоты;
- липиды.
Три первых пункта можно еще назвать биологическими полимерами.
Более подробная классификация органических химических веществ охватывает вещества не только биологического происхождения.
К углеводородам относятся:
- ациклические соединения:
- предельные углеводороды (алканы);
- непредельные углеводороды:
- алкены;
- алкины;
- алкадиены.
- циклические соединения:
- соединения карбоциклические:
- алициклические;
- ароматические.
- соединения гетероциклические.
- соединения карбоциклические:
Есть также иные классы органических соединений, в составе которых углерод соединяется с другими веществами, кроме водорода:
- спирты и фенолы;
- альдегиды и кетоны;
- карбоновые кислоты;
- сложные эфиры;
- липиды;
- углеводы:
- моносахариды;
- олигосахариды;
- полисахариды.
- мукополисахариды.
- амины;
- аминокислоты;
- белки;
- нуклеиновые кислоты.
Формулы органических веществ по классам

Примеры органических веществ
Как вы помните, в человеческом организме различного рода органические вещества – основа основ. Это наши ткани и жидкости, гормоны и пигменты, ферменты и АТФ, а также многое другое.
В телах людей и животных приоритет за белками и жирами (половина сухой массы клетки животных это белки). У растений (примерно 80% сухой массы клетки) – за углеводами, в первую очередь сложными – полисахаридами. В том числе за целлюлозой (без которой не было бы бумаги), крахмалом.
Давайте поговорим про некоторые из них подробнее.
Например, про углеводы . Если бы можно было взять и измерить массы всех органических веществ на планете, именно углеводы победили бы в этом соревновании.
Они служат в организме источником энергии, являются строительными материалами для клеток, а также осуществляют запас веществ. Растениям для этой цели служит крахмал, животным – гликоген.
Кроме того, углеводы очень разнообразны. Например, простые углеводы. Самые распространенные в природе моносахариды – это пентозы (в том числе входящая в состав ДНК дезоксирибоза) и гексозы (хорошо знакомая вам глюкоза).
Как из кирпичиков, на большой стройке природы выстраиваются из тысяч и тысяч моносахаридов полисахариды. Без них, точнее, без целлюлозы, крахмала, не было бы растений. Да и животным без гликогена, лактозы и хитина пришлось бы трудно.
Посмотрим внимательно и на белки . Природа самый великий мастер мозаик и пазлов: всего из 20 аминокислот в человеческом организме образуется 5 миллионов типов белков. На белках тоже лежит немало жизненно важных функций. Например, строительство, регуляция процессов в организме, свертывание крови (для этого существуют отдельные белки), движение, транспорт некоторых веществ в организме, они также являются источником энергии, в виде ферментов выступают катализатором реакций, обеспечивают защиту. В деле защиты организма от негативных внешних воздействий важную роль играют антитела. И если в тонкой настройке организма происходит разлад, антитела вместо уничтожения внешних врагов могут выступать агрессорами к собственным органам и тканям организма.

Белки также делятся на простые (протеины) и сложные (протеиды). И обладают присущими только им свойствами: денатурацией (разрушением, которое вы не раз замечали, когда варили яйцо вкрутую) и ренатурацией (это свойство нашло широкое применение в изготовлении антибиотиков, пищевых концентратов и др.).
Не обойдем вниманием и липиды (жиры). В нашем организме они служат запасным источником энергии. В качестве растворителей помогают протеканию биохимических реакций. Участвуют в строительстве организма – например, в формировании клеточных мембран.
И еще пару слов о таких любопытных органических соединениях, как гормоны . Они участвуют в биохимических реакциях и обмене веществ. Такие маленькие, гормоны делают мужчин мужчинами (тестостерон) и женщин женщинами (эстроген). Заставляют нас радоваться или печалиться (не последнюю роль в перепадах настроения играют гормоны щитовидной железы, а эндорфин дарит ощущение счастья). И даже определяют, «совы» мы или «жаворонки». Готовы вы учиться допоздна или предпочитаете встать пораньше и сделать домашнюю работу перед школой, решает не только ваш распорядок дня, но и некоторые гормоны надпочечников.
Заключение
Мир органических веществ по-настоящему удивительный. Достаточно углубиться в его изучение лишь немного, чтобы у вас захватило дух от ощущения родства со всем живым на Земле. Две ноги, четыре или корни вместо ног – всех нас объединяет волшебство химической лаборатории матушки-природы. Оно заставляет атомы углерода объединяться в цепочки, вступать в реакции и создавать тысячи таких разнообразных химических соединений.
Теперь у вас есть краткий путеводитель по органической химии. Конечно, здесь представлена далеко не вся возможная информация. Какие-то моменты вам, быть может, придется уточнить самостоятельно. Но вы всегда можете использовать намеченный нами маршрут для своих самостоятельных изысканий.
Вы также можете использовать приведенное в статье определение органического вещества, классификацию и общие формулы органических соединений и общие сведения о них, чтобы подготовиться к урокам химии в школе.
Расскажите нам в комментариях, какой раздел химии (органическая или неорганическая) нравится вам больше и почему. Не забудьте «расшарить» статью в социальных сетях, чтобы ваши одноклассники тоже смогли ею воспользоваться.
Пожалуйста, сообщите, если обнаружите в статье какую-то неточность или ошибку. Все мы люди и все мы иногда ошибаемся.
blog.сайт, при полном или частичном копировании материала ссылка на первоисточник обязательна.
В настоящее время установлено, что класс органических веществ - самый обширный среди других химических соединений. Что же ученые-химики относят к органическим веществам? Ответ таков: это те вещества, в состав которых включен углерод. Впрочем, из этого правила есть исключения: угольная кислота, цианиды, карбонаты, оксиды углерода не входят в состав органических соединений.
Углерод - очень любопытный в своем роде химический элемент. Его особенность состоит в том, что он может образовывать из своих атомов цепочки. Такая связь оказывается очень стабильной. В органических соединениях углерод демонстрирует высокую валентность (IV). Речь идет о способности образовывать связи с иными веществами. Эти связи вполне могут быть не только одинарными, но также двойными или тройными. По мере возрастания числа связей цепочка из атомов становится короче, стабильной этой связи увеличивается.
Углерод известен также тем, что он может образовывать линейные, плоские и даже объемные структуры. Эти свойства данного химического элемента обусловили такое разнообразие органических веществ в природе. Около трети всей массы каждой клетки человеческого тела составляют органические соединения. Это белки, из которых в основном и построено тело. Это углеводы - универсальное «топливо» для организма. Это жиры, которые позволяют запасать энергию. Гормоны управляют работой всех органов и даже влияют на поведение. А ферменты запускают внутри организма бурные химические реакции. Более того, «исходный код» живого существа - цепочка ДНК - это органическое соединение, в основе которого лежит углерод.
Почти все химические элементы, когда они соединяются с углеродом, способны дать начало органическим соединениям. Чаще всего в природе в состав органических веществ входят:
- кислород;
- водород;
- сера;
- азот;
- фосфор.
Развитие теории при изучении органических веществ шло сразу по двум взаимосвязанным направлениям: ученые изучали пространственное расположение молекул соединений и выясняли сущность химических связей в соединениях. У истоков теории строения органических веществ стоял русский химик А.М. Бутлеров.
Принципы классификации органических веществ
В разделе науки, известном как органическая химия, особое значение имеют вопросы классификации веществ. Сложность состоит в том, что описанию подлежат миллионы химических соединений.
Требования к номенклатуре очень строги: она должна быть систематической и пригодной для использования в международных масштабах. Специалисты любой страны должны понимать, о каком соединении идет речь и однозначно представлять его структуру. Предпринимается ряд усилий, которые позволят сделать классификацию органических соединений пригодной для компьютерной обработки.
В основе современной классификации лежит строение углеродного скелета молекулы и наличие в ней функциональных групп.
По строению своего углеродного скелета органические вещества делятся на группы:
- ациклические (алифатические);
- карбоциклические;
- гетероциклические.
Родоначальниками любых соединений в органической химии являются те углеводороды, которые состоят лишь из атомов углерода и водорода. Как правило, молекулы органических веществ содержат в своем составе так называемые функциональные группы. Это - атомы либо группы атомов, которые определяют, какими будут химические свойства соединения. Такие группы также позволяют отнести соединение к тому или иному классу.
Примерами функциональных групп могут служить:
- карбонильная;
- карбоксильная;
- гидроксильная.
Те соединения, которые содержат только одну функциональную группу, именуют монофункциональными. Если в молекуле органического вещества имеется несколько таких групп, они считаются полифункциональными (к примеру, глицерин или хлороформ). Гетерофункциональными будут соединения, где функциональные группы различны по составу. Их в одно и то же время вполне можно отнести к разным классам. Пример: молочная кислота. Ее можно рассматривать как спирт и как карбоновую кислоту.
Переход от класса к классу осуществляется, как правило, с участием функциональных групп, но без изменения углеродного скелета.
Скелетом применительно к молекуле называют последовательность соединения атомов. Скелет может быть углеродным или же содержать так называемые гетероатомы (к примеру, азот, серу, кислород и т.д.). Также скелет молекулы органического соединения может быть разветвленным или неразветвленным; открытым или же циклическим.
Особым типом циклических соединений считаются ароматические: для них не являются характерными реакции присоединения.
Основные классы органических веществ
Известны следующие органические вещества биологического происхождения:
- углеводы;
- белки;
- липиды;
- нуклеиновые кислоты.
В более подробную классификацию органических соединений включаются вещества, которые не имеют биологического происхождения.
Различают классы органических веществ, в составе которых углерод входит в соединение с другими веществами (кроме водорода):
- спирты и фенолы;
- карбоновые кислоты;
- альдегиды и кислоты;
- сложные эфиры;
- углеводы;
- липиды;
- аминокислоты;
- нуклеиновые кислоты;
- белки.
Строение органических веществ
Большое разнообразие органических соединений в природе объясняется особенностями атомов углерода. Они способны образовывать весьма прочные связи, объединяясь в группы - цепочки. Результатом становятся вполне устойчивые молекулы. Способ, который молекулы используют, чтобы соединиться в цепь, является ключевой особенностью их строения. Углерод способен объединяться как в открытые цепи, так и в замкнутые (их и называют циклическими).
Строение веществ непосредственно влияет на их свойства. Особенности строения дают возможность существовать десяткам и сотням самостоятельных соединений углерода.
Важную роль в поддержании многообразия органических веществ играют такие свойства как гомология и изомерия.
Речь идет о идентичных на первый взгляд веществах: их состав не отличается друг от друга, молекулярная формула одна и та же. А вот строение соединений принципиально различается. Разными будут и химические свойства веществ. К примеру, одно и то же написание имеют изомеры бутан и изобутан. Атомы в молекулах этих двух веществ располагаются в разном порядке. В одном случае они разветвлены, в другом - нет.
Под гомологией понимают характеристику углеродной цепи, где каждый последующий член можно получить, прибавляя к предыдущему одну и ту же группу. Иными словами, каждый из гомологических рядов вполне можно выразить одной и той же формулой. Зная такую формулу, можно без особого труда выяснить состав любого члена ряда.

Примеры органических веществ
Углеводы вполне победили бы в состязании между всеми органическими веществами, если взять их в целом по массе. Это - источник энергии для живых организмов и строительный материал для большинства клеток. Мир углеводов отличается большим разнообразием. Без крахмала и целлюлозы не смогли бы существовать растения. А животный мир стал бы невозможен без лактозы и гликогена.
Еще один представитель мира органических веществ - белки. Всего из двух десятков аминокислот природе удается образовать в организме человека до 5 млн типов белковых структур. В функции этих веществ входит регуляция жизненно важных процессов в организме, обеспечение свертываемости крови, перенос некоторых видов веществ в пределах организма. В виде ферментов белки выступают ускорителями реакций.
Еще один важный класс органических соединений - липиды (жиры). Эти вещества служат в качества запасного источника нужной организму энергии. Они являются растворителями и помогают протеканию биохимических реакций. Липиды участвуют также и в строительстве клеточных мембран.
Очень интересны и другие органические соединения - гормоны. Они отвечают за протекание биохимических реакций и обмен веществ. Это гормоны щитовидной железы заставляют человека испытывать радость или печалиться. А за ощущение счастья, как выяснили ученые, отвечает эндорфин.