Die elektronische Formel des Elements. Schema der Struktur des Atoms: Kern, Elektronenhülle
Lesen Sie auch
Chemikalien sind die Dinge, die die Welt um uns herum ausmachen.
Die Eigenschaften jeder chemischen Substanz werden in zwei Typen unterteilt: Chemische, die ihre Fähigkeit zur Bildung anderer Substanzen charakterisieren, und physikalische, die objektiv beobachtet werden und isoliert von chemischen Umwandlungen betrachtet werden können. Die physikalischen Eigenschaften eines Stoffes sind beispielsweise seine Aggregatzustand(fest, flüssig oder gasförmig), Wärmeleitfähigkeit, Wärmekapazität, Löslichkeit in verschiedenen Medien (Wasser, Alkohol etc.), Dichte, Farbe, Geschmack etc.
Die Umwandlung einiger chemischer Substanzen in andere Substanzen wird als chemische Phänomene oder chemische Reaktionen bezeichnet. Es sollte beachtet werden, dass es auch physikalische Phänomene gibt, die offensichtlich von einer Veränderung in einigen begleitet werden physikalische Eigenschaften Stoffe, ohne in andere Stoffe umgewandelt zu werden. ZU physikalische Phänomene B. das Schmelzen von Eis, das Gefrieren oder Verdunsten von Wasser usw.
Darüber, dass es im Laufe eines jeden Prozesses a chemisches Phänomen, können wir schließen, indem wir die charakteristischen Merkmale beobachten chemische Reaktionen wie Farbveränderung, Niederschlag, Gasentwicklung, Wärme- und/oder Lichtentwicklung.
So lässt sich beispielsweise ein Rückschluss auf den Ablauf chemischer Reaktionen ziehen, indem man beobachtet:
Die Bildung von Sedimenten beim Kochen von Wasser, im Alltag Kesselstein genannt;
Die Freisetzung von Wärme und Licht beim Brennen eines Feuers;
Ändern Sie die Slice-Farbe frischer Apfel auf Sendung;
Die Bildung von Gasblasen während der Gärung von Teig usw.
Die kleinsten Materieteilchen, die sich bei chemischen Reaktionen praktisch nicht verändern, sondern nur auf neue Weise miteinander verbunden werden, nennt man Atome.
Die Idee der Existenz solcher Materieeinheiten entstand in antikes griechenland in den Köpfen antike Philosophen, was eigentlich die Herkunft des Begriffs „Atom“ erklärt, denn „atomos“ bedeutet wörtlich übersetzt aus dem Griechischen „unteilbar“.
Entgegen der Vorstellung der antiken griechischen Philosophen sind Atome jedoch nicht das absolute Minimum der Materie, d.h. selbst haben eine komplexe Struktur.
Jedes Atom besteht aus den sogenannten subatomaren Teilchen – Protonen, Neutronen und Elektronen, die jeweils mit den Symbolen p + , n o und e – bezeichnet werden. Der hochgestellte Index in der verwendeten Notation zeigt an, dass das Proton eine positive Einheitsladung hat, das Elektron eine negative Einheitsladung hat und das Neutron keine Ladung hat.
Was die qualitative Struktur des Atoms betrifft, so hat jedes Atom alle Protonen und Neutronen, die im sogenannten Kern konzentriert sind, um den herum die Elektronen eine Elektronenhülle bilden.
Proton und Neutron haben praktisch die gleiche Masse, d.h. m p ≈ m n , und die Elektronenmasse ist fast 2000-mal kleiner als die Masse von jedem von ihnen, d.h. m p / me e ≈ m n / me e ≈ 2000.
Da die grundlegende Eigenschaft eines Atoms seine elektrische Neutralität ist und die Ladung eines Elektrons gleich der Ladung eines Protons ist, kann daraus geschlossen werden, dass die Anzahl der Elektronen in jedem Atom gleich der Anzahl der Protonen ist.
So zeigt beispielsweise die folgende Tabelle die mögliche Zusammensetzung von Atomen:
Die Art der Atome mit gleicher Kernladung, d.h. Mit die gleiche Nummer Protonen in ihren Kernen werden als chemisches Element bezeichnet. Aus der obigen Tabelle können wir also schließen, dass Atom1 und Atom2 zu einem chemischen Element gehören und Atom3 und Atom4 zu einem anderen chemischen Element gehören.
Jedes chemische Element hat seinen eigenen Namen und ein individuelles Symbol, das auf eine bestimmte Weise gelesen wird. So trägt beispielsweise das einfachste chemische Element, dessen Atome nur ein Proton im Kern enthalten, den Namen „Wasserstoff“ und wird mit dem Symbol „H“, das als „Asche“ gelesen wird, und dem chemischen Element bezeichnet mit einer Kernladung von +7 (d.h. mit 7 Protonen) - "Stickstoff", hat das Symbol "N", das als "en" gelesen wird.
Wie Sie der obigen Tabelle entnehmen können, sind die Atome eins Chemisches Element kann sich in der Anzahl der Neutronen in den Kernen unterscheiden.
Atome, die zum gleichen chemischen Element gehören, aber unterschiedlicher Betrag Neutronen und damit Masse nennt man Isotope.
So hat beispielsweise das chemische Element Wasserstoff drei Isotope - 1 H, 2 H und 3 H. Die Indizes 1, 2 und 3 über dem H-Symbol bedeuten die Gesamtzahl der Neutronen und Protonen. Diese. Wenn wir wissen, dass Wasserstoff ein chemisches Element ist, das dadurch gekennzeichnet ist, dass sich in den Kernen seiner Atome ein Proton befindet, können wir daraus schließen, dass es im 1 H-Isotop (1-1 = 0) überhaupt keine Neutronen gibt, in das 2 H-Isotop - 1 Neutron (2-1=1) und im Isotop 3 H - zwei Neutronen (3-1=2). Da, wie bereits erwähnt, ein Neutron und ein Proton die gleiche Masse haben und die Masse eines Elektrons dagegen vernachlässigbar ist, bedeutet dies, dass das 2 H-Isotop fast doppelt so schwer ist wie das 1 H-Isotop und das 3 H Isotop ist dreimal so schwer. Im Zusammenhang mit einer so großen Streuung der Massen von Wasserstoffisotopen wurden den 2 H- und 3 H-Isotopen sogar getrennte individuelle Namen und Symbole zugewiesen, was für kein anderes chemisches Element typisch ist. Das 2 H-Isotop wurde Deuterium genannt und erhielt das Symbol D, und das 3 H-Isotop erhielt den Namen Tritium und erhielt das Symbol T.
Wenn wir die Masse des Protons und des Neutrons als Einheit nehmen und die Masse des Elektrons vernachlässigen, kann der Index oben links zusätzlich zur Gesamtzahl der Protonen und Neutronen im Atom als seine Masse betrachtet werden, und Daher wird dieser Index als Massenzahl bezeichnet und mit dem Symbol A bezeichnet. Da die Ladung des Kerns aller Protonen dem Atom entspricht und die Ladung jedes Protons bedingt als gleich +1 angesehen wird, ist die Anzahl der Protonen im Kern wird Chargennummer (Z) genannt. Bezeichnet man die Anzahl der Neutronen in einem Atom mit dem Buchstaben N, lässt sich mathematisch die Beziehung zwischen Massenzahl, Ladungszahl und Neutronenzahl wie folgt ausdrücken:
Nach modernen Vorstellungen hat das Elektron eine duale (Teilchenwellen-) Natur. Es hat sowohl die Eigenschaften eines Teilchens als auch einer Welle. Wie ein Teilchen hat ein Elektron eine Masse und eine Ladung, aber gleichzeitig ist der Elektronenfluss wie eine Welle durch die Fähigkeit zur Beugung gekennzeichnet.
Um den Zustand eines Elektrons in einem Atom zu beschreiben, werden die Konzepte der Quantenmechanik verwendet, wonach das Elektron keine bestimmte Bewegungsbahn hat und sich an jedem Punkt im Raum befinden kann, jedoch mit unterschiedlichen Wahrscheinlichkeiten.
Der Raumbereich um den Kern, in dem sich am ehesten ein Elektron aufhält, wird als Atomorbital bezeichnet.
Ein Atomorbital haben kann verschiedene Form, Größe und Ausrichtung. Ein Atomorbital wird auch als Elektronenwolke bezeichnet.
Grafisch wird ein Atomorbital normalerweise als quadratische Zelle bezeichnet:
Die Quantenmechanik hat einen äußerst komplexen mathematischen Apparat, daher werden im Rahmen eines Schulchemiekurses nur die Konsequenzen der quantenmechanischen Theorie betrachtet.
Nach diesen Konsequenzen ist jedes Atomorbital und ein darauf befindliches Elektron vollständig durch 4 Quantenzahlen charakterisiert.
- Die Hauptquantenzahl - n - bestimmt die Gesamtenergie eines Elektrons in einem bestimmten Orbital. Der Wertebereich der Hauptquantenzahl ist alle ganze Zahlen, d.h. n = 1,2,3,4, 5 usw.
- Die Orbitalquantenzahl - l - charakterisiert die Form des Atomorbitals und kann beliebige ganzzahlige Werte von 0 bis n-1 annehmen, wobei n, wie Sie sich erinnern, die Hauptquantenzahl ist.
Orbitale mit l = 0 werden aufgerufen S-Orbitale. s-Orbitale sind kugelförmig und haben keine Richtung im Raum:
Orbitale mit l = 1 werden aufgerufen P-Orbitale. Diese Orbitale haben die Form einer dreidimensionalen Acht, d.h. die Form, die durch Drehen der Acht um die Symmetrieachse erhalten wird und äußerlich einer Hantel ähnelt:
Orbitale mit l = 2 werden aufgerufen D-Orbitale, und mit l = 3 – F-Orbitale. Ihre Struktur ist viel komplexer.
3) Die magnetische Quantenzahl - ml - bestimmt die räumliche Orientierung eines bestimmten Atomorbitals und drückt die Projektion des Bahndrehimpulses auf die Richtung aus Magnetfeld. Die magnetische Quantenzahl ml entspricht der Orientierung des Orbitals relativ zur Richtung des äußeren Magnetfeldstärkevektors und kann beliebige ganzzahlige Werte von –l bis +l einschließlich 0 annehmen, d.h. die Gesamtzahl der möglichen Werte ist (2l+1). Also zum Beispiel bei l = 0 m l = 0 (ein Wert), bei l = 1 m l = -1, 0, +1 (drei Werte), bei l = 2 m l = -2, -1, 0, + 1 , +2 (fünf Werte der magnetischen Quantenzahl) usw.
Also zum Beispiel p-Orbitale, d.h. Orbitale mit einer Orbitalquantenzahl l = 1, die die Form einer „dreidimensionalen Acht“ haben, entsprechen drei Werten der magnetischen Quantenzahl (-1, 0, +1), die wiederum entsprechen in drei senkrecht zueinander stehende Raumrichtungen.
4) Die Spinquantenzahl (oder einfach Spin) - m s - kann bedingt für die Drehrichtung eines Elektrons in einem Atom verantwortlich gemacht werden, sie kann Werte annehmen. Elektronen mit unterschiedlichen Spins sind durch vertikale Pfeile gekennzeichnet, die in unterschiedliche Richtungen zeigen: ↓ und .
Die Menge aller Orbitale in einem Atom, die den gleichen Wert der Hauptquantenzahl haben, wird als Energieniveau oder Elektronenhülle bezeichnet. Jede beliebige Energielevel mit irgendeiner Zahl besteht n aus n 2 Orbitalen.
Die Menge der Orbitale mit den gleichen Werten der Hauptquantenzahl und der Orbitalquantenzahl ist eine Energieunterebene.
Jedes Energieniveau, das der Hauptquantenzahl n entspricht, enthält n Unterniveaus. Jedes Energieunterniveau mit einer Orbitalquantenzahl l besteht wiederum aus (2l+1) Orbitalen. Somit besteht die s-Unterschicht aus einem s-Orbital, die p-Unterschicht aus drei p-Orbitalen, die d-Unterschicht aus fünf d-Orbitalen und die f-Unterschicht aus sieben f-Orbitalen. Da, wie bereits erwähnt, oft ein Atomorbital durch eine quadratische Zelle bezeichnet wird, lassen sich die s-, p-, d- und f-Unterebenen grafisch darstellen auf die folgende Weise:
Jedes Orbital entspricht einem einzelnen streng definierten Satz von drei Quantenzahlen n, l und m l .
Die Verteilung von Elektronen in Orbitalen wird als Elektronenkonfiguration bezeichnet.
Die Füllung von Atomorbitalen mit Elektronen erfolgt unter drei Bedingungen:
- Das Prinzip der minimalen Energie: Elektronen füllen Orbitale ausgehend von der niedrigsten Energieebene. Die Reihenfolge der Unterebenen in der Reihenfolge zunehmender Energie ist wie folgt: 1s<2s<2p<3s<3p<4s≤3d<4p<5s≤4d<5p<6s…;
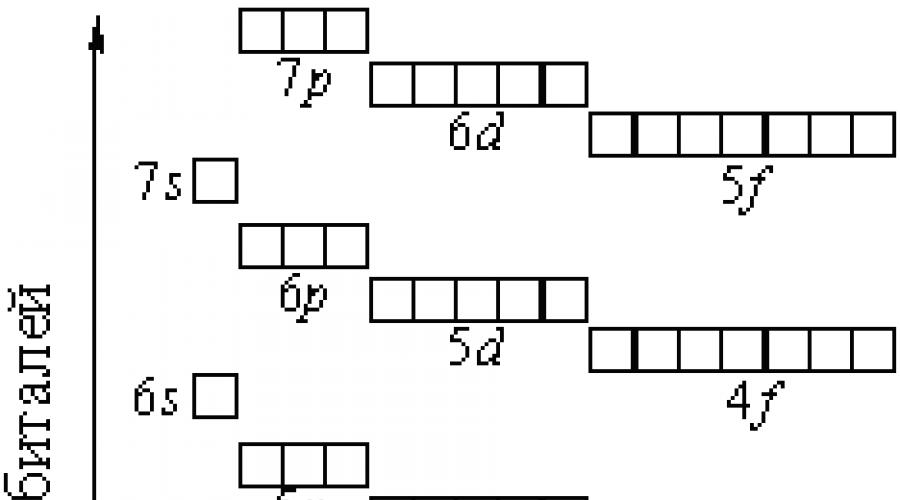
Um sich diese Reihenfolge des Füllens elektronischer Unterebenen leichter merken zu können, ist folgende grafische Darstellung sehr praktisch:
- Pauli-Prinzip: Jedes Orbital kann höchstens zwei Elektronen aufnehmen.
Wenn sich ein Elektron im Orbital befindet, wird es als ungepaart bezeichnet, und wenn es zwei gibt, werden sie als Elektronenpaar bezeichnet.
- Hundsche Regel: Der stabilste Zustand eines Atoms ist derjenige, in dem das Atom innerhalb einer Unterebene die maximal mögliche Anzahl ungepaarter Elektronen hat. Dieser stabilste Zustand des Atoms wird Grundzustand genannt.
Tatsächlich bedeutet das Obige, dass beispielsweise die Platzierung des 1., 2., 3. und 4. Elektrons auf drei Orbitalen der p-Unterebene wie folgt durchgeführt wird:
Die Füllung der Atomorbitale von Wasserstoff mit der Ladungszahl 1 bis Krypton (Kr) mit der Ladungszahl 36 wird wie folgt durchgeführt:
Eine ähnliche Darstellung der Reihenfolge, in der Atomorbitale gefüllt werden, wird als Energiediagramm bezeichnet. Anhand der elektronischen Diagramme einzelner Elemente können Sie deren sogenannte elektronische Formeln (Konfigurationen) aufschreiben. Also zum Beispiel ein Element mit 15 Protonen und daraus resultierend 15 Elektronen, also Phosphor (P) hat das folgende Energiediagramm:
Wenn es in eine elektronische Formel übersetzt wird, nimmt das Phosphoratom die Form an:
15 P = 1s 2 2s 2 2p 6 3s 2 3p 3
Normalgroße Zahlen links vom Sublevel-Symbol zeigen die Nummer des Energieniveaus, hochgestellte Zahlen rechts vom Sublevel-Symbol zeigen die Anzahl der Elektronen in dem entsprechenden Sublevel.
Unten sind die elektronischen Formeln der ersten 36 Elemente von D.I. Mendelejew.
| Zeitraum | Art.-Nr. | Symbol | Name | elektronische Formel |
| ICH | 1 | H | Wasserstoff | 1s 1 |
| 2 | Er | Helium | 1s2 | |
| II | 3 | Li | Lithium | 1s2 2s1 |
| 4 | Sei | Beryllium | 1s2 2s2 | |
| 5 | B | Bor | 1s 2 2s 2 2p 1 | |
| 6 | C | Kohlenstoff | 1s 2 2s 2 2p 2 | |
| 7 | N | Stickstoff | 1s 2 2s 2 2p 3 | |
| 8 | Ö | Sauerstoff | 1s 2 2s 2 2p 4 | |
| 9 | F | Fluor | 1s 2 2s 2 2p 5 | |
| 10 | Nein | Neon | 1s 2 2s 2 2p 6 | |
| III | 11 | N / A | Natrium | 1s 2 2s 2 2p 6 3s 1 |
| 12 | mg | Magnesium | 1s 2 2s 2 2p 6 3s 2 | |
| 13 | Al | Aluminium | 1s 2 2s 2 2p 6 3s 2 3p 1 | |
| 14 | Si | Silizium | 1s 2 2s 2 2p 6 3s 2 3p 2 | |
| 15 | P | Phosphor | 1s 2 2s 2 2p 6 3s 2 3p 3 | |
| 16 | S | Schwefel | 1s 2 2s 2 2p 6 3s 2 3p 4 | |
| 17 | Kl | Chlor | 1s 2 2s 2 2p 6 3s 2 3p 5 | |
| 18 | Ar | Argon | 1s 2 2s 2 2p 6 3s 2 3p 6 | |
| IV | 19 | K | Kalium | 1s 2 2s 2 2p 6 3s 2 3p 6 4s 1 |
| 20 | Ca | Kalzium | 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 | |
| 21 | sc | Scandium | 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 1 | |
| 22 | Ti | Titan | 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 2 | |
| 23 | v | Vanadium | 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 3 | |
| 24 | Kr | Chrom | 1s 2 2s 2 2p 6 3s 2 3p 6 4s 1 3d 5 S An D Unterebene | |
| 25 | Mn | Mangan | 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 5 | |
| 26 | Fe | Eisen | 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 6 | |
| 27 | co | Kobalt | 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 7 | |
| 28 | Ni | Nickel | 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 8 | |
| 29 | Cu | Kupfer | 1s 2 2s 2 2p 6 3s 2 3p 6 4s 1 3d 10 S An D Unterebene | |
| 30 | Zn | Zink | 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 | |
| 31 | Ga | Gallium | 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 1 | |
| 32 | Ge | Germanium | 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 2 | |
| 33 | Als | Arsen | 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 3 | |
| 34 | Se | Selen | 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 4 | |
| 35 | Br | Brom | 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 5 | |
| 36 | kr | Krypton | 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 |
Wie bereits erwähnt, sind Elektronen in Atomorbitalen in ihrem Grundzustand nach dem Prinzip der geringsten Energie angeordnet. Nichtsdestotrotz kann das Atom in Gegenwart leerer p-Orbitale im Grundzustand eines Atoms oft in den sogenannten angeregten Zustand überführt werden, wenn ihm überschüssige Energie verliehen wird. So hat zum Beispiel ein Boratom in seinem Grundzustand eine elektronische Konfiguration und ein Energiediagramm der folgenden Form:
5 B = 1s 2 2s 2 2p 1
Und im angeregten Zustand (*), d.h. Wenn dem Boratom etwas Energie zugeführt wird, sehen seine elektronische Konfiguration und sein Energiediagramm wie folgt aus:
5 B* = 1s 2 2s 1 2p 2
Je nachdem, welche Unterebene im Atom zuletzt gefüllt wird, werden chemische Elemente in s, p, d oder f eingeteilt.
Auffinden von s-, p-, d- und f-Elementen in der Tabelle D.I. Mendelejew:
- s-Elemente haben die letzte zu füllende s-Unterebene. Zu diesen Elementen gehören Elemente der Hauptuntergruppen (links in der Tabellenzelle) der Gruppen I und II.
- Für p-Elemente wird die p-Unterebene gefüllt. Die p-Elemente umfassen die letzten sechs Elemente jeder Periode, mit Ausnahme der ersten und siebten, sowie Elemente der Hauptuntergruppen der III-VIII-Gruppen.
- d-Elemente befinden sich in großen Perioden zwischen s- und p-Elementen.
- Die f-Elemente heißen Lanthanide und Actinide. Sie werden am Ende der Tabelle von D.I. Mendelejew.
Die Zusammensetzung des Atoms.
Ein Atom besteht aus Atomkern Und Elektronenhülle.
Der Kern eines Atoms besteht aus Protonen ( p+) und Neutronen ( N 0). Die meisten Wasserstoffatome haben einen einzelnen Protonenkern.
Anzahl der Protonen N(p+) ist gleich der Kernladung ( Z) und die Ordnungszahl des Elements in der natürlichen Reihe der Elemente (und im Periodensystem der Elemente).
N(P +) = Z
Die Summe der Anzahl der Neutronen N(N 0), einfach durch den Buchstaben gekennzeichnet N, und die Anzahl der Protonen Z genannt Massenzahl und ist mit dem Buchstaben gekennzeichnet A.
A = Z + N
Die Elektronenhülle eines Atoms besteht aus Elektronen, die sich um den Kern bewegen ( e -).
Anzahl der Elektronen N(e-) in der Elektronenhülle eines neutralen Atoms ist gleich der Anzahl der Protonen Z im Kern.
Die Masse eines Protons entspricht ungefähr der Masse eines Neutrons und der 1840-fachen Masse eines Elektrons, sodass die Masse eines Atoms praktisch gleich der Masse des Kerns ist.
Die Form eines Atoms ist kugelförmig. Der Radius des Kerns ist etwa 100.000 mal kleiner als der Radius des Atoms.
Chemisches Element- Art der Atome (Atommenge) mit gleicher Kernladung (mit gleicher Protonenzahl im Kern).
Isotop- eine Gruppe von Atomen eines Elements mit der gleichen Anzahl von Neutronen im Kern (oder eine Art von Atomen mit der gleichen Anzahl von Protonen und der gleichen Anzahl von Neutronen im Kern).
Verschiedene Isotope unterscheiden sich in der Anzahl der Neutronen in den Kernen ihrer Atome.
Bezeichnung eines einzelnen Atoms oder Isotops: (E - Elementsymbol), zum Beispiel: .
Die Struktur der Elektronenhülle des Atoms
Atomorbital ist der Zustand eines Elektrons in einem Atom. Orbitalsymbol - . Jedes Orbital entspricht einer Elektronenwolke.
Die Orbitale realer Atome im Grundzustand (nicht angeregt) sind von vier Arten: S, P, D Und F.
elektronische Wolke- der Teil des Weltraums, in dem sich ein Elektron mit einer Wahrscheinlichkeit von 90 (oder mehr) Prozent befindet.
Notiz: Manchmal werden die Konzepte "Atomorbital" und "Elektronenwolke" nicht unterschieden und beide als "Atomorbital" bezeichnet.
Die Elektronenhülle eines Atoms ist geschichtet. Elektronische Schicht von Elektronenwolken gleicher Größe gebildet. Orbitale einer Schicht bilden sich elektronische ("Energie") Ebene, ihre Energien sind für das Wasserstoffatom gleich, aber für andere Atome unterschiedlich.
Orbitale der gleichen Ebene werden gruppiert elektronisch (Energie) Unterebenen:
S- Unterebene (besteht aus einer S-Orbitale), Symbol - .
P Unterebene (besteht aus drei P
D Unterebene (besteht aus fünf D-Orbitale), Symbol - .
F Unterebene (besteht aus sieben F-Orbitale), Symbol - .
Die Energien der Orbitale derselben Unterebene sind gleich.
Bei der Bezeichnung von Unterebenen wird das Unterebenensymbol um die Nummer der Ebene (Elektronikebene) ergänzt, zum Beispiel: 2 S, 3P, 5D bedeutet S- Unterebene der zweiten Ebene, P- Unterebene der dritten Ebene, D- Unterebene der fünften Ebene.
Die Gesamtzahl der Unterebenen in einer Ebene ist gleich der Ebenennummer N. Die Gesamtzahl der Orbitale in einer Ebene ist N 2. Dementsprechend ist auch die Gesamtzahl der Wolken in einer Schicht N 2 .
Bezeichnungen: - freies Orbital (ohne Elektronen), - Orbital mit einem ungepaarten Elektron, - Orbital mit einem Elektronenpaar (mit zwei Elektronen).
Die Reihenfolge, in der Elektronen die Orbitale eines Atoms besetzen, wird durch drei Naturgesetze bestimmt (Formeln sind vereinfacht angegeben):
1. Das Prinzip der geringsten Energie – Elektronen füllen die Orbitale in der Reihenfolge zunehmender Energie der Orbitale.
2. Pauli-Prinzip - es können nicht mehr als zwei Elektronen in einem Orbital sein.
3. Hundsche Regel - Innerhalb der Unterebene füllen Elektronen zuerst freie Orbitale (eines nach dem anderen) und bilden erst danach Elektronenpaare.
Die Gesamtzahl der Elektronen in der elektronischen Ebene (oder in der elektronischen Schicht) beträgt 2 N 2 .
Die Verteilung der Unterebenen nach Energie wird als nächstes ausgedrückt (in der Reihenfolge zunehmender Energie):
1S, 2S, 2P, 3S, 3P, 4S, 3D, 4P, 5S, 4D, 5P, 6S, 4F, 5D, 6P, 7S, 5F, 6D, 7P ...
Visuell wird dieser Ablauf durch das Energiediagramm ausgedrückt:

Die Verteilung der Elektronen eines Atoms nach Ebenen, Unterebenen und Orbitalen (die elektronische Konfiguration eines Atoms) kann als elektronische Formel, als Energiediagramm oder einfacher als Diagramm elektronischer Schichten ("elektronisches Diagramm") dargestellt werden. .
Beispiele für die elektronische Struktur von Atomen:










Valenzelektronen- Elektronen eines Atoms, die an der Bildung chemischer Bindungen teilnehmen können. Für jedes Atom sind dies alle äußeren Elektronen plus die voräußeren Elektronen, deren Energie größer ist als die der äußeren. Zum Beispiel: Das Ca-Atom hat 4 Außenelektronen S 2, sie sind auch Valenz; das Fe-Atom hat externe Elektronen - 4 S 2 aber er hat 3 D 6, also hat das Eisenatom 8 Valenzelektronen. Die elektronische Valenzformel des Calciumatoms ist 4 S 2 und Eisenatome - 4 S 2 3D 6 .
Periodensystem der chemischen Elemente von D. I. Mendelejew
(natürliches System chemischer Elemente)
Periodengesetz der chemischen Elemente(moderne Formulierung): Die Eigenschaften chemischer Elemente sowie einfacher und komplexer Stoffe, die von ihnen gebildet werden, stehen in periodischer Abhängigkeit vom Wert der Ladung von Atomkernen.
Periodensystem- graphischer Ausdruck des periodischen Gesetzes.
Natürliches Spektrum chemischer Elemente- eine Anzahl chemischer Elemente, angeordnet nach der Zunahme der Anzahl der Protonen in den Kernen ihrer Atome oder, was dasselbe ist, nach der Zunahme der Ladungen der Kerne dieser Atome. Die Seriennummer eines Elements in dieser Reihe ist gleich der Anzahl der Protonen im Kern eines beliebigen Atoms dieses Elements.
Die Tabelle der chemischen Elemente wird durch „Einschneiden“ der natürlichen Reihen chemischer Elemente erstellt Perioden(horizontale Zeilen der Tabelle) und Gruppierungen (vertikale Spalten der Tabelle) von Elementen mit ähnlicher elektronischer Atomstruktur.
Je nachdem, wie Elemente in Gruppen zusammengefasst werden, kann eine Tabelle sein lange Zeit(Elemente mit gleicher Anzahl und Art von Valenzelektronen werden in Gruppen zusammengefasst) und kurzfristig(Elemente mit gleicher Zahl an Valenzelektronen werden in Gruppen zusammengefasst).
Die Gruppen der Kurzzeittabelle sind in Untergruppen ( hauptsächlich Und Nebenwirkungen), die mit den Gruppen der Langzeittabelle zusammenfallen.
Alle Atome von Elementen der gleichen Periode haben die gleiche Anzahl von Elektronenschichten, gleich der Nummer der Periode.
Die Anzahl der Elemente in den Perioden: 2, 8, 8, 18, 18, 32, 32. Die meisten Elemente der achten Periode wurden künstlich gewonnen, die letzten Elemente dieser Periode wurden noch nicht synthetisiert. Alle Perioden außer der ersten beginnen mit einem Alkalimetall bildenden Element (Li, Na, K usw.) und enden mit einem Edelgas bildenden Element (He, Ne, Ar, Kr usw.).
In der Kurzstundentafel – acht Gruppen, die jeweils in zwei Untergruppen (Haupt- und Nebengruppe) unterteilt sind, in der Langstundentafel – sechzehn Gruppen, die in römischen Ziffern mit den Buchstaben A oder B nummeriert sind, zum Beispiel: IA, IIIB, VIA, VIIB. Die Gruppe IA der langen Periodentafel entspricht der Hauptuntergruppe der ersten Gruppe der kurzen Periodentafel; Gruppe VIIB - sekundäre Untergruppe der siebten Gruppe: der Rest - ähnlich.
Die Eigenschaften chemischer Elemente ändern sich natürlich in Gruppen und Perioden.
In Perioden (mit steigender Seriennummer)
- die Kernladung steigt
- die Zahl der Außenelektronen steigt,
- der Radius der Atome nimmt ab,
- die Bindungsstärke der Elektronen zum Kern steigt (Ionisationsenergie),
- die Elektronegativität nimmt zu.
- die oxidierenden Eigenschaften einfacher Substanzen werden verstärkt ("Nichtmetallizität"),
- die reduzierenden Eigenschaften einfacher Substanzen ("Metallizität") schwächen,
- schwächt den basischen Charakter von Hydroxiden und den entsprechenden Oxiden,
- der saure Charakter von Hydroxiden und entsprechenden Oxiden nimmt zu.
In Gruppen (mit steigender Seriennummer)
- die Kernladung steigt
- der Radius der Atome nimmt zu (nur in A-Gruppen),
- die Stärke der Bindung zwischen Elektronen und Kern nimmt ab (Ionisationsenergie; nur in A-Gruppen),
- Elektronegativität nimmt ab (nur in A-Gruppen),
- schwächen die oxidierenden Eigenschaften einfacher Substanzen ("Nichtmetallizität"; nur in A-Gruppen),
- die reduzierenden Eigenschaften einfacher Substanzen werden verstärkt ("Metallizität"; nur in A-Gruppen),
- der basische Charakter der Hydroxide und der entsprechenden Oxide nimmt zu (nur in A-Gruppen),
- die saure Natur von Hydroxiden und den entsprechenden Oxiden wird geschwächt (nur in A-Gruppen),
- die Stabilität von Wasserstoffverbindungen nimmt ab (ihre Reduktionsaktivität nimmt zu; nur in A-Gruppen).
Aufgaben und Tests zum Thema "Thema 9. "Die Struktur des Atoms. Periodisches Gesetz und Periodensystem der chemischen Elemente von D. I. Mendeleev (PSCE)"."
- Periodisches Gesetz - Periodengesetz und Struktur der Atome Klasse 8–9
Sie sollten wissen: die Gesetze zum Füllen von Orbitalen mit Elektronen (Prinzip der kleinsten Energie, Pauli-Prinzip, Hund-Regel), die Struktur des Periodensystems der Elemente.Sie sollten in der Lage sein: die Zusammensetzung eines Atoms anhand der Position eines Elements im Periodensystem zu bestimmen und umgekehrt ein Element im Periodensystem zu finden, wenn Sie dessen Zusammensetzung kennen; das Strukturdiagramm, die elektronische Konfiguration eines Atoms, Ions darstellen und umgekehrt die Position eines chemischen Elements in der PSCE aus dem Diagramm und der elektronischen Konfiguration bestimmen; Charakterisieren Sie das Element und die Substanzen, die es gemäß seiner Position in der PSCE bildet; Änderungen des Radius von Atomen, der Eigenschaften chemischer Elemente und der von ihnen gebildeten Stoffe innerhalb einer Periode und einer Hauptuntergruppe des Periodensystems bestimmen.
Beispiel 1 Bestimmen Sie die Anzahl der Orbitale in der dritten elektronischen Ebene. Was sind diese Orbitale?
Um die Anzahl der Orbitale zu bestimmen, verwenden wir die Formel N Orbitale = N 2, wo N- Levelnummer. N Orbitale = 3 2 = 9. Eine 3 S-, drei 3 P- und fünf 3 D-Orbitale.Beispiel 2 Bestimmen Sie das Atom, dessen Element die elektronische Formel 1 hat S 2 2S 2 2P 6 3S 2 3P 1 .
Um zu bestimmen, um welches Element es sich handelt, müssen Sie seine Seriennummer herausfinden, die der Gesamtzahl der Elektronen im Atom entspricht. In diesem Fall: 2 + 2 + 6 + 2 + 1 = 13. Das ist Aluminium.Nachdem Sie sich vergewissert haben, dass Sie alles Notwendige gelernt haben, fahren Sie mit den Aufgaben fort. Wir wünschen Ihnen viel Erfolg.
Empfohlene Literatur:- O. S. Gabrielyan und andere Chemie, 11. Klasse. M., Trappe, 2002;
- G. E. Rudzitis, F. G. Feldman. Chemie 11 Zellen. M., Bildung, 2001.
Elektronische Konfiguration eines Atoms ist eine Formel, die die Anordnung von Elektronen in einem Atom nach Ebenen und Unterebenen zeigt. Nach dem Studium des Artikels erfahren Sie, wo und wie sich Elektronen befinden, lernen Quantenzahlen kennen und können die elektronische Konfiguration eines Atoms anhand seiner Anzahl aufbauen. Am Ende des Artikels befindet sich eine Elementtabelle.
Warum die elektronische Konfiguration von Elementen studieren?
Atome sind wie ein Konstruktor: Es gibt eine bestimmte Anzahl von Teilen, sie unterscheiden sich voneinander, aber zwei Teile des gleichen Typs sind genau gleich. Aber dieser Konstruktor ist viel interessanter als der aus Plastik, und hier ist der Grund. Die Konfiguration ändert sich je nachdem, wer in der Nähe ist. Zum Beispiel Sauerstoff neben Wasserstoff Vielleicht sich in Wasser verwandeln, neben Natrium in Gas, und in der Nähe von Eisen wird es vollständig zu Rost. Um die Frage zu beantworten, warum dies geschieht, und um das Verhalten eines Atoms neben einem anderen vorherzusagen, ist es notwendig, die elektronische Konfiguration zu untersuchen, die im Folgenden diskutiert wird.
Wie viele Elektronen sind in einem Atom?
Ein Atom besteht aus einem Kern und Elektronen, die ihn umkreisen, der Kern besteht aus Protonen und Neutronen. Im neutralen Zustand hat jedes Atom so viele Elektronen wie Protonen in seinem Kern. Die Anzahl der Protonen wurde durch die Seriennummer des Elements angegeben, zum Beispiel hat Schwefel 16 Protonen - das 16. Element des Periodensystems. Gold hat 79 Protonen – das 79. Element des Periodensystems. Dementsprechend gibt es im neutralen Zustand 16 Elektronen im Schwefel und 79 Elektronen im Gold.
Wo sucht man nach einem Elektron?
Aus der Beobachtung des Verhaltens eines Elektrons wurden bestimmte Muster abgeleitet, sie werden durch Quantenzahlen beschrieben, insgesamt gibt es vier davon:
- Hauptquantenzahl
- Orbitale Quantenzahl
- Magnetische Quantenzahl
- Spinquantenzahl
Orbital
Außerdem verwenden wir anstelle des Wortes Orbit den Begriff "Orbital", das Orbital ist ungefähr die Wellenfunktion des Elektrons - dies ist der Bereich, in dem das Elektron 90% der Zeit verbringt.
N - Niveau
L - Schale
M l - Orbitalzahl
M s - das erste oder zweite Elektron im Orbital
Bahnquantenzahl l
Als Ergebnis der Untersuchung der Elektronenwolke wurde festgestellt, dass die Wolke je nach Energieniveau vier Hauptformen annimmt: eine Kugel, Hanteln und die beiden anderen, komplexere. In aufsteigender Energiereihenfolge werden diese Formen als s-, p-, d- und f-Schalen bezeichnet. Jede dieser Schalen kann 1 (auf s), 3 (auf p), 5 (auf d) und 7 (auf f) Orbitale haben. Die Orbitalquantenzahl ist die Schale, auf der sich die Orbitale befinden. Die Orbitalquantenzahl für s-, p-, d- bzw. f-Orbitale nimmt die Werte 0,1,2 oder 3 an.
Auf der s-Schale ein Orbital (L=0) - zwei Elektronen
Es gibt drei Orbitale auf der p-Schale (L=1) – sechs Elektronen
Es gibt fünf Orbitale auf der d-Schale (L=2) – zehn Elektronen
Es gibt sieben Orbitale (L=3) auf der f-Schale – vierzehn Elektronen
Magnetische Quantenzahl m l
Es gibt drei Orbitale auf der p-Schale, sie werden mit Zahlen von -L bis +L bezeichnet, dh für die p-Schale (L=1) gibt es Orbitale "-1", "0" und "1". . Die magnetische Quantenzahl wird mit dem Buchstaben ml bezeichnet.
Innerhalb der Hülle ist es für Elektronen einfacher, sich in verschiedenen Orbitalen zu befinden, also füllen die ersten Elektronen eines für jedes Orbital und dann wird sein Paar zu jedem hinzugefügt.
Betrachten Sie eine D-Shell:
Die d-Schale entspricht dem Wert L=2, dh fünf Orbitale (-2,-1,0,1 und 2), die ersten fünf Elektronen füllen die Schale mit den Werten M l =-2, M l = –1, M l = 0, M l = 1, M l = 2.
Spinquantenzahl m s
Spin ist die Rotationsrichtung eines Elektrons um seine Achse, es gibt zwei Richtungen, also hat die Spinquantenzahl zwei Werte: +1/2 und -1/2. Nur zwei Elektronen mit entgegengesetztem Spin können sich auf derselben Energieunterebene befinden. Die Spinquantenzahl wird mit m s bezeichnet
Hauptquantenzahl n
Die Hauptquantenzahl ist das Energieniveau, derzeit sind sieben Energieniveaus bekannt, jedes wird mit einer arabischen Zahl bezeichnet: 1,2,3,...7. Die Anzahl der Muscheln auf jeder Ebene entspricht der Nummer der Ebene: Auf der ersten Ebene befindet sich eine Muschel, auf der zweiten zwei und so weiter.
Elektronenzahl

Jedes Elektron kann also durch vier Quantenzahlen beschrieben werden, die Kombination dieser Zahlen ist für jede Position des Elektrons einzigartig, nehmen wir das erste Elektron, das niedrigste Energieniveau ist N=1, eine Schale befindet sich auf der ersten Ebene, die erste Schale auf jeder Ebene hat die Form einer Kugel (s-Schale), d.h. L=0, die magnetische Quantenzahl kann nur einen Wert annehmen, M l =0 und der Spin wird gleich +1/2 sein. Nehmen wir das fünfte Elektron (in welchem Atom auch immer), dann sind die Hauptquantenzahlen dafür: N=2, L=1, M=-1, Spin 1/2.
Atom- ein elektrisch neutrales Teilchen, das aus einem positiv geladenen Kern und negativ geladenen Elektronen besteht. Im Zentrum eines Atoms befindet sich ein positiv geladener Kern. Es nimmt einen unbedeutenden Teil des Raums im Inneren des Atoms ein, die gesamte positive Ladung und fast die gesamte Masse des Atoms sind darin konzentriert.
Der Kern besteht aus Elementarteilchen - Proton und Neutron; Elektronen bewegen sich in geschlossenen Orbitalen um den Atomkern.
Proton (r)- ein Elementarteilchen mit einer relativen Masse von 1,00728 atomaren Masseneinheiten und einer Ladung von +1 konventioneller Einheit. Die Anzahl der Protonen im Atomkern ist gleich der Seriennummer des Elements im Periodensystem von D.I. Mendelejew.
Neutron (n)- ein neutrales Elementarteilchen mit einer relativen Masse von 1,00866 atomaren Masseneinheiten (a.m.u.).
Die Anzahl der Neutronen im Kern N wird durch die Formel bestimmt:
![]()
wobei A die Massenzahl ist, Z die Ladung des Kerns ist, gleich der Anzahl der Protonen (laufende Zahl).
Normalerweise werden die Parameter des Kerns eines Atoms wie folgt geschrieben: Die Ladung des Kerns wird unten links vom Symbol des Elements platziert und die Massenzahl wird zum Beispiel oben platziert:
Dieser Eintrag zeigt, dass die Kernladung (daher die Anzahl der Protonen) für ein Phosphoratom 15 ist, die Massenzahl 31 ist und die Anzahl der Neutronen 31 - 15 = 16 ist. Da sich die Massen von Proton und Neutron nur sehr wenig unterscheiden voneinander ist die Masse die Zahl ungefähr gleich der relativen Atommasse des Kerns.
Elektron (e-)- ein Elementarteilchen mit einer Masse von 0,00055 a. EM und Bedingte Gebühr –1. Die Anzahl der Elektronen in einem Atom entspricht der Ladung des Atomkerns (der Seriennummer des Elements im Periodensystem von D. I. Mendeleev).
Elektronen bewegen sich auf fest definierten Bahnen um den Kern und bilden die sogenannte Elektronenwolke.
Der Raumbereich um den Atomkern, in dem sich das Elektron am ehesten aufhält (90 % oder mehr), bestimmt die Form der Elektronenwolke.
Die Elektronenwolke des s-Elektrons hat eine Kugelform; die s-Energie-Unterebene kann maximal zwei Elektronen haben.
Die Elektronenwolke des p-Elektrons ist hantelförmig; Drei p-Orbitale können maximal sechs Elektronen aufnehmen.
Orbitale werden als Quadrat dargestellt, darüber oder darunter schreiben sie die Werte der Haupt- und Nebenquantenzahlen, die dieses Orbital beschreiben. Eine solche Aufzeichnung wird als grafische elektronische Formel bezeichnet, zum Beispiel:

In dieser Formel bezeichnen Pfeile ein Elektron, und die Richtung des Pfeils entspricht der Richtung des Spins - dem intrinsischen magnetischen Moment des Elektrons. Elektronen mit entgegengesetztem Spin ↓ heißen gepaart.
Die elektronischen Konfigurationen von Atomen von Elementen können als elektronische Formeln dargestellt werden, in denen die Unterebenensymbole angegeben sind, der Koeffizient vor dem Unterebenensymbol die Zugehörigkeit zu dieser Ebene anzeigt und der Grad des Symbols die Anzahl der Elektronen dieser Ebene anzeigt Unterebene.
Tabelle 1 zeigt die Struktur der Elektronenhüllen von Atomen der ersten 20 Elemente des Periodensystems der chemischen Elemente von D.I. Mendelejew.
Chemische Elemente, bei deren Atomen die s-Unterebene der äußeren Ebene mit ein oder zwei Elektronen aufgefüllt wird, nennt man s-Elemente. Chemische Elemente, in deren Atomen die p-Unterebene (von einem bis sechs Elektronen) gefüllt ist, werden als p-Elemente bezeichnet.
Die Anzahl der Elektronenschichten in einem Atom eines chemischen Elements ist gleich der Periodenzahl.
Gemäß Hundsche Regel Elektronen befinden sich in gleichartigen Orbitalen des gleichen Energieniveaus so, dass der Gesamtspin maximal ist. Folglich besetzt jedes Elektron beim Füllen der Energieunterebene zunächst eine separate Zelle, und erst danach beginnt ihre Paarung. Beispielsweise befinden sich bei einem Stickstoffatom alle p-Elektronen in getrennten Zellen, und bei Sauerstoff beginnt ihre Paarung, die vollständig in Neon endet.


Isotope werden Atome desselben Elements genannt, die in ihren Kernen die gleiche Anzahl von Protonen, aber eine unterschiedliche Anzahl von Neutronen enthalten.
Isotope sind für alle Elemente bekannt. Daher sind die Atommassen der Elemente im Periodensystem Mittelwerte der Massenzahlen natürlicher Isotopengemische und unterscheiden sich von ganzzahligen Werten. Daher kann die Atommasse eines natürlichen Isotopengemisches nicht als Hauptmerkmal eines Atoms und folglich eines Elements dienen. Eine solche Eigenschaft eines Atoms ist die Kernladung, die die Anzahl der Elektronen in der Elektronenhülle des Atoms und seine Struktur bestimmt.
Sehen wir uns in diesem Abschnitt einige typische Aufgaben an.
Beispiel 1 Welches Elementatom hat die elektronische Konfiguration 1s 2 2s 2 2p 6 3s 2 3p 6 4s 1 ?
Dieses Element hat ein 4s-Elektron in seinem äußeren Energieniveau. Daher befindet sich dieses chemische Element in der vierten Periode der ersten Gruppe der Hauptuntergruppe. Dieses Element ist Kalium.
Zu dieser Antwort kann man auch anders kommen. Wenn wir die Gesamtzahl aller Elektronen addieren, erhalten wir 19. Die Gesamtzahl der Elektronen ist gleich der Ordnungszahl des Elements. Kalium ist die Nummer 19 im Periodensystem.
Beispiel 2 Das höchste Oxid RO 2 entspricht dem chemischen Element. Die elektronische Konfiguration des externen Energieniveaus des Atoms dieses Elements entspricht der elektronischen Formel:
- ns 2 np 4
- ns 2 np 2
- ns 2 np 3
- ns 2 np 6
Gemäß der Formel des höchsten Oxids (siehe die Formeln der höchsten Oxide im Periodensystem) stellen wir fest, dass dieses chemische Element in der vierten Gruppe der Hauptuntergruppe steht. Diese Elemente haben vier Elektronen in ihrem äußeren Energieniveau - zwei s und zwei p. Daher ist die richtige Antwort 2.
Ausbildungsaufgaben
1. Die Gesamtzahl der s-Elektronen in einem Calciumatom ist
1) 20
2) 40
3) 8
4) 6
2. Die Anzahl der gepaarten p-Elektronen in einem Stickstoffatom ist
1) 7
2) 14
3) 3
4) 4
3. Die Anzahl der ungepaarten s-Elektronen in einem Stickstoffatom ist
1) 7
2) 14
3) 3
4) 4
4. Die Anzahl der Elektronen im äußeren Energieniveau eines Argonatoms ist
1) 18
2) 6
3) 4
4) 8
5. Die Anzahl der Protonen, Neutronen und Elektronen im Atom beträgt 9 4 Be
1) 9, 4, 5
2) 4, 5, 4
3) 4, 4, 5
4) 9, 5, 9
6. Verteilung der Elektronen über die Elektronenschichten 2; 8; 4 - entspricht dem Atom in (in)
1) 3. Periode, IA-Gruppe
2) 2. Periode, IVA-Gruppe
3) 3. Periode, IVA-Gruppe
4) 3. Periode, VA-Gruppe
7. Das in der 3. Periode der VA-Gruppe befindliche chemische Element entspricht dem Schema der elektronischen Struktur des Atoms
1) 2, 8, 6
2) 2, 6, 4
3) 2, 8, 5
4) 2, 8, 2
8. Ein chemisches Element mit der elektronischen Konfiguration 1s 2 2s 2 2p 4 bildet eine flüchtige Wasserstoffverbindung, deren Formel lautet
1) EN
2) EN 2
3) EN 3
4) DE 4
9. Die Anzahl der Elektronenschichten in einem Atom eines chemischen Elements ist
1) seine Seriennummer
2) Gruppennummer
3) die Anzahl der Neutronen im Kern
4) Periodennummer
10. Die Anzahl der externen Elektronen in den Atomen der chemischen Elemente der Hauptuntergruppen ist
1) die Seriennummer des Elements
2) Gruppennummer
3) die Anzahl der Neutronen im Kern
4) Periodennummer
11. Zwei Elektronen befinden sich in der äußeren Elektronenschicht der Atome jedes der chemischen Elemente in der Reihe
1) Er, sei, Ba
2) Mg, Si, O
3) C, Mg, Ca
4) Ba, Sr, B
12. Ein chemisches Element, dessen elektronische Formel 1s 2 2s 2 2p 6 3s 2 3p 6 4s 1 ist, bildet ein Oxid der Zusammensetzung
1) Li 2 O
2) MgO
3) K2O
4) Na20
13. Die Anzahl der Elektronenschichten und die Anzahl der p-Elektronen in einem Schwefelatom ist
1) 2, 6
2) 3, 4
3) 3, 16
4) 3, 10
14. Die elektronische Konfiguration ns 2 np 4 entspricht dem Atom
1) Chlor
2) Schwefel
3) Magnesium
4) Silizium
15. Die Valenzelektronen des Natriumatoms im Grundzustand befinden sich auf der Energieunterebene
1) 2s
2) 2p
3) 3 Sek
4) 3p
16. Die Stickstoff- und Phosphoratome haben
1) die gleiche Anzahl von Neutronen
2) die gleiche Anzahl von Protonen
3) die gleiche Konfiguration der äußeren Elektronenschicht
17. Calciumatome haben die gleiche Anzahl an Valenzelektronen
1) Kalium
2) Aluminium
3) Beryllium
4) Bor
18. Die Kohlenstoff- und Fluoratome haben
1) die gleiche Anzahl von Neutronen
2) die gleiche Anzahl von Protonen
3) die gleiche Anzahl elektronischer Schichten
4) die gleiche Anzahl von Elektronen
19. Am Kohlenstoffatom im Grundzustand ist die Anzahl der ungepaarten Elektronen
1) 1
3) 3
2) 2
4) 4
20. Im Sauerstoffatom im Grundzustand ist die Anzahl der gepaarten Elektronen
Elektronen
Das Konzept eines Atoms stammt aus der Antike, um die Teilchen der Materie zu bezeichnen. Atom bedeutet im Griechischen „unteilbar“.

Der irische Physiker Stoney kam aufgrund von Experimenten zu dem Schluss, dass Elektrizität von den kleinsten Teilchen getragen wird, die in den Atomen aller chemischen Elemente vorhanden sind. 1891 schlug Stoney vor, diese Teilchen Elektronen zu nennen, was auf Griechisch „Bernstein“ bedeutet. Einige Jahre nachdem das Elektron seinen Namen erhielt, bewiesen der englische Physiker Joseph Thomson und der französische Physiker Jean Perrin, dass Elektronen eine negative Ladung tragen. Dies ist die kleinste negative Ladung, die in der Chemie als Einheit genommen wird (-1). Thomson gelang es sogar, die Geschwindigkeit des Elektrons zu bestimmen (die Geschwindigkeit eines Elektrons in der Umlaufbahn ist umgekehrt proportional zur Umlaufbahnnummer n. Die Radien der Umlaufbahnen wachsen proportional zum Quadrat der Umlaufbahnnummer. In der ersten Umlaufbahn des Wasserstoffs Atom (n=1; Z=1), die Geschwindigkeit ist ≈ 2,2 106 m / c, also etwa hundertmal kleiner als die Lichtgeschwindigkeit c=3 108 m/s) und die Masse eines Elektrons ( es ist fast 2000 mal kleiner als die Masse eines Wasserstoffatoms).

Der Zustand der Elektronen in einem Atom
Der Zustand eines Elektrons in einem Atom ist eine Reihe von Informationen über die Energie eines bestimmten Elektrons und den Raum, in dem es sich befindet. Ein Elektron in einem Atom hat keine Bewegungsbahn, d.h. man kann nur davon sprechen die Wahrscheinlichkeit, es im Raum um den Kern herum zu finden.
 Es kann sich in jedem Teil dieses den Kern umgebenden Raums befinden, und die Gesamtheit seiner verschiedenen Positionen wird als Elektronenwolke mit einer bestimmten negativen Ladungsdichte betrachtet. Bildlich kann man sich das so vorstellen: Könnte man die Position eines Elektrons in einem Atom in Hundertstel- oder Millionstelsekunden fotografieren, wie in einem Fotofinish, dann würde das Elektron in solchen Fotografien als Punkte dargestellt. Die Überlagerung unzähliger solcher Fotos würde zu einem Bild einer Elektronenwolke mit der höchsten Dichte führen, wo sich die meisten dieser Punkte befinden werden.
Es kann sich in jedem Teil dieses den Kern umgebenden Raums befinden, und die Gesamtheit seiner verschiedenen Positionen wird als Elektronenwolke mit einer bestimmten negativen Ladungsdichte betrachtet. Bildlich kann man sich das so vorstellen: Könnte man die Position eines Elektrons in einem Atom in Hundertstel- oder Millionstelsekunden fotografieren, wie in einem Fotofinish, dann würde das Elektron in solchen Fotografien als Punkte dargestellt. Die Überlagerung unzähliger solcher Fotos würde zu einem Bild einer Elektronenwolke mit der höchsten Dichte führen, wo sich die meisten dieser Punkte befinden werden.
Der Raum um den Atomkern, in dem sich das Elektron am ehesten aufhält, wird als Orbital bezeichnet. Es enthält ca 90 % E-Cloud, und das bedeutet, dass sich das Elektron etwa 90 % der Zeit in diesem Teil des Raums aufhält. Durch Form unterschieden 4 derzeit bekannte Arten von Orbitalen, die lateinisch bezeichnet werden Buchstaben s, p, d und f. Eine grafische Darstellung einiger Formen elektronischer Orbitale ist in der Abbildung gezeigt.

Das wichtigste Merkmal der Bewegung eines Elektrons in einer bestimmten Umlaufbahn ist die Energie seiner Verbindung mit dem Kern. Elektronen mit ähnlichen Energiewerten bilden eine einzelne Elektronenschicht oder Energieebene. Die Energieniveaus sind ausgehend vom Kern nummeriert - 1, 2, 3, 4, 5, 6 und 7.
Eine ganze Zahl n, die die Nummer des Energieniveaus bezeichnet, wird als Hauptquantenzahl bezeichnet. Es charakterisiert die Energie von Elektronen, die ein bestimmtes Energieniveau einnehmen. Die Elektronen des ersten Energieniveaus, das dem Kern am nächsten ist, haben die niedrigste Energie. Verglichen mit den Elektronen der ersten Ebene zeichnen sich die Elektronen der nächsten Ebenen durch eine große Energiemenge aus. Folglich sind die Elektronen der äußeren Ebene am wenigsten stark an den Atomkern gebunden.
Die größte Anzahl von Elektronen im Energieniveau wird durch die Formel bestimmt:
N = 2n2,
wobei N die maximale Anzahl von Elektronen ist; n ist die Niveaunummer oder die Hauptquantenzahl. Folglich kann das erste kernnächste Energieniveau nicht mehr als zwei Elektronen enthalten; am zweiten - nicht mehr als 8; am dritten - nicht mehr als 18; am vierten - nicht mehr als 32.
Ab dem zweiten Energieniveau (n = 2) wird jedes der Niveaus in Unterniveaus (Unterschichten) unterteilt, die sich in der Bindungsenergie mit dem Kern etwas voneinander unterscheiden. Die Anzahl der Unterebenen ist gleich dem Wert der Hauptquantenzahl: das erste Energieniveau hat ein Unterniveau; die zweite - zwei; dritte - drei; vierte - vier Unterebenen. Unterebenen wiederum werden durch Orbitale gebildet. Jeder Wertn entspricht der Anzahl der Orbitale gleich n.
Es ist üblich, Unterebenen in lateinischen Buchstaben sowie die Form der Orbitale, aus denen sie bestehen, zu bezeichnen: s, p, d, f.

Protonen und Neutronen

Ein Atom eines beliebigen chemischen Elements ist vergleichbar mit einem winzigen Sonnensystem. Daher wird ein solches von E. Rutherford vorgeschlagenes Atommodell genannt planetarisch.
Der Atomkern, in dem die gesamte Masse des Atoms konzentriert ist, besteht aus Teilchen zweier Arten - Protonen und Neutronen.
Protonen haben eine Ladung gleich der Ladung von Elektronen, aber mit entgegengesetztem Vorzeichen (+1) und eine Masse gleich der Masse eines Wasserstoffatoms (es wird in der Chemie als Einheit akzeptiert). Neutronen tragen keine Ladung, sie sind neutral und haben die gleiche Masse wie ein Proton.
Protonen und Neutronen werden zusammen als Nukleonen bezeichnet (vom lateinischen Kern - Kern). Die Summe der Anzahl von Protonen und Neutronen in einem Atom nennt man Massenzahl. Zum Beispiel die Massenzahl eines Aluminiumatoms:

13 + 14 = 27
Protonenzahl 13, Neutronenzahl 14, Massenzahl 27
Da die vernachlässigbare Masse des Elektrons vernachlässigt werden kann, ist offensichtlich, dass die gesamte Masse des Atoms im Kern konzentriert ist. Elektronen repräsentieren e - .
Denn das Atom elektrisch neutral, ist es auch offensichtlich, dass die Anzahl der Protonen und Elektronen in einem Atom gleich ist. Sie ist gleich der laufenden Nummer des ihm im Periodensystem zugeordneten chemischen Elements. Die Masse eines Atoms setzt sich aus der Masse von Protonen und Neutronen zusammen. Wenn Sie die Seriennummer des Elements (Z), d. h. die Anzahl der Protonen, und die Massenzahl (A) kennen, die der Summe der Anzahl der Protonen und Neutronen entspricht, können Sie die Anzahl der Neutronen (N) mithilfe von ermitteln Formel:

N=A-Z
Beispielsweise beträgt die Anzahl der Neutronen in einem Eisenatom:
56 — 26 = 30
Isotope
Sorten von Atomen des gleichen Elements, die die gleiche Kernladung, aber unterschiedliche Massenzahlen haben, werden als bezeichnet Isotope. Chemische Elemente, die in der Natur vorkommen, sind eine Mischung von Isotopen. Kohlenstoff hat also drei Isotope mit einer Masse von 12, 13, 14; Sauerstoff - drei Isotope mit einer Masse von 16, 17, 18 usw. Die relative Atommasse eines chemischen Elements, die normalerweise im Periodensystem angegeben wird, ist der Durchschnittswert der Atommassen einer natürlichen Mischung von Isotopen eines bestimmten Elements ihren relativen Gehalt in der Natur berücksichtigen. Die chemischen Eigenschaften der Isotope der meisten chemischen Elemente sind genau gleich. Wasserstoffisotope unterscheiden sich jedoch stark in ihren Eigenschaften aufgrund des dramatischen Anstiegs ihrer relativen Atommasse; Sie haben sogar individuelle Namen und chemische Symbole erhalten.

Elemente der ersten Periode
Schema der elektronischen Struktur des Wasserstoffatoms:

Schemata der elektronischen Struktur von Atomen zeigen die Verteilung von Elektronen über elektronische Schichten (Energieniveaus).

Die grafische elektronische Formel des Wasserstoffatoms (zeigt die Verteilung der Elektronen über Energieniveaus und Unterniveaus):

Grafische elektronische Formeln von Atomen zeigen die Verteilung von Elektronen nicht nur in Ebenen und Unterebenen, sondern auch in Umlaufbahnen.
In einem Heliumatom ist die erste Elektronenschicht abgeschlossen - sie hat 2 Elektronen. Wasserstoff und Helium sind s-Elemente; für diese Atome ist das s-Orbital mit Elektronen gefüllt.

Alle Elemente der zweiten Periode die erste Elektronenschicht wird gefüllt, und die Elektronen füllen die s- und p-Orbitale der zweiten Elektronenschicht nach dem Prinzip der kleinsten Energie (zuerst s, dann p) und den Regeln von Pauli und Hund.
Im Neonatom ist die zweite Elektronenschicht fertig - sie hat 8 Elektronen.
Für Atome von Elementen der dritten Periode sind die erste und zweite Elektronenschicht fertig, also ist die dritte Elektronenschicht gefüllt, in der Elektronen 3s-, 3p- und 3d-Unterniveaus besetzen können.
Am Magnesiumatom wird ein 3s-Elektronenorbital vollendet. Na und Mg sind s-Elemente.
Für Aluminium und nachfolgende Elemente ist die 3p-Unterebene mit Elektronen gefüllt.
Die Elemente der dritten Periode haben ungefüllte 3d-Orbitale.
Alle Elemente von Al bis Ar sind p-Elemente. s- und p-Elemente bilden die wichtigsten Untergruppen im Periodensystem.

Elemente der vierten - siebten Periode
An den Kalium- und Calciumatomen erscheint eine vierte Elektronenschicht, die 4s-Unterebene ist gefüllt, da sie weniger Energie hat als die 3d-Unterebene.
K, Ca - s-Elemente in den Hauptuntergruppen enthalten. Für Atome von Sc bis Zn ist die 3d-Unterebene mit Elektronen gefüllt. Dies sind 3D-Elemente. Sie gehören zu den sekundären Nebengruppen, sie haben eine vorgefüllte äußere Elektronenschicht, sie werden als Übergangselemente bezeichnet.
Achten Sie auf die Struktur der Elektronenhüllen von Chrom- und Kupferatomen. Bei ihnen kommt es zu einem „Ausfall“ eines Elektrons von der 4s- in die 3d-Unterebene, was durch die größere Energiestabilität der resultierenden elektronischen Konfigurationen 3d 5 und 3d 10 erklärt wird:

Im Zinkatom ist die dritte Elektronenschicht abgeschlossen - alle 3s-, 3p- und 3d-Unterebenen sind darin ausgefüllt, insgesamt befinden sich 18 Elektronen darauf. In den Elementen nach Zink wird weiterhin die vierte Elektronenschicht aufgefüllt, die 4p-Unterebene.
Elemente von Ga bis Kr sind p-Elemente.
Die äußere Schicht (vierte) des Kryptonatoms ist vollständig und hat 8 Elektronen. Aber in der vierten Elektronenschicht können nur 32 Elektronen sein; die 4d- und 4f-Unterebenen des Kryptonatoms bleiben noch unbesetzt Die Elemente der fünften Periode füllen die Unterebenen in folgender Reihenfolge: 5s - 4d - 5p. Und es gibt auch Ausnahmen im Zusammenhang mit " Versagen» Elektronen, y 41 Nb, 42 Mo, 44 Ru, 45 Rh, 46 Pd, 47 Ag.
In der sechsten und siebten Periode erscheinen f-Elemente, d. h. Elemente, in denen die 4f- bzw. 5f-Unterebenen der dritten äußeren elektronischen Schicht gefüllt sind.
4f-Elemente werden Lanthanide genannt.
5f-Elemente werden Actiniden genannt.
Die Reihenfolge der Füllung elektronischer Unterebenen in den Atomen der Elemente der sechsten Periode: 55 Cs und 56 Ba - 6s-Elemente; 57 La … 6s 2 5d x - 5d-Element; 58 Ce - 71 Lu - 4f-Elemente; 72 Hf - 80 Hg - 5d-Elemente; 81 T1 - 86 Rn - 6d-Elemente. Aber auch hier gibt es Elemente, bei denen die Reihenfolge der Füllung elektronischer Orbitale „verletzt“ ist, was z. Je nachdem, welche Unterebene des Atoms zuletzt mit Elektronen gefüllt ist, werden alle Elemente in vier elektronische Familien oder Blöcke eingeteilt:
- s-Elemente. Die s-Unterebene der äußeren Ebene des Atoms ist mit Elektronen gefüllt; s-Elemente umfassen Wasserstoff, Helium und Elemente der Hauptuntergruppen der Gruppen I und II.
- p-Elemente. Die p-Unterebene der äußeren Ebene des Atoms ist mit Elektronen gefüllt; p-Elemente umfassen Elemente der Hauptuntergruppen der III-VIII-Gruppen.
- d-Elemente. Die d-Unterebene der voräußeren Ebene des Atoms ist mit Elektronen gefüllt; d-Elemente schließen Elemente sekundärer Untergruppen der Gruppen I-VIII ein, d. h. Elemente von interkalaren Dekaden großer Perioden, die zwischen s- und p-Elementen liegen. Sie werden auch Übergangselemente genannt.
- f-Elemente. Die f-Unterebene der dritten äußeren Ebene des Atoms ist mit Elektronen gefüllt; dazu gehören die Lanthanide und Antinoide.

Der Schweizer Physiker W. Pauli stellte 1925 fest, dass es in einem Atom in einem Orbital nicht mehr als zwei Elektronen mit entgegengesetztem (antiparallelem) Spin (übersetzt aus dem Englischen - „Spindel“) geben kann, d.h. mit solchen Eigenschaften, die man sich bedingt vorstellen kann die Drehung eines Elektrons um seine imaginäre Achse: im Uhrzeigersinn oder gegen den Uhrzeigersinn.

Dieses Prinzip heißt Pauli-Prinzip. Wenn sich ein Elektron im Orbital befindet, wird es als ungepaart bezeichnet, wenn es zwei gibt, handelt es sich um gepaarte Elektronen, dh Elektronen mit entgegengesetztem Spin. Die Abbildung zeigt ein Diagramm der Aufteilung der Energieniveaus in Unterniveaus und der Reihenfolge, in der sie gefüllt werden.


Sehr oft wird die Struktur der Elektronenhüllen von Atomen mithilfe von Energie- oder Quantenzellen dargestellt - sie schreiben die sogenannten grafischen elektronischen Formeln auf. Für diese Aufzeichnung wird die folgende Notation verwendet: Jede Quantenzelle wird durch eine Zelle bezeichnet, die einem Orbital entspricht; jedes Elektron ist durch einen der Richtung des Spins entsprechenden Pfeil gekennzeichnet. Beim Schreiben einer grafischen elektronischen Formel sollten zwei Regeln beachtet werden: Pauli-Prinzip und die Regel von F. Hund, wonach Elektronen freie Zellen zunächst einzeln besetzen und gleichzeitig den gleichen Spinwert haben, und sich erst dann paaren, aber die Spins nach dem Pauli-Prinzip bereits entgegengesetzt gerichtet sein werden.
Hundsche Regel und Paulisches Prinzip
Hundsche Regel- die Regel der Quantenchemie, die die Reihenfolge des Füllens der Orbitale einer bestimmten Unterschicht bestimmt und wie folgt formuliert ist: Der Gesamtwert der Spinquantenzahl der Elektronen dieser Unterschicht sollte maximal sein. 1925 von Friedrich Hund formuliert.
Das bedeutet, dass in jedem der Orbitale der Unterschicht zunächst ein Elektron aufgefüllt wird und erst nach Erschöpfung der unbesetzten Orbitale ein zweites Elektron zu diesem Orbital hinzukommt. In diesem Fall befinden sich in einem Orbital zwei Elektronen mit halbzahligen Spins entgegengesetzten Vorzeichens, die sich paaren (eine Zwei-Elektronen-Wolke bilden) und dadurch der Gesamtspin des Orbitals gleich Null wird.
Andere Formulierung: Unten in Energie liegt der atomare Term, für den zwei Bedingungen erfüllt sind.
- Die Vielfalt ist maximal
- Wenn die Multiplizitäten zusammenfallen, ist der Gesamtbahnimpuls L maximal.
Analysieren wir diese Regel am Beispiel des Füllens der Orbitale der p-Unterebene P- Elemente der zweiten Periode (dh von Bor bis Neon (im folgenden Diagramm zeigen horizontale Linien Orbitale, vertikale Pfeile Elektronen und die Richtung des Pfeils die Ausrichtung des Spins an).
Klechkovskys Regel
Klechkovskys Regel - Wenn die Gesamtzahl der Elektronen in Atomen zunimmt (mit einer Zunahme der Ladungen ihrer Kerne oder der Ordnungszahlen chemischer Elemente), werden Atomorbitale so besetzt, dass das Auftreten von Elektronen in Orbitalen mit höherer Energie nur davon abhängt die Hauptquantenzahl n und hängt nicht von allen anderen Quantenzahlen ab, auch nicht von denen aus l. Physikalisch bedeutet dies, dass in einem wasserstoffähnlichen Atom (ohne Interelektronenabstoßung) die Umlaufenergie eines Elektrons nur durch die räumliche Entfernung der Elektronenladungsdichte vom Kern bestimmt wird und nicht von den Eigenschaften seiner Bewegung abhängt im Bereich des Kerns.
Klechkovskys empirische Regel und die daraus entstehende Folge von Folgen einer etwas widersprüchlichen Realenergiefolge von Atomorbitalen nur in zwei gleichartigen Fällen: für Atome Cr, Cu, Nb, Mo, Ru, Rh, Pd, Ag, Pt, Au kommt es zu einem „Ausfall“ eines Elektrons mit s-Unterebene der äußeren Schicht zur d-Unterebene der vorherigen Schicht, was zu einem energetisch stabileren Zustand des Atoms führt, nämlich: nach Auffüllen des Orbitals 6 mit zwei Elektronen S