capacité en oxygène. capacité en oxygène du sang
Lire aussi
1. Ventilation des poumons. Ventilation par le sang des poumons. Espace mort physiologique. Ventilation alvéolaire.
2. Perfusion des poumons avec du sang. Effet de la gravité sur la ventilation des poumons. Effet de la gravité sur la perfusion pulmonaire de sang.
3. Coefficient des rapports ventilation-perfusion dans les poumons. Échange gazeux dans les poumons.
4. Composition de l'air alvéolaire. Composition gazeuse de l'air alvéolaire.
5. Tension des gaz dans les capillaires sanguins des poumons. Le taux de diffusion de l'oxygène et du dioxyde de carbone dans les poumons. L'équation de Fick.
7. L'affinité de l'hémoglobine pour l'oxygène. Modification de l'affinité de l'hémoglobine pour l'oxygène. Effet Bohr.
8. Dioxyde de carbone. transport de dioxyde de carbone.
9. Le rôle des érythrocytes dans le transport du dioxyde de carbone. Effet Holden.
10. Régulation de la respiration. Régulation de la ventilation pulmonaire.
La circulation sanguine remplit l'une des fonctions les plus importantes transfert d'oxygène des poumons aux tissus, et gaz carbonique- des tissus aux poumons. La consommation d'oxygène par les cellules tissulaires peut varier considérablement, par exemple lors du passage d'un état de repos à activité physique et vice versa. A cet égard, le sang doit disposer d'importantes réserves nécessaires pour augmenter sa capacité à transporter l'oxygène des poumons vers les tissus, et le gaz carbonique en sens inverse.
transport d'oxygène.
A 37 C, la solubilité de 02 dans le liquide est de 0,225 ml l-1 kPa-1 (0,03 ml/l/mm Hg). Dans des conditions normales de pression partielle d'oxygène dans l'air alvéolaire, soit 13,3 kPa ou 100 mm Hg, 1 l le plasma sanguin peut transporter seulement 3 ml 02, ce qui n'est pas suffisant pour la vie de l'organisme dans son ensemble. Au repos, le corps humain consomme environ 250 ml d'oxygène par minute. Pour que les tissus reçoivent une telle quantité d'oxygène dans un état physiquement dissous, le cœur doit pomper une énorme quantité de sang par minute. Dans l'évolution des êtres vivants, le problème du transport de l'oxygène a été résolu plus efficacement grâce à la réaction chimique avec l'hémoglobine érythrocytaire. L'oxygène est transporté par le sang des poumons vers les tissus du corps par les molécules d'hémoglobine, qui sont contenues dans les globules rouges.
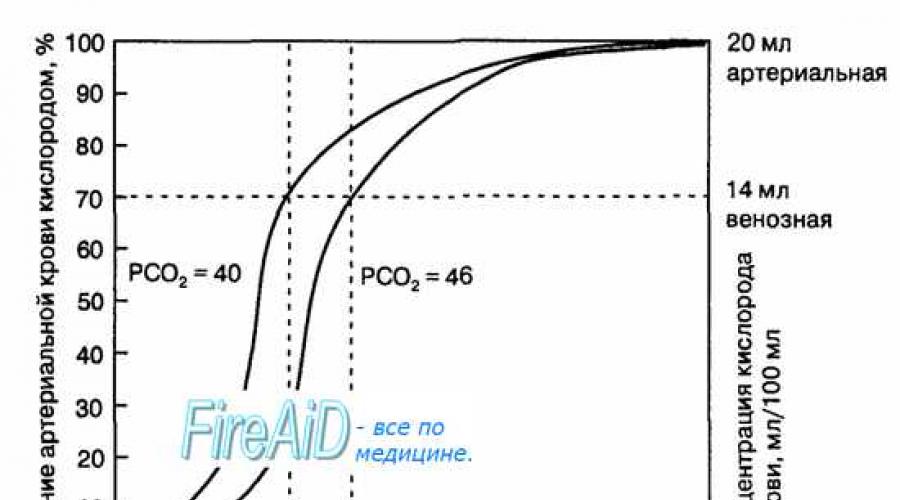
L'hémoglobine est capable de capter l'oxygène de l'air alvéolaire (le composé est appelé oxyhémoglobine) et libère quantité requise l'oxygène dans les tissus. Une caractéristique de la réaction chimique de l'oxygène avec l'hémoglobine est que la quantité d'oxygène lié est limitée par le nombre de molécules d'hémoglobine dans les globules rouges. La molécule d'hémoglobine possède 4 sites de liaison à l'oxygène qui interagissent de telle sorte que la relation entre la pression partielle d'oxygène et la quantité d'oxygène transportée dans le sang a une forme en S, appelée courbe de saturation ou de dissociation de l'oxyhémoglobine (Fig. 10.18). A une pression partielle d'oxygène de 10 mm Hg. Art. la saturation de l'hémoglobine en oxygène est d'environ 10% et à P02 30 mm Hg. Art. - 50-60 %. Avec une nouvelle augmentation de la pression partielle d'oxygène à partir de 40 mm Hg. Art. jusqu'à 60 mmHg Art. il y a une diminution de la pente de la courbe de dissociation de l'oxyhémoglobine et le pourcentage de sa saturation en oxygène augmente dans la plage de 70-75 à 90%, respectivement. Puis la courbe de dissociation de l'oxyhémoglobine commence à prendre une position quasi horizontale, depuis une augmentation de la pression partielle d'oxygène de 60 à 80 mm Hg. Art. provoque une augmentation de 6% de la saturation en hémoglobine en oxygène. Dans la gamme de 80 à 100 mm Hg. Art. le pourcentage de formation d'oxyhémoglobine est d'environ 2. En conséquence, la courbe de dissociation de l'oxyhémoglobine se transforme en une ligne horizontale et le pourcentage de saturation de l'hémoglobine en oxygène atteint la limite, c'est-à-dire 100. La saturation de l'hémoglobine en oxygène sous l'influence de P02 caractérise une sorte de "l'appétit" moléculaire de ce composé pour l'oxygène.
Pente de courbe importante saturation de l'hémoglobine en oxygène dans la plage de pression partielle de 20 à 40 mm Hg. Art. contribue au fait que dans les tissus du corps, une quantité importante d'oxygène peut diffuser du sang dans les conditions d'un gradient de sa pression partielle entre le sang et les cellules tissulaires (au moins 20 mm Hg). Un pourcentage insignifiant de saturation de l'hémoglobine en oxygène dans la plage de sa pression partielle de 80 à 100 mm Hg. Art. contribue au fait qu'une personne sans risque de réduire la saturation du sang artériel en oxygène peut se déplacer dans la plage d'altitudes jusqu'à 2000 m au-dessus du niveau de la mer.
 Riz. 10.18. Courbe de dissociation de l'oxyhémoglobine. Limites de fluctuation de la courbe à PC02 = 40 mm Hg. Art. (sang artériel) et PC02 = 46 mm Hg. Art. (sang veineux) montrent un changement dans l'affinité de l'hémoglobine pour l'oxygène ( Effet Hoden).
Riz. 10.18. Courbe de dissociation de l'oxyhémoglobine. Limites de fluctuation de la courbe à PC02 = 40 mm Hg. Art. (sang artériel) et PC02 = 46 mm Hg. Art. (sang veineux) montrent un changement dans l'affinité de l'hémoglobine pour l'oxygène ( Effet Hoden).
Réserves totales d'oxygène dans le corps sont dues à sa quantité, qui est à l'état lié avec les ions Fe2 + dans la composition des molécules organiques d'hémoglobine dans les érythrocytes et de myoglobine dans les cellules musculaires.
Un gramme d'hémoglobine lie 1,34 ml 02. Par conséquent, normalement, à une concentration d'hémoglobine de 150 g / l, chaque 100 ml de sang peut transporter 20,0 ml 02.
La quantité de 02 qui peut se lier à l'hémoglobine des globules rouges lorsqu'elle est saturée à 100 % de sa quantité est appelée capacité en oxygène de l'hémoglobine. Un autre indicateur de la fonction respiratoire du sang est la teneur en 02 dans le sang ( capacité en oxygène du sang), qui reflète sa véritable quantité, à la fois associée à l'hémoglobine et physiquement dissoute dans le plasma. Comme le sang artériel normal est saturé à 97 % en oxygène, 100 ml de sang artériel contiennent environ 19,4 ml d'O2.
La quantité maximale d'oxygène lié de manière réversible par le sang ; exprimé en pourcentage en volume ; dépend de la concentration d'hémoglobine dans le sang. Capacité en oxygène du sang humain env. 18 20% ... Grand dictionnaire encyclopédique
capacité en oxygène du sang- la quantité maximale d'oxygène qui peut être liée dans 100 ml de sang ... Grand dictionnaire médical
capacité en oxygène du sang- la quantité maximale d'oxygène lié de manière réversible par le sang ; exprimé en pourcentage en volume ; dépend de la concentration d'hémoglobine dans le sang. La capacité humaine en oxygène est d'environ 18 à 20 %. * * * CAPACITÉ EN OXYGÈNE DU SANG CAPACITÉ EN OXYGÈNE DU SANG,… … Dictionnaire encyclopédique
Oxygénothérapie- I Oxygénothérapie (traitement therapeia grec ; synonyme d'oxygénothérapie) l'utilisation de l'oxygène avec but thérapeutique. Principalement utilisé pour le traitement de l'hypoxie chez Formes variées insuffisance respiratoire aiguë et chronique, moins souvent pour ... ... Encyclopédie médicale
hypoxie- I L'hypoxie (hypoxie; grec hypo + latin oxy oxygène; synonyme: manque d'oxygène, manque d'oxygène) est un processus pathologique qui se produit lorsqu'il y a un apport insuffisant d'oxygène aux tissus corporels ou une violation de son utilisation dans ... ... Encyclopédie médicale
Échange de gaz- I Les échanges gazeux sont un ensemble de processus d'échanges gazeux entre le corps et environnement; consiste en la consommation d'oxygène et la libération de dioxyde de carbone avec de petites quantités de produits gazeux et de vapeur d'eau. L'intensité de G. ... ... Encyclopédie médicale
Famille des Scombridae (Scombridae)- Les maquereaux sont un sous-ordre bien séparé, dont tous les représentants vivent dans la mer et mènent une vie pélagique, n'étant associés au fond à aucune période cycle de la vie. Ils se caractérisent par un corps fusiforme allongé ... Encyclopédie biologique
thon rouge- (Thunnus thynnus) voir aussi FAMILLE DU MAQUEREAU (SCOMBRIDAE) Le thon rouge est très gros poisson, atteignant une longueur de 3 m et une masse d'environ 560 kg. Ce géant a une épaisse, presque ronde la Coupe transversale, corps fusiforme, fortement ... ... Poisson de Russie. Annuaire
Arrêt respiratoire- I L'insuffisance respiratoire est un état pathologique dans lequel le système respiratoire externe ne fournit pas composition du gaz sang, ou il n'est fourni que par un travail respiratoire accru, se manifestant par un essoufflement. C'est la définition... Encyclopédie médicale
La structure des mammifères- L'apparence des mammifères est diverse. Cela est dû à l'étonnante variété de leurs conditions de vie - la surface du sol, les cimes des arbres, le sol, l'eau, l'air. La taille du corps varie considérablement de 3,8 cm avec ... ... Encyclopédie biologique
La quantité d'oxygène que l'hémoglobine peut lier lorsqu'elle est complètement saturée s'appelle la capacité en oxygène du sang (KEK).
1 gramme d'Hb lie 1,39 ml d'O2
Facteur d'utilisation de l'oxygène
Le coefficient d'utilisation de l'oxygène est la quantité d'oxygène abandonnée lors du passage du sang à travers les capillaires tissulaires, rapportée à la capacité en oxygène du sang.
La tension d'oxygène dans le sang artériel des capillaires est de 100 mm Hg. Art.
Sur les membranes des cellules situées entre les capillaires 20 mm Hg. Art.
Dans les mitochondries - 0,5 mm Hg. Art.
Coefficient respiratoire
Le rapport entre le CO2 formé à la suite de l'oxydation et la quantité d'oxygène consommée dans le corps est appelé fréquence respiratoire.
Au repos, le corps consomme en moyenne 250 ml d'O2 par minute et libère environ 230 ml de CO2.
De l'O2 total de l'air inhalé, seulement 1/3 pénètre dans le sang à travers la barrière air-sang dans les poumons.
D'importance majeure sont relation optimale ventilation alvéolaire à la circulation sanguine
Échange de gaz et transport de CO2
Le flux de CO2 dans les alvéoles pulmonaires à partir du sang provient des sources suivantes :
Du CO 2 dissous dans le plasma sanguin (5-10%),
A partir de bicarbonates (80-90%).
Des composés carbamiques des érythrocytes (5-15%), capables de se dissocier
Rôle physiologique du monoxyde d'azote
L'oxyde nitrique réduit la libération et la production d'hormones de stress, est capable de limiter les dommages causés par le stress à l'organisme.
Une augmentation de la production de NO se produit sous l'action de facteurs de stress à court terme ou modérés, et une diminution de sa formation a été révélée dans des conditions d'effets à long terme et néfastes des facteurs de stress.
Fonctions physiologiques du CO
1. Neurotransmission
2. Vasodilatation
3.Relaxation des muscles lisses des organes internes
4.Suppression de l'agrégation plaquettaire
5.Effet anti-prolifératif.
Explication physiologique:
CO - effet tonique, car : CO - molécule à longue durée de vie, faible effet vasodilatateur.
Le NO est un effet phasique, car : Le NO est une molécule à vie courte avec un fort effet vasodilatateur.
Conférence 18
Régulation de la respiration
La régulation de la respiration externe est une réaction systémique de l'organisme associée à une modification du volume minute de respiration (MOD), et donc du volume minute de circulation sanguine (MOV) dans conditions diverses assurer la constance de la composition gazeuse de l'environnement interne du corps, et donc l'homéostasie en général.
Le contenu et l'équilibre de l'O2 et du CO2 dans le sang artériel sont particulièrement importants pour le déroulement normal des processus vitaux du corps.
Ceci est assuré par l'établissement d'un équilibre gazeux (hors équilibre) dans les capillaires des poumons, qui assure les processus de transfert de masse synchrone d'oxygène et de CO2 dans le compartiment pulmonaire.
Haldane est arrivé à la conclusion que le principal facteur de régulation de la respiration est la tension du dioxyde de carbone dans le sang artériel.
Sa principale conclusion est que une augmentation du dioxyde de carbone dans le sang artériel entraîne augmentation de MOD, est restée fidèle à ce jour.
capacité en oxygène du sang- la quantité d'oxygène qui peut être liée par le sang lorsqu'il est complètement saturé ; exprimée en pourcentage en volume (% vol.) ; dépend de la concentration d'hémoglobine dans le sang. La détermination de la capacité en oxygène du sang est importante pour caractériser la fonction respiratoire du sang. La capacité en oxygène du sang humain est d'environ 18 à 20 % vol.
Voir également
Donnez votre avis sur l'article "Capacité en oxygène du sang"
Liens
| hélice alpha | Cet article en biochimie est un bout . Vous pouvez aider le projet en y ajoutant. |
|
||||||||||||||||||||||
Un extrait caractérisant la capacité en oxygène du sang
– Où est ce Grand Temple, Radomir ? demanda Madeleine surprise.- Dans un merveilleux pays lointain... Tout au "sommet" du monde... (c'est-à-dire pôle Nord, l'ancien pays d'Hyperborée - Daaria), - tranquillement, comme s'il était entré dans un passé infiniment lointain, murmura Radomir. « Là se dresse une montagne sacrée faite par l'homme, que ni la nature, ni le temps, ni les hommes ne peuvent détruire. Car cette montagne est éternelle... C'est le Temple de la Connaissance Éternelle. Temple de nos anciens dieux, Maria...
Une fois, il y a longtemps, leur clé scintillait au sommet de la montagne sacrée - ce cristal vert qui protégeait la Terre, ouvrait les âmes et enseignait les dignes. Seulement maintenant nos dieux sont partis. Et depuis, la Terre est plongée dans les ténèbres, que l'homme lui-même n'a pas encore pu détruire. Il y a encore trop d'envie et de méchanceté en lui. Et aussi paresseux...
Capacité en oxygène du sang (KEK) et indice de couleur (KP)
KEK est le volume d'oxygène contenu sang VIH. La KEK dépend de la quantité d'hémoglobine du VIH dans le sang et de ses propriétés de fixation et de libération d'oxygène.
1 g d'Hb peut ajouter au maximum 1,34 ml d'oxygène (nombre de Hüfner). 1 litre de sang contient en moyenne 140 g d'Hb, qui peut lier 140 1,34 = 187,6 ml d'oxygène.
Dans le plasma sanguin à Po2 100 mm Hg. Art. seulement 3 ml d'oxygène se dissolvent dans 1 litre. Ainsi, le rôle principal dans le transport de l'oxygène appartient à l'hémoglobine des érythrocytes.
Une molécule d'hémoglobine contient 4 molécules d'hème, ne peut transporter plus de quatre molécules d'oxygène, tandis que la valence du fer ne change pas, c'est pourquoi l'ajout d'oxygène (O2) à l'hémoglobine (Hb) est appelé oxygénation, entraînant la formation d'oxyhémoglobine (HbO2). En spectroscopie, il présente deux raies d'absorption dans la partie jaune-vert du spectre et donne au sang artériel une couleur rouge vif.
La capacité de l'hémoglobine à fixer l'oxygène augmente avec une diminution des facteurs suivants :
■ Pso2 dans le sang, c'est-à-dire quand hypocapnie,
■ température du sang - à hypothermie
alcalose
■ la concentration d'acide 2,3-diphosphoglycérique (2,3-DFG) dans les érythrocytes, qui se forme lors de la glycolyse.
La capacité de l'oxyhémoglobine à donner de l'oxygène augmente en raison de la croissance de tels facteurs dans le sang:
■ RSO, dans le sang - à hypercapnie,
■ température du sang - à hyperthermie
■ concentration d'ions hydrogène - à acidose
■ Concentration de 2,3-DPG dans les érythrocytes au cours de la glycolyse.
indice de couleur- une valeur relative qui caractérise la saturation de l'érythrocyte en hémoglobine et reflète leur pourcentage. Si l'on prend une valeur pour 100% d'hémoglobine qui est classiquement égale à 166,7 g/l, et pour 100% d'érythrocytes - 5 1012/l, alors la CP sera de 1. Normalement, la CP varie de 0,85 à 1.
Le rôle du fer
Le fer est élément important dans la formation de l'hémoglobine et de nombreuses enzymes. La quantité totale de fer est d'environ 4 g, dont 65 % dans l'hémoglobine, environ 4 % dans la myoglobine, de 15 à 30 % - dans les cellules du système réticulo-endothélial et du parenchyme hépatique sous forme de ferritine (Fig. 9.11).
La quantité de fer fournie avec les aliments dépend du régime alimentaire, mais doit être d'au moins 15 mg / jour.
L'absorption du fer dans l'intestin grêle dépend des facteurs suivants :
■ la présence de NSI dans le suc gastrique, grâce à laquelle il est libéré des complexes sous forme de Fe2 + et est activement absorbé dans la partie supérieure du duodénum, où pH = 3 :
■ sur les propriétés de Fe2+, plus soluble en milieu neutre que Fe3+ ;
■ des glycoprotéines de l'estomac, sécrétées par les cellules pariétales de la muqueuse.
Le fer, absorbé dans l'intestin grêle dans le sang, rejoint la protéine de transport plasmatique bêta-globuline, entraînant la formation de l'apotransférine, qui se transforme en transferrine et est transporté par le plasma vers les cellules de certains tissus, où il est libéré. Une caractéristique de la transferrine est qu'elle se lie fortement aux membranes des érythroblastes dans la moelle osseuse rouge, après quoi elle pénètre dans leur cytoplasme par endocytose. L'excès de fer s'installe dans toutes les cellules, mais surtout dans le système réticulo-endothélial et les hépatocytes du foie. Dans le cytoplasme des cellules, il se combine avec la protéine apôtre ferritine, à partir de laquelle il est formé ferritine . Une faible proportion de fer est retenue dans la fraction soluble - hémosidérine . Lorsque la quantité de fer dans le plasma chute de manière significative, elle peut être reconstituée avec de l'hémosidérine.
Les érythrocytes anciens (vivant jusqu'à 120 jours) sont détruits principalement dans la rate, l'hémoglobine est libérée des cellules et pénètre dans le système monocyte-macrophage, où le fer libre se forme sous forme de ferritine, qui peut être réutilisée pour la synthèse de hémoglobine. Environ 0,6 mg de fer est excrété par le corps
RIZ. 9.11.
quotidiennement, principalement avec des matières fécales. Une perte supplémentaire de fer se produit pendant le saignement. Chez les femmes, environ 0,7 mg de fer par jour est perdu pendant les menstruations. La carence totale en fer peut être déterminée par la formule :
Fer (mg) \u003d (Hb est normal - Hb du test) poids corporel (kg) 2,21 + 1000.
Un certain rôle dans l'érythropoïèse est attribué au cuivre, qui est amené dans la moelle osseuse par la circulation sanguine et favorise l'incorporation du fer dans la structure de l'hème. En l'absence de cuivre, les érythrocytes mûrissent au stade de réticulocytes, avec une carence, une anémie se développe.
Le rôle de la vitamine B12 (cobalamine) et acide folique
cobalamine - Il s'agit d'une molécule contenant un atome de cobalt au centre, associé à quatre cycles pyrolim et à des nucléotides. Il pénètre dans le corps avec de la nourriture animale. Le plus souvent, un manque de cobalamine est une conséquence de l'atrophie des cellules pariétales de l'estomac, de l'absence facteur interne Château, qui favorise l'absorption de la vitamine B12 dans l'iléon. Elle survient 4 à 10 ans après la malabsorption.
Une carence en acide folique, que l'on trouve dans légumes frais et fruits, survient trois semaines après l'arrêt de son utilisation avec de la nourriture.
Le manque de cobalamine (vitamine B12) ou d'acide folique entraîne une diminution de la synthèse de l'hémoglobine et des érythrocytes (anémie), l'apparition de mégaloblastes, ce qui indique une violation de la synthèse de l'ADN dans les mécanismes de l'érythropoïèse.