Totul despre aerul atmosferic. Ce este aerul și în ce constă
Citeste si
Compoziția gazoasă a aerului atmosferic
Compoziția gazoasă a aerului pe care îl respirăm este de 78% azot, 21% oxigen și 1% alte gaze. Dar în atmosfera marilor orașe industriale, acest raport este adesea încălcat. O proporție semnificativă este formată din impurități nocive cauzate de emisiile de la întreprinderi și vehicule. Transportul cu motor aduce multe impurități în atmosferă: hidrocarburi cu compoziție necunoscută, benzo (a) piren, dioxid de carbon, compuși de sulf și azot, plumb, monoxid de carbon.
Atmosfera este formată dintr-un amestec dintr-un număr de gaze - aer, în care sunt suspendate impurități coloidale - praf, picături, cristale etc. Compoziția aerului atmosferic se modifică puțin odată cu înălțimea. Totuși, începând de la o înălțime de aproximativ 100 km, alături de oxigenul molecular și azotul, apare și oxigenul atomic ca urmare a disocierii moleculelor și începe separarea gravitațională a gazelor. Peste 300 km predomină în atmosferă oxigenul atomic, peste 1000 km - heliu și apoi hidrogenul atomic. Presiunea și densitatea atmosferei scad odată cu înălțimea; aproximativ jumătate din masa totală a atmosferei este concentrată în cei 5 km inferiori, 9/10 - în cei 20 km inferiori și 99,5% - în cei 80 km inferiori. La altitudini de aproximativ 750 km, densitatea aerului scade la 10-10 g/m3 (în timp ce în apropierea suprafeței pământului este de aproximativ 103 g/m3), dar chiar și o densitate atât de mică este totuși suficientă pentru apariția aurorelor. Atmosfera nu are o limită superioară ascuțită; densitatea gazelor sale constitutive
Compoziția aerului atmosferic pe care fiecare dintre noi îl respiră include mai multe gaze, dintre care principalele sunt: azotul (78,09%), oxigenul (20,95%), hidrogen (0,01%) dioxid de carbon (dioxid de carbon) (0,03%) și inert. gaze (0,93%). În plus, în aer există întotdeauna o anumită cantitate de vapori de apă, a cărei cantitate se modifică întotdeauna cu temperatura: cu cât temperatura este mai mare, cu atât conținutul de vapori este mai mare și invers. Datorită fluctuațiilor cantității de vapori de apă din aer, procentul de gaze din acesta este de asemenea variabil. Toate gazele din aer sunt incolore și inodore. Greutatea aerului variază în funcție nu numai de temperatură, ci și de conținutul de vapori de apă din acesta. La aceeași temperatură, greutatea aerului uscat este mai mare decât a aerului umed, deoarece vaporii de apă sunt mult mai ușori decât vaporii de aer.
Tabelul arată compozitia gazelor atmosfera în raportul de masă în volum, precum și durata de viață a componentelor principale:
| Componentă | % din volum | % masa |
| N 2 | 78,09 | 75,50 |
| O2 | 20,95 | 23,15 |
| Ar | 0,933 | 1,292 |
| CO2 | 0,03 | 0,046 |
| Ne | 1,8 10 -3 | 1,4 10 -3 |
| El | 4,6 10 -4 | 6,4 10 -5 |
| CH 4 | 1,52 10 -4 | 8,4 10 -5 |
| kr | 1,14 10 -4 | 3 10 -4 |
| H2 | 5 10 -5 | 8 10 -5 |
| N2O | 5 10 -5 | 8 10 -5 |
| Xe | 8,6 10 -6 | 4 10 -5 |
| O 3 | 3 10 -7 - 3 10 -6 | 5 10 -7 - 5 10 -6 |
| Rn | 6 10 -18 | 4,5 10 -17 |
Proprietățile gazelor care formează aerul atmosferic se modifică sub presiune.
De exemplu: oxigenul sub presiune mai mare de 2 atmosfere are un efect toxic asupra organismului.
Azotul sub presiune peste 5 atmosfere are efect narcotic (intoxicație cu azot). O creștere rapidă de la adâncime provoacă boală de decompresie datorită eliberării rapide a bulelor de azot din sânge, ca și cum ar fi spuma.
O creștere a dioxidului de carbon cu peste 3% în amestecul respirator provoacă moartea.
Fiecare componentă care face parte din aer, cu o creștere a presiunii până la anumite limite, devine o otravă care poate otravi organismul.
Studii ale compoziției gazelor din atmosferă. chimia atmosferică
Pentru istoria dezvoltării rapide a unei ramuri relativ tinere a științei numită chimia atmosferică, termenul „spurt” (aruncare) folosit în sporturile de mare viteză este cel mai potrivit. Lovitura de la pistolul de pornire, probabil, a fost două articole publicate la începutul anilor 1970. Ei s-au ocupat de posibila distrugere a ozonului stratosferic de către oxizii de azot - NO și NO 2 . Primul i-a aparținut viitorului laureat al Premiului Nobel și apoi unui angajat al Universității din Stockholm, P. Krutzen, care a considerat sursa probabilă de oxizi de azot din stratosferă ca fiind protoxidul de azot natural N 2 O care se descompune sub acțiunea luminii solare. Autorul celui de-al doilea articol, un chimist de la Universitatea din California din Berkeley G. Johnston, a sugerat că oxizii de azot apar în stratosferă ca urmare a activității umane, și anume, în timpul emisiilor de produse de combustie. motoare cu reactie aeronave de mare altitudine.
Desigur, ipotezele de mai sus nu au apărut de la zero. Raportul dintre cel puțin componentele principale din aerul atmosferic - molecule de azot, oxigen, vapori de apă etc. - era cunoscut mult mai devreme. Deja în a doua jumătate a secolului al XIX-lea. în Europa s-au făcut măsurători ale concentrației de ozon în aerul de suprafață. În anii 1930, omul de știință englez S. Chapman a descoperit mecanismul formării ozonului într-o atmosferă pur de oxigen, indicând un set de interacțiuni ale atomilor și moleculelor de oxigen, precum și a ozonului în absența oricăror alte componente ale aerului. Cu toate acestea, la sfârșitul anilor 1950, măsurătorile meteorologice cu rachete au arătat că în stratosferă era mult mai puțin ozon decât ar trebui să fie conform ciclului de reacție Chapman. Deși acest mecanism rămâne fundamental până în zilele noastre, a devenit clar că există și alte procese care sunt, de asemenea, implicate activ în formarea ozonului atmosferic.
Este de menționat că, la începutul anilor 1970, cunoștințele în domeniul chimiei atmosferice au fost obținute în principal datorită eforturilor oamenilor de știință individuali, ale căror cercetări nu au fost unite de niciun concept semnificativ social și au fost cel mai adesea pur academice. Un alt lucru este munca lui Johnston: conform calculelor sale, 500 de avioane, care zboară 7 ore pe zi, ar putea reduce cantitatea de ozon stratosferic cu cel puțin 10%! Și dacă aceste evaluări ar fi corecte, atunci problema ar deveni imediat una socio-economică, deoarece în acest caz toate programele de dezvoltare a aviației de transport supersonic și a infrastructurii aferente ar trebui să sufere o ajustare semnificativă, și poate chiar o închidere. În plus, atunci pentru prima dată a apărut cu adevărat întrebarea că activitatea antropică ar putea provoca nu un cataclism local, ci global. Desigur, în situația actuală, teoria avea nevoie de o verificare foarte dură și în același timp promptă.
Reamintim că esența ipotezei de mai sus a fost că oxidul de azot reacționează cu ozonul NO + O 3 ® ® NO 2 + O 2, apoi dioxidul de azot format în această reacție reacționează cu atomul de oxigen NO 2 + O ® NO + O 2 , restabilind astfel prezența NO în atmosferă, în timp ce molecula de ozon se pierde iremediabil. În acest caz, o astfel de pereche de reacții, constituind ciclul catalitic al azotului de distrugere a ozonului, se repetă până când orice procese chimice sau fizice duc la îndepărtarea oxizilor de azot din atmosferă. Deci, de exemplu, NO 2 este oxidat la acid azotic HNO 3, care este foarte solubil în apă și, prin urmare, este îndepărtat din atmosferă prin nori și precipitații. Ciclul catalitic al azotului este foarte eficient: o moleculă de NO reușește să distrugă zeci de mii de molecule de ozon în timpul șederii în atmosferă.
Dar, după cum știți, problemele nu vin singure. Curând, specialiştii din universităţile americane – Michigan (R. Stolyarsky şi R. Cicerone) şi Harvard (S. Wofsi şi M. McElroy) – au descoperit că ozonul ar putea avea un inamic şi mai nemiloasă – compuşii clorului. Conform estimărilor acestora, ciclul catalitic al clorului de distrugere a ozonului (reacțiile Cl + O 3 ® ClO + O 2 și ClO + O ® Cl + O 2) a fost de câteva ori mai eficient decât cel cu azot. Singurul motiv pentru un optimism prudent a fost că cantitatea de clor natural din atmosferă este relativ mică, ceea ce înseamnă că efectul general al impactului său asupra ozonului poate să nu fie prea puternic. Cu toate acestea, situația s-a schimbat dramatic când, în 1974, angajații Universității din California din Irvine, S. Rowland și M. Molina, au stabilit că sursa de clor din stratosferă este compușii clorofluorohidrocarburi (CFC), care sunt utilizați pe scară largă în unități frigorifice, pachete de aerosoli etc. Fiind neinflamabile, netoxice și pasive din punct de vedere chimic, aceste substanțe sunt transportate lent prin curenții de aer ascendenți de la suprafața pământului spre stratosferă, unde moleculele lor sunt distruse de lumina soarelui, având ca rezultat eliberarea de atomi de clor liber. productie industriala CFC-urile, care au început în anii 1930, iar emisiile lor în atmosferă au crescut constant în toți anii următori, în special în anii 70 și 80. Astfel, într-o perioadă foarte scurtă de timp, teoreticienii au identificat două probleme în chimia atmosferică cauzate de poluarea antropică intensă.
Cu toate acestea, pentru a testa viabilitatea ipotezelor propuse, a fost necesar să se realizeze multe sarcini.
In primul rand, extinde cercetările de laborator, în timpul cărora ar fi posibil să se determine sau să clarifice vitezele reacțiilor fotochimice dintre diferitele componente ale aerului atmosferic. Trebuie spus că datele foarte slabe despre aceste viteze care existau la acea vreme au avut și erori destul de bune (până la câteva sute de procente). În plus, condițiile în care s-au făcut măsurătorile, de regulă, nu corespundeau prea mult cu realitățile atmosferei, ceea ce a agravat grav eroarea, deoarece intensitatea majorității reacțiilor depindea de temperatură, iar uneori de presiunea sau aerul atmosferic. densitate.
În al doilea rând, studiază intens proprietățile optice de radiație ale unui număr de gaze atmosferice mici în condiții de laborator. Moleculele unui număr semnificativ de componente ale aerului atmosferic sunt distruse de radiația ultravioletă a Soarelui (în reacțiile de fotoliză), printre acestea nu se numără doar CFC-urile menționate mai sus, ci și oxigenul molecular, ozonul, oxizii de azot și multe altele. Prin urmare, estimările parametrilor fiecărei reacții de fotoliză au fost la fel de necesare și importante pentru reproducerea corectă a condițiilor atmosferice. procese chimice, precum și vitezele de reacții între diferite molecule.
AER
amestec de gaze care formează atmosfera Pământului, extinzându-se la o altitudine de 1000-1200 km. Până la o înălțime de aprox. 11 km compoziția atmosferei rămâne neschimbată. Acest strat se numește troposferă. Ea joacă majoritatea proceselor meteorologice care determină vremea. Aici este o circulație intensivă a aerului, sunt vânturi, furtuni și uragane, turbulențele sunt mari. Troposfera conține aproape toți vaporii de apă din atmosferă și aproape tot praful de aer și, prin urmare, aici se formează norii în cea mai mare parte. Deasupra troposferei, extinzându-se pe aproximativ 50 km, se află un strat al stratosferei. Aici, curenți uriași de aer relativ calm circulă pe distanțe lungi fără perturbări semnificative. În partea inferioară a stratosferei se formează nori rari, formați din cele mai mici cristale de gheață. Deasupra stratosferei la o înălțime de aprox. Mezosfera se întinde pe 80 km - stratul în care se atinge cea mai scăzută temperatură naturală a aerului, care este de aproximativ -110 ° C (160 K). Mai departe până la o înălțime de aprox. 720 km urmează stratul termosferei. Aici, moleculele de aer se mișcă atât de repede încât, dacă densitatea aerului ar fi aceeași ca la nivelul mării (și nu de miliarde de ori mai mică), atunci temperatura sa ar fi aproape de 3000 ° C. Stratul superior al atmosferei este exosfera. În el, aerul este extrem de rarefiat, iar ciocnirile moleculelor între ele sunt atât de rare încât majoritatea se deplasează de-a lungul unor traiectorii balistice simple, ca un glonț, iar unele dintre ele de-a lungul orbitelor eliptice, ca sateliții artificiali ai Pământului. O anumită fracțiune de molecule, în principal hidrogen și heliu, ating viteze la care este posibil să depășească limitele forțelor gravitaționale ale pământului și să se disipeze în spațiul dintre Pământ și Lună (vezi și ATMOSFERĂ). Dintre toate diferitele proprietăți ale aerului, cel mai important este că este necesar pentru viața pe Pământ. Existența oamenilor și a animalelor ar fi imposibilă fără oxigen. Deoarece respirația necesită oxigen în formă diluată, prezența altor gaze în aer este, de asemenea, vitală.
Compus. La nivelul mării și în troposferă, compoziția gazoasă a aerului (în vol%) este următoarea: azot - 78,08%, oxigen - 20,95%, argon - 0,93%, dioxid de carbon (dioxid de carbon) - 0,034%, hidrogen - 5 x 10-5%; în plus, există cantități „urme” ale așa-numitelor gaze nobile (sau inerte, rare): neon - 1,8 x 10-3%, heliu - 5,24 x 10-4%, cripton - 1 x 10-4% și xenon - 8 x 10-6%. Aerul din troposferă conține și cantități variabile de vapori de apă; umiditatea acestuia depinde de condițiile de temperatură și de altitudine. Atmosfera inferioară conține cantități variabile de praf și cenușă în suspensie, care se formează, de exemplu, în procesele de ardere și în timpul erupțiilor vulcanice. Prezența unor astfel de particule de aerosoli în aer este asociată culori deschise răsărituri și apusuri din cauza împrăștierii luminii solare asupra lor.
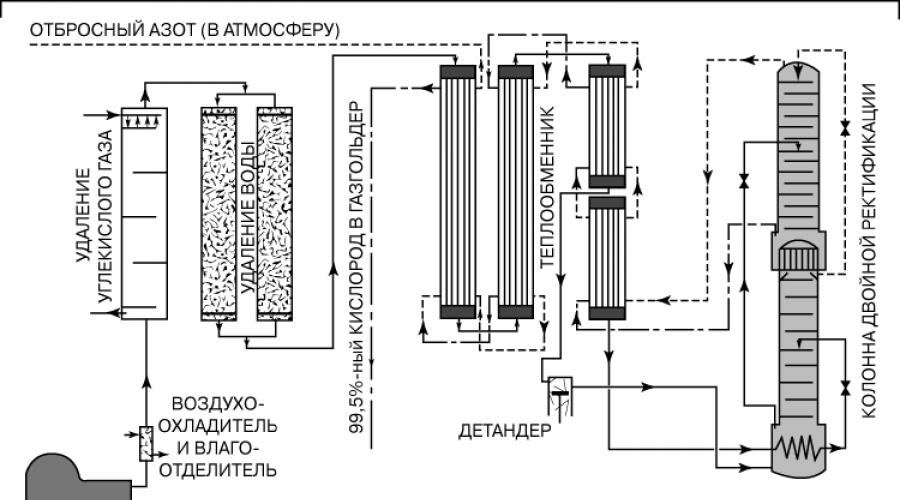
SEPARAREA AERULUI RECTIFICARE
Diverse gaze care alcătuiesc aerul atmosferic pot fi transformate într-o stare lichidă și chiar solidă dacă presiunea este crescută și temperatura este coborâtă în consecință. Oamenii au găsit utilizări numeroase și variate pentru aer. Scara de aplicare a componentelor de gaz din aerul atmosferic în știință și tehnologie, industrie și viața de zi cu zi sa extins de multe ori după ce a fost dezvoltată o metodă pentru separarea amestecului de aer în componente individuale. Această metodă constă în faptul că aerul este mai întâi transformat în stare lichidă, iar apoi supus distilarii sau rectificării (fracționării) în același mod în care țițeiul este separat în diferite produse petroliere. Pentru prima dată, lichefierea aerului a fost realizată cu succes în 1883 de Z. Vroblevsky și K. Olshevsky. Pentru aplicarea industrială a separării aerului de distilare, două circumstanțe sunt importante. În primul rând, gazele care formează aerul formează un amestec fizic, nu un compus chimic, iar în al doilea rând, punctele de fierbere ale diferitelor componente ale aerului diferă semnificativ. Mijloacele tehnice, create ținând cont de ambele, asigură o separare aproape completă a principalelor componente ale aerului și cu un grad înalt puritatea fiecărei componente. Procesul de separare a aerului se desfășoară în trei etape: 1) prepararea sau purificarea aerului, 2) transformarea aerului purificat într-o fază lichidă (lichefiere) și 3) rectificarea separarea unui amestec lichid în gaze separate.

Îndepărtarea impurităților.Înainte ca aerul să intre în admisia secțiunilor de lichefiere și rectificare ale instalației de separare a aerului, toate impuritățile sunt îndepărtate din aceasta, care fie sunt suspendate în aerul atmosferic sub formă de particule solide, fie se pot transforma cu ușurință în solide atunci când temperatura scade. În caz contrar, blocarea rapidă a canalelor înguste ale echipamentului este inevitabilă. Acești contaminanți includ vaporii de apă, praful, fumul și vaporii din alte substanțe, precum și dioxidul de carbon. Cea mai mare parte a acestor impurități este reținută de capcanele de ulei și umezeală, de regulă, după compresia compresorului. Uscarea aerului după comprimare este mai de preferat, deoarece în acest caz trebuie îndepărtată mai puțină apă sub formă de vapori, deoarece în timpul compresiei se transformă în cea mai mare parte într-un lichid. Uscarea ulterioară a aerului se realizează prin trecerea acestuia prin adsorbante cu alumină activată sau silicagel (dioxid de siliciu parțial deshidratat). Dioxidul de carbon poate fi îndepărtat chimic prin reacție cu hidroxid de potasiu (potasiu caustic) sau sodiu (sodă caustică). Cu toate acestea, aceste substanțe chimice sunt epuizate rapid și necesită o completare frecventă. În instalațiile mari de separare a aerului se folosesc schimbătoare de căldură, în care dioxidul de carbon și vaporii de apă sunt îndepărtați simultan, iar aerul care intră în sistem este răcit. Gazele ușor înghețate se depun sub formă solidă pe suprafețele metalice ale schimbătoarelor de căldură, care sunt menținute la temperaturi foarte scăzute prin fluxul de gaze separate care trec prin canalele lor interne. Sistemul este curățat periodic de impuritățile acumulate prin inversarea fluxului de gaze în schimbătorul de căldură.
Lichefiere. Aerul purificat intră în secțiunea de lichefiere și este răcit în sistemul de refrigerare mecanică până când cea mai mare parte se transformă într-un lichid. În funcție de presiunea la care aerul a fost comprimat inițial, temperatura acestuia scade aici la aproximativ 100 K. Presiunile ciclului variază de la 0,6 la 20 MPa. În timpul răcirii se folosește frigul gazelor separate anterior provenite din secția de distilare. Într-un schimbător de căldură proiectat optim, frigul gazelor separate este aproape complet transferat în aerul de intrare. În unele instalații, în special cele în care unele dintre gazele separate sunt preluate sub formă lichidă, pentru pre-răcire sunt prevăzute schimbătoare de căldură cu freon sau clorură de metil până la aproximativ -40 ° C (230 K). La temperaturile mai scăzute necesare pentru a lichefia aerul, lichidul de răcire este fie aerul care intra sau azot separat. Acest gaz, comprimat la o anumită presiune, antrenează o mașină de expansiune sau un expandator (compresor inversat). Expandându-se, gazul mișcă pistonul, care prin arborele cotit rotește generatorul, care îndeplinește funcția de „frână”. Deoarece gazul funcționează în timpul expansiunii în expandor, conținutul său de căldură și temperatura scad. La prima pornire a instalației, este necesară mai întâi răcirea acesteia la temperatura de funcționare, iar aceasta necesită mai mult frig decât în regimul de funcționare permanent (răcirea instalației). Răcirea poate fi efectuată și prin extinderea gazelor comprimate în faza gazoasă sau lichidă atunci când curg printr-o supapă de accelerație. În acest caz, scăderea temperaturii se datorează efectului Joule-Thomson (efect de sufocare). Aceste metode de răcire se bazează pe diferite efecte termodinamice, iar dacă sunt introduse în ciclul în succesiunea corectă, atunci poți folosi avantajele fiecăruia dintre ele
(Vezi si
Căldură;
TERMODINAMICĂ;
FIZICA TEMPERATURII JOSE).
Secțiunile de fluidizare și distilare care funcționează la temperaturi criogenice necesită bine izolatie termica exterioara. Prin urmare, dispozitivele acestor secțiuni sunt furnizate cu carcase umplute cu materiale termoizolante precum vata minerala, vată de sticlă și cenușă vulcanică poroasă. Materialele de construcție ale schimbătoarelor de căldură, coloanelor de distilare și conductelor de legătură sunt alese cu mare atenție. Oțelurile carbon devin fragile la temperaturi criogenice. Prin urmare, se preferă materiale precum cuprul, bronzul, alama, oțelul inoxidabil și aluminiul, care prezintă caracteristici excelente de rezistență în condiții criogenice.
Rectificare. Separarea aerului lichefiat în componente se realizează în aparate cilindrice verticale numite coloane de distilare. În interiorul unei astfel de coloane există un rând vertical de „tăvi” orizontale cu găuri prin care lichidul curge în jos, iar gazul se ridică din partea inferioară a coloanei, intrând în contact cu lichidul de pe plăci. În instalațiile de extracție cu un grad ridicat de puritate a tuturor componentelor aerului, întreaga linie astfel de coloane. În partea superioară a fiecărei coloane se introduce un lichid cu compoziția corespunzătoare, iar în partea inferioară se creează condițiile necesare pentru o vaporizare suficient de intensă, astfel încât în coloană să se producă o separare treptată a amestecului. În condiții de presiune atmosferică normală, aerul se lichefiază la o temperatură de aproximativ 80 K (-190° C); compoziţia amestecului se modifică faţă de originalul. Dacă aerul sursă conține aproximativ 79% azot și 21% oxigen, atunci, ca urmare a redistribuirii cinetice naturale, lichidul va fi 65% azot și 35% oxigen, iar gazul de deasupra lichidului va fi 87% azot și 13% oxigen. . Celelalte gaze constitutive se comportă exact în același mod, indiferent de raportul dintre oxigen și azot. De obicei, vaporii de deasupra lichidului sunt îmbogățiți în componenta punctului de fierbere inferior. Raportul dintre faze depinde, desigur, de presiune. Pe măsură ce lichidul coboară și vaporii se ridică coloană de distilare, crește concentrațiile componentelor eliberate în ele; în cele din urmă, în partea inferioară a coloanei este selectat oxigen de puritate „comercială”, în partea superioară - azot de înaltă calitate, în alte puncte - argon și un amestec de gaze „rare”. Deoarece temperatura în instalațiile de separare a aerului nu scade, de obicei, sub punctul de fierbere al azotului, neonul și heliul rămân nelichefiate și pot fi îndepărtate necondensat ca amestec cu azotul din principalul coloană de distilare. Este mai dificil să se separe amestecurile de oxigen cu argon decât amestecurile de gaze cu mare diferență la temperaturi de fierbere. În instalațiile mari de separare a aerului, procesul de condensare-evaporare este completat de un proces chimic pentru a crește randamentul de argon de înaltă puritate. La amestecul de oxigen, azot și argon luat din secțiunea criogenică a sistemului, se adaugă o cantitate măsurată de hidrogen gazos. Oxigenul reacționează cu hidrogenul în prezența unui catalizator de paladiu pentru a forma apă, care este îndepărtată în uscătoare. Amestecul gazos rămas de argon și azot este din nou răcit și trimis pentru re-rectificare. Gazele rare (heliu, neon, kripton și xenon) sunt în cele din urmă separate în instalații combinate, unde metoda condensare-evaporare este combinată cu metoda adsorbției selective. Adesea folosit ca adsorbant Cărbune activ răcit la temperatura azotului lichid.
Transport si depozitare. Oxigenul, azotul și argonul sunt transportate și stocate atât sub formă lichidă, cât și gazoasă. Pentru lichidele criogenice se folosesc vase speciale izolate termic. Gazele de joasă temperatură sunt stocate sub presiune de până la 17 MPa în cilindri de oțel. Gazele rare sunt eliberate în vase de sticla Dewar cu o capacitate de 1-2 litri; se mai folosesc termosuri din otel.
APLICAȚII INDUSTRIALE ALE GAZELOR SEPARATE
Este greu de găsit vreun tip de activitate industrială în care unul sau altul dintre gazele separate ale aerului nu joacă un rol semnificativ. Doar cele mai importante aplicații sunt notate mai jos.
Oxigen.În prelucrarea metalelor, oxigenul în combinație cu diferite gaze combustibile (acetilenă, propan, gaz natural) este utilizat pentru tăierea și sudarea oțelului cu o flacără la temperatură ridicată. Flacăra de oxi-acetilenă este utilizată pentru stripare suprafete metalice pentru îndepărtarea ruginii și a calcarului și pentru lipirea multor metale. În metalurgie, folosind oxigen într-un amestec cu gaze combustibile, curățarea la foc a oțelului nou este efectuată pentru a elimina defectele. Pentru a accelera procesele de fabricare a oțelului, oxigenul este consumat în cantități mari ca agent de decarburare și oxidare. În legătură cu utilizarea din ce în ce mai largă a sticlelor refractare, oxigenul este din ce în ce mai utilizat în tehnica de turnare a produselor din sticlă. LA rachete spațiale oxigenul este folosit ca componentă a combustibilului. Din cauza lipsei de spațiu liber în astfel de aeronave, acesta este stocat sub formă lichidă, dar înainte de a fi alimentat în motor, este transformat într-un gaz.
Vezi si RACHETA; CERCETARE ȘI UTILIZARE SPAȚIALĂ.
Azot. Datorită inerției sale relative, azotul este deosebit de potrivit pentru protecția produselor care se deteriorează (oxidează) sub influența oxigenului. În industria alimentară, atmosfera de azot este adesea folosită ca mijloc de prevenire a contactului cu oxigenul atmosferic, care poate duce la alterarea. produs alimentar sau pierderea mirosului natural. În industria chimică, a uleiului și a vopselei, o pătură cu gaz de azot este utilizată pentru a menține produsul curat și pentru a preveni incendiile și exploziile în timpul procesării. În industria electronică, azotul gazos este purjat pentru a înlocui aerul din becurile tubului vidat și carcasele semiconductoarelor înainte ca acestea să fie sigilate și sigilate. Azotul este utilizat pentru a crea o atmosferă controlată în timpul recoacerii și tratamentului termic, pentru a sufla aluminiul topit pentru a îndepărta hidrogenul dizolvat și pentru a curăța aluminiul secundar (deșeuri). În inginerie electrică, o atmosferă de azot presurizat este adesea folosită pentru a menține rezistența ridicată a izolației și pentru a crește durata de viață a materialelor izolatoare. Spațiul de expansiune din transformatoarele umplute cu ulei este de obicei umplut cu azot. Azotul lichid este utilizat pe scară largă pentru răcire atât în industrie, cât și în cercetarea științifică, în special în testele de mediu.
Vezi și AZOT.
Argon. Spre deosebire de azot, care poate reacționa cu anumite metale la temperaturi ridicate, argonul este complet inert în toate condițiile. Prin urmare, este utilizat pentru a crea o atmosferă protectoare în producerea unor metale reactive precum titanul și zirconiul. De asemenea, servește ca mediu de protecție în sudarea cu arc a metalelor și aliajelor greu de sudat - aluminiu, bronz, cupru, metal monel și oțeluri inoxidabile. Argonul este potrivit pentru umplerea lămpilor cu incandescență (cu adaos de azot). Având o conductivitate termică scăzută, argonul permite temperaturi mai ridicate ale filamentului, ceea ce mărește eficiența luminoasă a lămpii, iar greutatea sa moleculară semnificativă face dificilă evaporarea metalului dintr-un filament de tungsten fierbinte. Ca rezultat, durata de viață a lămpii este prelungită. Argonul, pur sau amestecat cu alte gaze, este de asemenea umplut cu lămpi fluorescente, atât iluminat (cu catod fierbinte), cât și reclamă (cu catod rece). În plus, este utilizat în producția de materiale semiconductoare de înaltă puritate (germaniu și siliciu) pentru fabricarea tranzistoarelor. Vezi și TRANZISTOR.
Neon, cripton și xenon. Toate aceste trei gaze au o capacitate crescută de ionizare, adică. devin conductoare electric la tensiuni mult mai mici decât majoritatea celorlalte gaze. Când sunt ionizate, aceste gaze, cum ar fi argonul și heliul, emit lumină strălucitoare, fiecare de o culoare diferită și, prin urmare, sunt utilizate în lămpi pentru iluminatul publicitar. În industria electronică, aceste gaze rare sunt folosite pentru a umple tipuri speciale de tuburi electronice - diode Zener, startere, fotocelule, tiratroni, lămpi de sterilizare cu ultraviolete și contoare Geiger. În industria nucleară, ele sunt utilizate pentru a umple camerele de ionizare și cu bule și alte dispozitive pentru studierea particulelor subatomice și măsurarea intensității radiațiilor penetrante.
Hidrogen, heliu și dioxid de carbon. Aceste gaze sunt produse în cantități mari prin alte metode care le fac mai ieftine de produs. Prin urmare, după separare în procesul de separare a aerului fracționat, acestea sunt de obicei eliberate în atmosferă. Vezi și HIDROGEN.
AER COMPRIMAT
Energia aerului comprimat poate fi utilizată pentru a efectua lucrări mecanice, pentru a crea un flux de aer sau o pernă de aer. Aerul comprimat este ușor transportat prin țevi și furtunuri, astfel încât să poată fi folosit la o distanță considerabilă de sursă (compresor sau rezervor). presiune ridicata) fără pierderi mari de energie în linia de transport.
Aplicație. Aerul comprimat este folosit la motoarele pneumatice care antrenează burghie, polizoare de mână și altele scule pneumatice, în burghie și ciocane pneumatice și în turbinele cu aer de torpile. Fluxul de aer creat de aer comprimat este folosit pentru a transporta cereale, praf de cărbune și alte materiale pulverulente prin aeroslide. Cu ajutorul aerului comprimat, minele, clădirile și alte spații închise sunt ventilate, lichidele sunt amestecate, barbotandu-le în cuve și se creează tiraj forțat în furnalele și alte cuptoare. Aerul comprimat este utilizat pentru a echilibra presiunea apei în costumele de scafandru, pentru a umfla anvelopele pneumatice, pentru a acționa frânele trenurilor și pentru a influența de la distanță dispozitivele de control al echipamentelor de proces. Sunt peste 200 în total diferite feluri aplicatii cu aer comprimat. Utilizarea energiei aerului comprimat pe scară largă a început în 1861, când M. Sommeyer a proiectat un compresor cu piston de apă, acţionat de o roată de apă. La construcția tunelului Mont Cenis din Alpi a fost furnizat aer comprimat ciocanelor de foraj. Anterior, se folosea în schimb aburul, dar aburul de evacuare crea condiții insuportabile pentru cei care lucrau în tunel. Avantajele antrenării pneumatice, în special în minerit subteran, au devenit evidente și a început dezvoltarea rapidă a tehnologiei pneumatice.
Compresoare. A fost dezvoltat un compresor cu piston pentru a furniza aer sub presiune. Pistonul dintr-un astfel de compresor este antrenat de motorul principal. În timpul cursei de aspirație, aerul este aspirat prin supapa de admisie, iar în timpul cursei de retur a pistonului, este comprimat și împins afară prin cealaltă supapă. Supapele cu clapetă cu arc funcționează fără un mecanism de control extern. Un compresor cu acțiune simplă comprimă doar o parte a pistonului, în timp ce un compresor cu acțiune dublă folosește ambele capete ale cilindrului pentru a comprima. Când aerul este comprimat, temperatura acestuia crește. O astfel de încălzire este nedorită deoarece condițiile de funcționare ale pistonului se deteriorează. În plus, dacă căldura eliberată în timpul compresiei este îndepărtată, atunci este necesară mai puțină muncă pentru compresie. Prin urmare, compresoarele sunt de obicei răcite cu apă sau aer. La presiuni de refulare peste 0,4 MPa, compresia se realizează în trepte. Doi sau mai mulți cilindri sunt conectați în așa fel încât aerul de la ieșirea unei trepte să intre în admisia altuia, iar presiunea de descărcare completă să fie atinsă numai la ieșirea ultimului. Între etape sunt prevăzute schimbătoare de căldură care scad temperatura aerului. Compresoarele cu șase trepte de acest tip sunt capabile să furnizeze aer comprimat la presiuni de până la 100 MPa. Compresoarele rotative volumetrice sunt de două tipuri - lamelare și cu rotor dublu. Compresorul cu palete este proiectat în același mod ca și motorul cu aer cu palete (vezi mai jos), doar rotorul se rotește în sens opus. Într-un compresor cu dublu rotor, aerul este prins în spațiul dintre rotoare și peretele carcasei și este forțat să iasă de ochiurile rotoarelor. Suflantele și compresoarele centrifuge sunt mașini de tip rotativ similar pompelor centrifuge. Energia aerului este crescută prin acțiunea centrifugă a rotoarelor rotative. Suflantele sunt numite mașini care comprimă aerul la o presiune de cel mult 0,3 MPa (g), iar compresoare - la presiuni care depășesc această valoare. Pentru a crește presiunea, ambele sunt realizate în mai multe etape. Mai multe rotoare sunt amplasate pe un arbore, iar aerul, care trece de la o treaptă la alta, este comprimat secvenţial.
Motoare pneumatice. Un motor pneumatic este o mașină care transformă munca mecanica energia aerului comprimat. Pneumomotoarele sunt cu piston, rotative lamelare și turbină. Aerul este comprimat în afara motorului, de exemplu într-un compresor.

Motoare pneumatice cu piston. Un motor cu piston cu aer este similar cu un motor cu abur. Aerul comprimat intră în cutia supapelor, iar supapa, atunci când este activată, lasă aer să intre în cilindru. Sub presiunea aerului, pistonul efectuează o muncă utilă printr-o manivela sau alt mecanism, după care aerul evacuat este eliberat în atmosferă. Pneumociclul poate fi fără expansiune și cu expansiune.
Motoare cu aer rotativ lamelar. Rotorul unui astfel de motor este decalat față de linia centrală a corpului fix. Plăcile dreptunghiulare (sau paletele) instalate în fantele radiale ale rotorului sunt presate pe peretele interior al carcasei. Aerul comprimat intră în corpul cilindric printr-un orificiu din perete și umple „camera” formată de peretele rotorului, peretele corpului și una dintre plăci. Sub presiunea aerului, placa se rotește împreună cu rotorul, iar placa următoare, trecând pe lângă gaură, întrerupe fluxul de aer în această cameră și îi dă acces la următoarea. Aerul prins se extinde, eliberând o parte din energia sa, până când se atinge volumul complet al camerei. După aceea, ieșirea se deschide și o parte din aerul evacuat iese.
Motoare cu turbine cu aer.Într-o turbină cu aer, energia de presiune a aerului comprimat este convertită în energia cinetică a mișcării sale direcționate atunci când aerul se extinde în duze. Un jet de aer de mare viteză lovește paletele rotorului, acționează asupra acestuia cu o forță tangenţială și îl face să se rotească (turbinele cu aer sunt similare cu turbinele cu abur).
Aerul este necesar pentru toate organismele vii: animale pentru respirație și plante pentru hrană. În plus, aerul protejează Pământul de distrugeri radiații ultraviolete Soare. Principalii constituenți ai aerului sunt azotul și oxigenul. În aer există, de asemenea, impurități mici de gaze nobile, dioxid de carbon și o anumită cantitate de particule solide - funingine, praf. Toate animalele au nevoie de aer pentru a respira. Aproximativ 21% din aer este oxigen. O moleculă de oxigen (O 2) este formată din doi oxigeni legați.
Compoziția aerului
Procentul diferitelor gaze din aer variază ușor în funcție de loc, perioada anului și zi. Azotul și oxigenul sunt componentele principale ale aerului. Un procent din aer este format din gaze nobile, dioxid de carbon, vapori de apă și poluanți precum dioxidul de azot. Gazele din aer pot fi separate prin distilație fracțională. Aerul este răcit până când gazele devin lichide (vezi articolul „”). După aceea, amestecul lichid este încălzit. fiecare lichid are propriul punct de fierbere, iar gazele formate în timpul fierberii pot fi colectate separat. Oxigenul, azotul și dioxidul de carbon intră constant din aer în aer și revin în aer, de exemplu. are loc un ciclu. Animalele inspiră oxigen și expiră dioxid de carbon.
Oxigen
Azot
Mai mult de 78% din aer este azot. Proteinele din care sunt construite organismele vii conțin și azot. Lucrul principal aplicație industrială azot - producția de amoniac necesare pentru îngrășământ. Azotul pentru aceasta este combinat cu. Azotul este pompat în ambalaje pentru carne sau pește, deoarece. atunci când sunt expuse la aerul obișnuit, produsele se oxidează și se deteriorează.Organele umane destinate transplantului sunt depozitate în azot lichid deoarece este rece și inert chimic. Molecula de azot (N2) este formată din doi atomi de azot legați.
gaze nobile
Gazele nobile sunt 6 din a 8-a grupă. Sunt extrem de inerți din punct de vedere chimic. Numai ei există sub formă de atomi individuali care nu formează molecule. Din cauza pasivității lor, lămpile sunt umplute cu unele dintre ele. Xenonul practic nu este folosit de oameni, dar argonul este pompat în becuri, iar lămpile fluorescente sunt umplute cu cripton. Neonul luminează intermitent roșu-portocaliu atunci când trece o descărcare electrică. Este folosit la lămpile stradale cu sodiu și lămpile cu neon. Radonul este radioactiv. Se formează ca urmare a degradarii metalului radiu. Niciun compus de heliu nu este cunoscut de știință, iar heliul este considerat absolut inert. Densitatea sa este de 7 ori mai mică decât densitatea aerului, așa că dirijabilele sunt pline cu el. Umplut cu heliu baloane dotat cu aparatură științifică și lansat în atmosfera superioară.
Efect de sera
 Acesta este numele creșterii observate în prezent a conținutului de dioxid de carbon din atmosferă și rezultatul încălzire globală
, adică o creștere a temperaturilor medii anuale în întreaga lume. Dioxidul de carbon împiedică căldura să părăsească Pământul, la fel cum sticla păstrează căldura în interiorul unei sere. Pe măsură ce există din ce în ce mai mult dioxid de carbon în aer, din ce în ce mai multă căldură este prinsă în atmosferă. Chiar și o încălzire ușoară provoacă creșterea nivelului Oceanului Mondial, modificarea vântului și topirea unor gheață în apropierea polilor. Oamenii de știință cred că, dacă conținutul de dioxid de carbon continuă să crească la fel de rapid, atunci în 50 de ani temperatura medie ar putea crește cu 1,5 °C până la 4 °C.
Acesta este numele creșterii observate în prezent a conținutului de dioxid de carbon din atmosferă și rezultatul încălzire globală
, adică o creștere a temperaturilor medii anuale în întreaga lume. Dioxidul de carbon împiedică căldura să părăsească Pământul, la fel cum sticla păstrează căldura în interiorul unei sere. Pe măsură ce există din ce în ce mai mult dioxid de carbon în aer, din ce în ce mai multă căldură este prinsă în atmosferă. Chiar și o încălzire ușoară provoacă creșterea nivelului Oceanului Mondial, modificarea vântului și topirea unor gheață în apropierea polilor. Oamenii de știință cred că, dacă conținutul de dioxid de carbon continuă să crească la fel de rapid, atunci în 50 de ani temperatura medie ar putea crește cu 1,5 °C până la 4 °C.
Aerul este cea mai importantă substanță, fără acces la care o persoană nu va trăi nici măcar câteva minute. Înțelegem cu toții cât de important este aerul pentru noi, dar știm ce este?
Din păcate, cunoștințele celor mai mulți dintre noi în această problemă sunt foarte limitate. Să reparăm situația.
aer într-un mod științific
Strict vorbind, aerul este amestecul natural de gaze care formează atmosfera pământului. Componenta principală a aerului care o determină rol esentialîn viața organismelor vii, este oxigenul. Oxigenul este folosit în procesele oxidative, în urma cărora se eliberează energia necesară vieții.
Compoziția chimică a aerului
Omul de știință scoțian Joseph Black în 1754, printr-o serie de experimente, a demonstrat că aerul nu este o substanță omogenă, ci un amestec de gaze. Compoziția chimică a aerului a fost determinată de omul de știință francez Antoine Lavoisier. Și din aceasta constă învelișul nostru pământesc:
- azot - 78%;
- oxigen - 21%;
- alte gaze (dioxid de carbon, argon, neon, metan, heliu, krypton, hidrogen, xenon) - 1%.
Apropo, aerul nu a fost întotdeauna așa - acum 4 miliarde de ani, în zorii nașterii planetei noastre, aerul era în principal dioxid de carbon. Inutil să spun că viața pur și simplu nu s-ar putea dezvolta în astfel de condiții. Treptat, dioxidul de carbon a intrat în diferite reacții (dizolvat în apă, a reacționat cu roci), iar conținutul său în aer a scăzut.
Când au apărut plantele verzi, care, după cum știți, absorb activ dioxidul de carbon și îl folosesc în procesele lor de viață, conținutul său în atmosferă a început să scadă mult mai repede, până când în cele din urmă s-a format compoziția finală.
Pentru dreptate, trebuie menționat că această compoziție foarte finală de 78% / 21% / 1% variază în funcție de loc: în păduri se respectă compoziția minimă a impurităților, iar în orașele mari, dimpotrivă, cea maximă. . În plus, în părți diferite conținutul de lumină al unui anumit gaz poate varia cu 3% pentru fiecare.
Proprietăți fizice
Principalele proprietăți fizice ale aerului includ temperatura, umiditatea și presiunea atmosferică. Fiecare dintre aceste proprietăți afectează într-un mod special starea mediului și a omului.
Temperatura aerului
Temperatura aerului determină starea termică Mediul extern adică transferul de căldură. Temperaturile ridicate și scăzute afectează negativ transferul de căldură.
La temperaturi ridicate (mai mult de 35 de grade Celsius), organismul scapă de excesul de căldură, în principal prin transpirație. Împreună cu transpirația, sărurile și vitaminele solubile în apă sunt excretate din organism, ceea ce duce la o mulțime de efecte negative, în special, la creșterea vâscozității sângelui, probleme cardiace etc. Supraîncălzirea excesivă a corpului poate duce la insolație.
La temperaturi scăzute, organismul suferă un deficit de căldură. Răcirea generală este însoțită de o slăbire a activității musculare, răcirea locală contribuie la dezvoltarea răcelilor.
Umiditatea aerului
Umiditatea caracterizează conținutul de vapori de apă din aer. Aerul excesiv de uscat afectează negativ membrana mucoasă a tractului respirator superior, provocând inflamații și fisuri.
Presiunea atmosferică
O modificare a presiunii atmosferice este deosebit de acută la vârsta adultă, iar schimbările bruște ale presiunii provoacă consecințe negative asupra unui corp tânăr.
Reducerea presiunii atmosferice duce la hipoxie (foamete de oxigen), care, la rândul său, provoacă dureri de cap, coordonare afectată a mișcărilor, somnolență etc.
Printre consecințele negative ale presiunii atmosferice ridicate se numără creșterea ritmului cardiac, respirația, creșterea tensiunii arteriale maxime și scăderea minimă etc.
Rezultat important
După cum puteți vedea, aerul și dacă este uscat sau umed, cald sau rece joacă un rol crucial. Astfel, aerul nu este necesar doar pentru activitatea vitală a organismelor vii, el determină și calitatea acestei activități foarte vitale.
Citiți mai multe despre cea mai importantă substanță pentru noi în articole.
Acea parte a atmosferei, care este adiacentă Pământului și pe care, în consecință, o persoană respiră, se numește troposferă. Troposfera are o înălțime de nouă până la unsprezece kilometri și este un amestec mecanic de diferite gaze.
Compoziția aerului nu este constantă. Depinzând de locație geografică, terenul, condițiile meteo, aerul pot avea o compoziție diferită și proprietăți diverse. Aerul poate fi gazat sau evacuat, proaspăt sau greu - toate acestea înseamnă că conține anumite impurități.
Azot - 78,9 la sută;
Oxigen - 20,95 la sută;
Dioxid de carbon - 0,3 la sută.
În plus, în atmosferă sunt prezente și alte gaze (heliu, argon, neon, xenon, cripton, hidrogen, radon, ozon), precum și suma lor este puțin mai mică de unu la sută.
De asemenea, merită subliniată prezența în aer a unor impurități permanente de origine naturală, în special a unor produse gazoase care se formează în urma proceselor atât biologice, cât și chimice. Amoniacul merită o mențiune specială printre ele (compoziția aerului departe de zonele populate include aproximativ trei până la cinci miimi de miligram pe metru cub), metan (nivelul său este în medie de două zece miimi de miligram pe metru cub), oxizi de azot ( în atmosferă concentrația lor ajunge la aproximativ cincisprezece miimi de miligram pe metru cub), hidrogen sulfurat și alți produși gazoși.
Pe lângă vapori și impurități gazoase, compoziția chimică a aerului include de obicei praf de origine cosmică, care cade pe suprafața Pământului în cantitate de șapte sute de miimi de tonă pe kilometru pătrat în timpul anului, precum și particule de praf care provin din erupții vulcanice.
Cu toate acestea, în cea mai mare măsură (și nu în bine) compoziția aerului și poluează troposfera este așa-numita sol (vegetal, sol) praf și fum de la incendiile forestiere. Mai ales o mulțime de astfel de praf în masele de aer continentale originare din deșerturile din Asia Centrală și Africa. De aceea putem spune cu încredere că un mediu de aer ideal curat pur și simplu nu există și este un concept care există doar teoretic.
Compoziția aerului tinde să se schimbe constant, iar schimbările sale naturale joacă de obicei un rol destul de mic, mai ales în comparație cu consecinte posibileîncălcările sale artificiale. Aceste tulburări sunt în principal legate de activitati de productie umanitate, utilizarea dispozitivelor pentru serviciile consumatorilor, precum și vehicule. Aceste încălcări pot duce, printre altele, la denaturarea aerului, adică la diferențe pronunțate în compoziția și proprietățile acestuia față de indicatorii corespunzători ai atmosferei.
Acestea și multe alte tipuri de activitate umană au dus la faptul că compoziția de bază a aerului a început să sufere modificări lente și nesemnificative, dar totuși absolut ireversibile. De exemplu, oamenii de știință au calculat că aproximativ aceeași cantitate de oxigen a fost folosită de omenire în ultimii cincizeci de ani ca în milioane de ani anteriori, iar în procent- două zecimi de procent din rezerva sa totală în atmosferă. În același timp, eliberarea în aer crește în mod corespunzător.Această eliberare, conform ultimelor date, a ajuns la aproape patru sute de miliarde de tone în ultimele sute de ani.
Astfel, compoziția aerului se schimbă în rău și este greu de imaginat ce va deveni în câteva decenii.