Основные типы кристаллических структур. Значение знаний о кристаллическом строении металлов
Читайте также
В зависимости от вида структурных единиц вещества различают каркасные (атомные), металлические, ионные и молекулярные структуры. Встречаются и комбинированные типы структур.
В каркасной структуре атомы одного или нескольких химических элементов связаны ковалентными химическими связями. Вследствие этого выбор определенной структуры диктуется направленностью связей. В структуре отсутствуют изолированные группы атомов, т.е. сетка ковалентных связей охватывает всю структуру. Наиболее известным примером вещества с каркасной структурой является алмаз. Элементарная ячейка алмаза представлена на рис. 8.7. Атомы углерода расположены в вершинах кубической ячейки, центрах всех граней и в шахматном порядке занимают центры четырех из восьми кубиков, на которые можно разбить элементарную ячейку. От этих атомов внутри ячейки ковалентные связи тетраэ- дрически направлены к атому углерода в одной из вершин и трем атомам углерода на гранях. Расстояния между всеми атомами углерода 154 пм. Алмазоподобные структуры имеют многие вещества. Среди них кремний, карбид кремния SiC, сульфид цинка (цинковая обманка) ZnS. В этом веществе атомы цинка находятся в вершинах и на гранях элементарной ячейки, а атомы серы занимают места внутри ячейки. Таким образом, структура этого вещества, по традиции причисляемого к солям, не ионная, а каркасная.
Кристалл вещества с каркасной структурой может рассматриваться как единая молекула. Такие вещества проявляют термическую устойчивость, практически не растворимы в воде, имеют высокие температуры плавления и твердость.
Металлическая структура отличается от каркасной тем, что расположение атомов определяется не направленностью связей, а только условием плотнейшей упаковки атомных сфер. Для большинства металлов характерны лишь три разновидности элементарных ячеек - объемно-центрированная кубическая, гранецентрированная кубическая и гексагональная компактная. Многие металлы проявляют полиморфизм , изменяя кристаллическую структуру при нагревании.
Рис. 8.7.
в виде клиньев показаны связи между атомами углерода внутри ячейки
Ионная структура строится из чередующихся ионов с противоположными по знаку зарядами. Такого типа структуру имеет хлорид натрия (см. рис. 2.8). Положения ионов натрия и хлора полностью взаимозаменяемы. В вершинах ячейки и центрах граней можно поместить ионы хлора. Тогда ионы натрия окажутся на серединах ребер и в центре ячейки. Можно поступить наоборот, т.е. все ионы поменять местами. Такую структуру можно представить как две гранецентрированные решетки - одна с ионами Na + и другая с ионами С1~, - вставленные одна в другую со смещением на половину длины ребра куба.
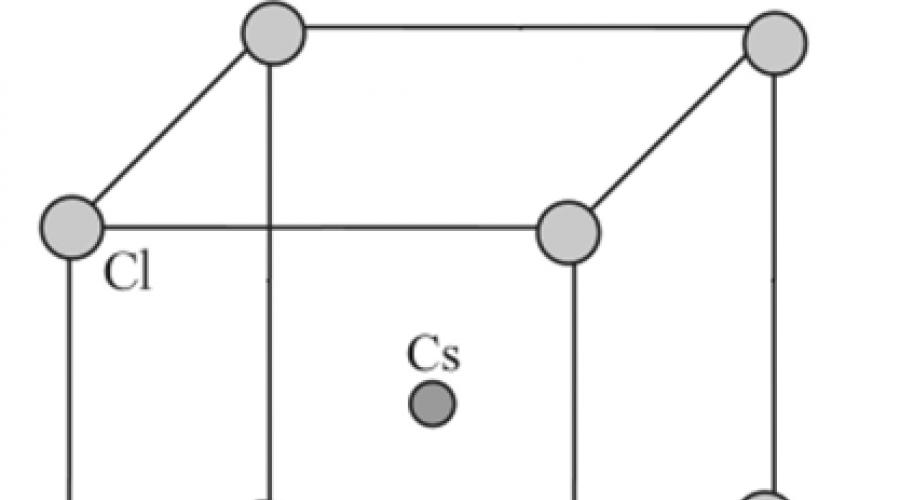
Возникновение той или иной ионной структуры зависит главным образом от зарядов ионов и соотношения их радиусов. В хлориде цезия, более тяжелого щелочного металла, чем натрий, значительно увеличен радиус катиона, вследствие чего его координационное число повышается до восьми. В кубической ячейке каждый ион цезия окружен восемью ионами хлора (рис. 8.8). Эту структуру тоже можно представить как две кубические решетки, образованные ионами цезия и ионами хлора, вставленные одна в другую так, что ион одного вида оказывается в центре ячейки с ионами другого вида.

Рис. 8.8.
Вещества с ионной структурой характеризуются высокими температурами плавления вследствие значительной энергии электростатического притяжения ионов. Многие ионные вещества хорошо растворимы в воде.
Вещества с молекулярными структурами резко отличаются от рассмотренных выше низкими температурами плавления. Именно среди них имеются жидкости и газы. При рентгеноструктурном исследовании таких веществ обнаруживаются короткие межатомные расстояния внутри молекул и значительно удлиненные расстояния между такими же атомами в разных молекулах. Например, в кристаллах иода 1 2 (рис. 8.9) расстояние между атомами в молекуле - 272 пм, расстояние между молекулами в слое - 350 нм, а ближайшее расстояние между атомами, находящимися в разных слоях, - 397 пм.

Рис . 8.9.
Вещества, состоящие из многоатомных молекул, образуют весьма сложные структуры. Без рентгеновского исследования понять их строение было бы просто невозможно. Можно напомнить о молекулах ДНК, имеющих двойную спиральную структуру. Определение их структуры открыло новый этап в развитии биологии.
Очевидно, что молекула не может находиться в узле кристаллической структуры, так как представляет собой некоторую совокупность атомов. На рис. 8.10 в качестве примера приведена структура комплексного соединения |Pt(CN) 2 (NH 3)(NH 2 CH 3)|. Элементарная ячейка представлена в виде проекции вдоль оси У. Вершины ячейки не заняты атомами. Плоские молекулы комплексного соединения на проекции видны сбоку. Пунктиром показаны водородные связи между молекулами аммиака, находящимися в разных молекулах комплексного соединения. Оси симметрии второго порядка проходят параллельно оси У. Одна из них проходит через центр ячейки. Восемь молекул, находящихся в элементарной ячейке, располагаются на двух уровнях по оси У в шахматном порядке. Этот пример дает представление о сложности молекулярных структур.

Рис. 8.10. Проекция элементарной ячейки комплексного соединения вдоль оси Y
1.4. Основные типы кристаллических структур
Точечное расположение атомов в пространственных решетках является упрощенным и непригодным для изучения кристаллических структур, когда определяется расстояние между ближайшими атомами или ионами. Однако физические свойства кристаллических структур зависят от химической природы веществ, размеров атомов (ионов) и сил взаимодействия между ними. Поэтому в дальнейшем будем считать, что атомы или ионы имеют форму шара и характеризуются эффективным радиусом , понимая под ним радиус сферы их влияния, равный половине расстояния между двумя ближайшими соседними однотипными атомами или ионами. В кубической решетке эффективный атомный радиус равен а 0 /2.
Эффективный радиус имеет различные собственные значения в каждой определенной структуре и зависит от природы и числа соседних атомов. Атомные радиусы разных элементов можно сравнивать только тогда, когда они образуют кристаллы с одинаковым координационным числом. Координационным числом z данного атома (иона) называют число окружающих его ближайших однотипных атомов (ионов) в кристаллической структуре. Мысленно соединив прямыми линиями центры соседних частиц друг с другом, получим
координационный многогранник ; при этом атом (ион), для которого строится такой многогранник, находится в его центре.
Координационное число и отношение эффективных радиусов частиц определенным образом связаны друг с другом: чем меньше различие в размерах частиц, тем больше z .
В зависимости от кристаллической структуры (типа решетки), z может изменяться от 3 до 12. Как будет показано ниже, в структуре алмаза z = 4, в каменной соли z = 6 (каждый ион натрия окружен шестью ионами хлора). Для металлов характерно координационное число z = 12, для кристаллических полупроводников z = 4 или z = 6. Для жидкостей координационное число определяется статистически как среднее число ближайших соседей любого атома.
Координационное число связано с плотностью упаковки атомов в кристаллической структуре. Относительная плотность упаковки –
это отношение объема, занимаемого атомами, к общему объему структуры. Чем больше координационное число, тем выше относительная плотность упаковки.

Раздел 1. Основныеположен ия физико химическо й кристаллографии
Кристаллическая решетка стреми тся обладать минимумом свободной энергии. Это возмож но только в том случае, когда каждая частица будет взаимодействовать с максимально возм ожным числом других частиц. Иначе говоря, координационное число должно быть максимальны м. Стремление к плотней шей упаковке свойственно всем типам кристаллических структур.
Рассмотрим плоскую структуру, состоя щую из атомов одной природы, которые касаются друг друга и заполняют бóльшую часть пространства. В этом случае возможе н только один способ плотнейшей упаковки атомов, прилегающих друг к другу: вокруг центрально-
центры тяжести приходятся н а пустоты первого слоя. Это хорошо видно на правом изображении на рис. 1.10, а (вид сверху), где проекции атомов второго слоя окрашены в бледно-серый цвет. Атомы второго слоя образуют базисный треугольник (показан сплошной линией) с вершиной, направленной вверх.
Рис. 1.10. Последовательность слоев при упаковке шаров одина кового размера в структурах двух типов: a – АВАВ... при гексагональной плотнейшей упаковке (ГПУ); б – АВСАВС... пр и кубической плотнейшей у паковке (К ПУ), дающей гранецентрированную кубическую (ГЦК) решетку. Для нагляд ности третий и четверт ый слои показаны не полностью заполн енными

Глава 1. Элементы кристаллофизики
Атомы третьего слоя могут располагаться двумя способами. Если центры тяжести атомов третьего слоя находятся над центрами тяжести атомов первого слоя, то повторится укладка первого слоя (рис. 1.10, а ). Результирующая структура представляет собой гексагональную плотнейшую упаковку (ГПУ). Ее можно представить в виде последовательности слоев АВАВАВАВ … в направлении оси Z .
Если атомы третьего слоя C (показаны темно-серым цветом справа на рис. 1.10, б ) расположены над другими пустотами первого слоя и образуют базисный треугольник, развернутый относительно слоя B на 180º (показан пунктиром), а четвертый слой идентичен первому, то результирующая структура представляет собой кубическую плотнейшую упаковку (КПУ), которая соответствует гранецентрированной кубической структуре (ГЦК) с последовательностью слоев АВСАВСАВСАВС … в направлении оси Z .
Для плотнейших упаковок z = 12. Это хорошо видно на примере центрального шара в слое В : его ближайшее окружение составляют шесть шаров слоя А и по три шара ниже и выше его в слоях В
(рис. 1.10, a ).
Кроме координационного числа z различные структуры характеризуются также плотностью упаковки, вводимой как отношение объема V ат , занимаемого атомами, к объему всей ячейки Браве V яч . Атомы представляются твердыми шарами радиусом r , поэтому V ат = n (4π/3)r 3 , где n – число атомов в ячейке.
Объем кубической ячейки V яч = a 0 3 , где а 0 – период решетки. Для ячейки ГПУ с площадью шестиугольного основания S = 3a 0 2 2 3
и высотой c = 2a 0 23 получаем V яч = 3a 0 3 2 .
Соответствующие параметры кристаллических структур – примитивной кубической (ПК), объемно-центрированной кубической (ОЦК), гранецентрированной кубической (ГЦК), гексагональной плотноупакованной (ГПУ) – приведены в табл. 1.2. Радиусы атомов записаны с учетом того, что они соприкасаются вдоль ребер куба в ПК-структуре (2r = а 0 ), вдоль пространственных диагоналей (4r = a 0 3) в ОЦК-структуре и вдоль диагоналей граней (4r = a 0 2)
в ГЦК-структуре.
Таким образом, в структурах с плотнейшей упаковкой (ГЦК и ГПУ), имеющих z = 12, объем ячейки на 74 % занят атомами. C уменьшением координационного числа до 8 и 6 плотность упаковки снижается соответственно до 68 (ОЦК) и 52 % (ПК).

Таблица 1.2
Параметры кубических и гексагональных кристаллов
Параметры кристалла |
|||||
Координационное число z |
|||||
Число атомов n в ячейке |
|||||
Радиус атома r |
а 0 /2 |
a 2 4 |
а 0 /2 |
||
Объем одного атома, V ат /n |
|||||
a 0 3 π 6 |
a3 π |
a 3 π 2 24 |
π a 0 3 6 |
||
Плотность упаковки, |
|||||
π 3 8 = 0, 6 |
π 2 6 = 0,74 |
π 2 6 = 0,74 |
|||
V ат/ V яч |
|||||
Уже отмечалось, что при кристаллизации вещества система стремится обеспечить минимум свободной энергии. Одним из факторов, снижающих потенциальную энергию взаимодействия между частицами, является их максимальное сближение и установление взаимной связи с возможно бóльшим числом частиц, т. е. стремление к более плотной упаковке с наибольшим координационным числом.
Тенденция к реализации плотнейшей упаковки свойственна всем типам структур, но сильнее всего она выражена в металлических, ионных и молекулярных кристаллах. В них связи ненаправленные или слабонаправленные (см. гл. 2), так что для атомов, ионов
и молекул вполне приемлемой является модель твердых несжимаемых шаров.
Трансляционными решетками Браве, приведенными на рис. 1.3
и в табл. 1.1, не исчерпываются все возможные варианты построения кристаллических структур, в первую очередь для химических соединений. Дело в том, что периодическое повторение ячейки Браве дает трансляционную решетку, состоящую только из частиц (молекул, атомов, ионов) одного сорта. Поэтому структуру сложного соединения можно построить комбинацией решеток Браве, определенным образом вставленных одна в другую. Так, полупроводниковые кристаллы используют направленную ковалентную (неполярную или полярную) связь, которая обычно реализуется путем комбинации, по крайней мере, двух решеток, по отдельности достаточно плотно упакованных, но в итоге обеспечивающих малые координационные числа «суммарной» решетки (вплоть до z = 4).
Существуют группы веществ, характеризующиеся идентичным пространственным расположением атомов и отличающиеся друг от друга только параметрами (но не типом) кристаллической решетки.

Поэтому их структуру можно описать с помощ ью одной пространственной модели (одним структурным типом ) с указанием конкретных значений параметров решетки для каждого вещ ества. Таким образом, кристаллы различных вещес тв относятся к ограниченному числу структурных типов.
Наиболее часто встречаются следующие типы структур:
в металлических кристаллах :
структура вольфрама (ОЦ К-решетка); структура меди (ГЦК-ре шетка), структура магния (ГПУ-решетка);
в диэлектрических кристаллах :
структура хлористого натрия (сдвоенная Г ЦК-решетка); структура хлористого цезия (сдвоенная ПК-решетка);
в полупроводни ковых кристаллах:
структура алмаза (сдвоенная ГЦК-решетка); структура сфалер ита (сдвоенная Г ЦК-решетка); структура вюрцита (сдвоенная ГП У-решетка).
Рассмотрим кратко особенности и реализуемость перечисленных выше структур и соответствующие им решетки Браве.
1.4.1. Метал лические кристаллы
Структура вольфрама (рис. 1.1 1, а ). Объемно-центрированная кубическая решетка не является структурой с плотнейш ей упаковкой, имеет относительную плотность упаковки 0,6 8 и координационное число z = 8. Наиболее плотно упакованы плоско сти {11 1}.
Рис. 1.11. Типы кубических решеток: а – объемно-центрированная кубиче ская (ОЦК); б – простая куб ическая

Раздел 1. Основные положения физико химической кристаллографии
Помимо вольфрама W, ОЦК-решетку имеют все щелочные и щелочно-земельные металлы, а также большинство тугоплавких металлов: хром Cr, железо Fe, молибден Mo, цирконий Zr, тантал Ta, ниобий Nb и др. Последнее находит следующее объяснение. В ячейке ОЦК для центрального атома ближайшими соседями являются атомы в вершинах куба (z = 8). Они отстоят друг от друга на расстоянии
шесть центральных атомов в соседних ячейках (вторая координационная сфера), что практически увеличивает координационное число до z 14. Это дает суммарный выигрыш энергии, компенсирующий отрицательный вклад от небольшого увеличения средних расстояний между атомами по сравнению с ГЦК-решеткой, где атомы находятся на расстоянии d = a 0 ( 2) 2 = 0,707a 0 . В результате повышается проч-
ность кристаллов, проявляющаяся в их высокой температуре плавления, достигающей для вольфрама 3 422 ºС. Для сравнения: простая кубическая структура (рис. 1.11, б ) с z = 8 имеет неплотную упаковку и встречается только у полония Ро.
Структура меди (ГЦК-решетка), показанная на рис. 1.12, а , относится к плотноупакованным структурам, имеет относительную плотность упаковки 0,74 и координационное число z = 12. Кроме меди Cu она характерна для многих металлов, таких как золото Au, серебро Ag, платина Pt, никель Ni, алюминий Al, свинец Pb, палладий Pd, торий Th и др.
Рис. 1.12. Структуры плотноупакованных кристаллических решеток: а – гранецентрированная кубическая (структура меди); б – гексагональная плотноупакованная (структура магния)

Глава 1.Элементы кристаллофизики
Перечисленные металлы сравнительно мягкие и пластичные. Дело в том, что в структурах типа меди тетраэдрические и октаэдрические пустоты в ГЦК-решетке не заполнены другими частицами. Это допускает, в силу ненаправленности связей между атомами, их смещение по так называемым плоскостя м скольж ения . В решетке ГЦК таковыми являются плоскости наибольшей упаковки {111}, одна из которых изображена заштрихованной на рис. 1.12, а .
Структура магния (ГПУ-решетка), показанная на рис. 1.12, б , характерна не только для магния Mg, но и для кадмия Cd, цинка Zn, титана Ti, таллия Tl, бериллия Be и др., а также для большинства редкоземельных элементов. В отличие от ПК-решетки, ГПУ-решетка на рис. 1 .12, б имеет слой В (заштрихованный), расположенный посередине между базисными слоями А на фиксированном расстоянии
с 2 = a 0 2 3 (с наблюдаемым отклонением вплоть до 10 % для неко-
торых металлов). Атомы в слоях В размещаются над центрами треугольников в базисной плоскости (0001) с плотнейшей упаковкой.
1.4.2. Диэлектрические кристаллы
Структура хлористого натрия (рис. 1.13, а ) может быть опи-
сана как две гранецентрированные кубические решетки (структурный тип меди), сдвинутые на полпериода решетки (a 0 /2) вдоль любого из ребер <100>.
Крупные анионы хлора Cl− занимают узлы ГЦК-ячейки и образуют кубическую плотнейшую упаковку, в которой катионы натрия Na+ , имея меньший размер, заполняют только октаэдрические пустоты. Иными словами, в структуре NaCl каждый катион окружен четырьмя анионами в плоскости (100) и двумя ионами в перпендикулярной плоскости, которые находятся на равном расстоянии от катиона. В результате имеет место октаэдрическая координация. Это в равной степени справедливо и для анионов. Поэтому отношение координационных чисел подрешеток равно 6:6.
Структура хлористого цезия CsCl (сдвоенная ПК-решетка),
показанная на рис. 1.13, б , состоит из двух примитивных кубических решеток, сдвинутых на половину объемной диагонали. Дело в том, что ионы цезия больше ионов натрия и не могут поместиться в октаэдрических (и тем более в тетраэдрических) пустотах решетки хлора, если бы она была типа ГЦК, как в структуре NaCl. В структуре CsCl каждый ион цезия окружен восемью ионами хлора и наоборот.
В структуры этого типа кристаллизуются и другие галогениды, например Cs (Br, I), Rb (Br, I), Tl (Br, Cl), полупроводниковые соединения типа AIV BVI и многие сплавы редкоземельных элементов. Подобные структуры наблюдаются и в гетерополярных ионных соединениях.
1.4.3. Полупроводниковые кристаллы
Структура алмаза представляет собой сочетание двух ГЦКрешеток, вставленных одна в другую и сдвинутых по пространственной диагонали на четверть длины (рис. 1.14, а ). Каждый атом окружен четырьмя, которые расположены в вершинах тетраэдра (жирные линии на рис. 1.14, а ). Все связи в структуре алмаза равноправны, направлены по <111> и составляют друг с другом углы 109º 28" . Решетка алмаза относится к неплотноупакованным структурам с координационным числом z = 4. В структуре алмаза кристаллизуются германий, кремний, серое олово. Кроме алмаза в структуре этого типа кристаллизуются также элементарные полупроводники – кремний Si, германий Ge, серое олово Sn.
Структура сфалерита (сдвоенная ГЦК-решетка). Если две вспомогательные гранецентрированные кубические решетки образованы разными атомами, то возникает новая структура, называемая структурой сфалерита ZnS или цинковой обманки (рис. 1.14, б ).

Глава 1.Элем енты кристаллофизи ки
Рис. 1 .14. Структуры алм аза (а ), с фалерита (б ), вюрцита (в ). Жирными линиями выделены т етраэдрические связи
Такой структурой обладают многие полупроводниковые соединения типа AIII BV (арсенид галлия GaA s, фосфид галлия GaP, фосфид индия InP, антимонид индия I nSb и др.) и типа AII BVI (селенид цинка ZnSe, теллури д цинка ZnTe, сульфид кадмия CdS, селенид кадмия
Структура сфалерита идентична структуре алмаза с тетраэдрическим окружением атомов (рис. 1.14, а ), только одна ГЦКподрешетка занята ат омами галлия Ga, а другая – атомами мышьяка As. В ячейке GaAs отсутствует центр симметрии, т. е. структура полярна по четырем направления м < 111 > . Наблюдается различие между плотноупак ованными плоскостями 111) и (111 ): если одна из них содержит ато мы Ga, то другая – атомы As. Это обусловливает анизотропию свойств поверхности (микротвердость, адсорбция, химическое травление и т. п.).
В структуре сфалерита треугольные основания тетраэдров любого слоя ориентированы так же, как и основания тетраэдров предыдущего слоя.
Структура вюрцита (с двоенная ГПУ-решетка), изображ енная на рис. 1.14, в , характерна для гексагональной модификации сульфида цинка. Такой структурой обладают бл изкие к ZnS полупроводники, например сульфид кадмия CdS и селенид кадмия CdSe. Для большинства соедине ний AII B VI хара ктерен ф азовый переход «сфалерит – вюрцит». Структура вюрцита реализуется, если атом неметалла имеет малые размеры и большую электроотр ицательность.
На рис. 1.14, в приведена примитивная ячейка вюрцита для ZnS в форме прямой призм ы с ромбом в основании и углом 120° в центре шестиугольника, образованного тремя такими призмами (две из которых показаны на рису нке).
Рис. 17. Снежинки-скелетные кристаллы льда
Из опыта известно, что в кристаллическом веществе физические свойства одинаковы в параллельных направлениях, а представление о строении веществ требует, чтобы слагающие кристалл частицы (молекулы, атомы или ионы) находились одна от другой на некоторых конечных расстояниях. Исходя из этих предположений, возможно построить геометрическую схему строения кристаллического . Для этого положение каждой слагающей частицы можно отметить точкой. Вся кристаллическая постройка представится тогда системою точек, закономерно расположенных в пространстве, причем для любых параллельных направлений расстояния между точками будут одинаковыми. Такое правильное расположение точек в пространстве называют
пространственной решеткой, а если каждая точка представляет положение атома, иона или молекулы в кристалле - кристаллической решеткой.
Построение пространственной решетки можно себе представить следующим образом.
А 0 (рис. 18) обозначает центр атома или иона. Пусть ближайший к ней такой же центр обозначается точкой Ль тогда, на основании однородности кристаллического , на расстоянии А 1 А 2 = А 0 А 1 должен находиться центр А 2 ; продолжая это рассуждение далее, можно получить ряд точек: А 0 , А 1 , А 2 , А 3 …
Положим, что ближайшая точка к А 0 в другом направлении будетR 0 , тогда должна существовать частица S 0 на расстоянии R 0 S 0 = Л 0 R 0 и т. д., т. е. получится другой ряд одинаковых точекА 0 , R 0 , S 0 … Если через R 0 , S 0 и т. п. провести линии, параллельные A 0 , A 1 , A 2 , получатся одинаковые ряды R 0 , R 1 , R 2 , S 0 , S 1 , S 2 … и т. д

Рис. 18. Пространственная решетка
Врезультате сделанного построения получилась сетка, узлыкоторой соответствуют центрам частиц, слагающих кристалл.
Если представить себе, что в каждой точке В 0, Со и т. д. восстановлена такая же сетка, как и в A 0 , в результате этого построения получится пространственная решетка, которая в известном смысле и будет выражать геометрическое строение кристаллического .
Кристаллы это что
Теория пространственных решеток, созданная великим русским кристаллографом Е. С. Федоровым, получила блестящее подтверждение при исследовании структуры кристаллов посредством рентгеновских лучей. Эти исследования дают не только картины пространственных решеток, но и точные длины промежутков между частицами, находящимися в их узлах.

Рис. 19. Структура алмаза
При этом выяснилось, что существует несколько типов пространственных решеток, отличающихся как характером расположения частиц, так и химической природой их.
Отметим следующие типы пространственных решеток:
Атомные структурные решетки. В узлах этих решеток расположены атомы каких-либо веществ или элемента, соединяющиеся непосредственно между собою в кристаллическую решетку. Такого типа решетка характерна для алмаза, цинковой обманки и некоторых других минералов (см. рис. 19 и 20).
Ионные структурные решетки. В узлах этих решеток расположены ионы, т. е. атомы, имеющие положительный или отрицательный заряд.
Ионные решетки обычны для неорганических соединений, например галогенов щелочных металлов, силикатов и пр.
Прекрасным примером является решетка каменной соли (NaCl) (рис. 21). В ней ионы натрия (Na) по трем взаимно перпендикулярным направлениям чередуются с ионами хлора (Сl) через промежутки, равные 0,28 миллимикрона.

Рис. 20. Структура цинковой обманки
В кристаллических веществах с подобной структурой промежутки между атомами в молекуле равны промежуткам между молекулами, и само понятие молекулы теряет смысл для таких кристаллов. На рис. 20 каждый ион натрия имеет
сверху, снизу, справа, слева, спереди и сзади на равных от него расстояниях по одному иону хлора, которые принадлежат как к данной «молекуле», так и к соседним «молекулам», и нельзя сказать, с каким именно ионом хлора из этих шести составляет молекулу или составлял бы ее при переходе в газообразное состояние.
Кроме описанных выше типов, существуют молекулярные структурные решетки, в узлах которых находятся не атомы или ионы, а обособленные, электрически нейтральные молекулы. Молекулярные решетки особенно характерны для различных органических соединений или, например, для «сухого льда» - кристаллической СO 2 .

Рис. 21. Кристаллическая решетка каменной соли
Слабые («остаточные») связи между структурными единицами таких решеток обусловливают малую механическую прочность подобных решеток, их низкие температуры плавления и кипения. Существуют и такие кристаллы, в которых сочетаются различные типы решеток. В одних направлениях связи частиц являются ионными (валентными), а в других молекулярными (остаточными). Такое строение приводит к различной механической прочности в разных направлениях, обусловливая резкую анизотропию механических свойств. Так, кристаллы молибденита (MoS 2) легко раскалываются по направлению пинакоида (0001) и придают кристаллам этого минерала чешуйчатый облик, подобно кристаллам графита, где обнаруживается сходная структура. Причиной малой механической прочности в направлении перпендикулярном (0001) является отсутствие в этом направлении ионных связей. Целостность решетки здесь удерживается только связями молекулярного (остаточного) характера.
Принимая во внимание все изложенное выше, легко провести параллель между внутренней структурой аморфного вещества, с одной стороны, и кристаллического, с другой:
1.В аморфном веществе частицы располагаются в беспорядке, как бы закрепляя частично хаотическое состояние жидкости; поэтому некоторые исследователи называют , например , переохлажденными жидкостями.
2.В кристаллическом веществе частицы располагаются в стройном порядке и занимают определенное положение в узлах пространственной решетки.
Различие между кристаллическим и стекловатым (аморфным) веществом можно сравнить с тем различием, которое имеется между дисциплинированной воинской частью и рассеянной толпой. Естественно, что кристаллическое состояние более устойчиво, чем аморфное, и аморфное вещество будет легче растворяться, химически реагировать или плавиться. Природные всегда имеют тенденцию приобретать кристаллическое строение, «раскристаллизовываться», например (аморфный кремнезем) со временем переходит в халцедон - кристаллический кремнезем.
Вещество в кристаллическом состоянии обычно занимает несколько меньший объем, чем в аморфном виде, и имеет больший удельный вес; например альбит - полевой шпат состава NaAlSi 3 O 8 в аморфном состоянии занимает 10 куб. единиц, а в кристаллическом-только 9; 1 см 3 кристаллического кремнезема (кварца) весит 2,54 г, а такой же объем стекловатого кремнезема (сплавленного кварца) - только 2,22 г. Особый случай представляет лед, имеющий меньший удельный вес, чем , взятая в том же количестве.
ИССЛЕДОВАНИЕ КРИСТАЛЛОВ РЕНТГЕНОВСКИМИ ЛУЧАМИ
Вопрос о причинах закономерности в распределении физических свойств в кристаллическом веществе, вопрос о внутренней структуре кристаллов впервые пытался разрешить М. В. в 1749 г. на примере селитры. Этот вопрос затем был более широко разработан уже в конце XVIII в. французским кристаллографом Аюи. Аюи высказал предположение, что каждому веществу свойственна определенная кристаллическая форма. Это положение было в дальнейшем опровергнуто обнаружением явлений изоморфизма и полиморфизма. Указанные явления, играющие большую роль в минералогии, будут рассмотрены нами несколько позже.
Благодаря работам русского кристаллографа Е. С. Федорова и некоторых других кристаллографов, теория пространственных решеток, кратко изложенная в предыдущей главе, была разработана математически, и на основании исследования формы кристаллов были выведены возможные типы пространственных решеток; но только в XX в., благодаря исследованию кристаллов рентгеновскими лучами, эта теория была проверена на опыте и блестяще подтвердилась. Целому ряду физиков: Лауэ, Брэггам, Г. В. Вульфу и др. удалось, используя теорию пространственных решеток, доказать совершенно точно, что в узлах кристаллических решеток находятся в одних случаях атомы, а в других молекулы или ионы.
Открытые Рентгеном в 1895 г. лучи, носящие его имя, представляют один из видов лучистой энергии и по многим свойствам напоминают лучи света, отличаясь от них только длиной волны, которая в несколько тысяч раз меньше длины световых волн.

Рис. 22. Схема получения рентгенограммы кристалла по методу Лауэ:
А - рентгеновская трубка; В - диафрагма; С - кристалл; D - фотопластинка
В 1912 г. Лауэ воспользовался кристаллом, где атомы расположены по пространственной решетке, как дифракционной решеткой для получения интерференции рентгеновских лучей. В поставленном им исследовании узкий пучок параллельных рентгеновских лучей (рис. 22) пропускался через тонкий кристалл цинковой обманки С. На некотором расстоянии от кристалла и пер пендикулярно к пучку лучей была помещена фотографическая пластинка D, защищенная от непосредственного действия боковых рентгеновских лучей и от дневного света свинцовыми экранами.
При продолжительной выдержке в течение нескольких часов экспериментаторы получили картину, сходную с рис. 23.
Для световых лучей, обладающих сравнительно с размерами атомов большой длиной волны, атомные сетки пространственной решетки играют роль практически сплошных плоскостей, и световые лучи полностью отражаются от поверхности кристалла. Гораздо более короткие рентгеновские лучи, отраженные от многочисленных атомных сеток, расположенных на определенных расстояниях друг от друга, идя по одному и тому же направлению, будут интерферировать, то ослабляя, то усиливая друг друга. На фотографической пластинке, поставленной на их пути, усиленные лучи дадут при продолжительной экспозиции черные пятна, расположенные закономерно, в тесной связи с внутренним строением кристалла, т. е. с его атомной сеткой и с особенностями расположенных в ней отдельных атомов.
Если взять пластинку, вырезанную из кристалла в определенном кристаллографическом направлении, и произвести с ней тот жеопыт, то на рентгенограмме будет виден узор, соответствующий симметрии строения кристалла.
Более плотным атомным сеткам соответствуют наиболее темные пятна. Редко усаженные атомами грани дают слабые точки или почти не дают их. Центральное пятно на такой рентгенограмме получается от рентгеновских лучей, прошедших через пластинку

Рис. 23. Рентгенография кристалла каменной соли по оси 4-го порядка
по прямому пути; остальные пятна образуют лучи, отраженные от атомных сеток.
На рис. 23 изображена рентгенофотография кристалла каменной соли, из которого была вырезана пластинка около 3 мм толщиной, параллельная грани куба. Посредине видно большое пятно - след центрального пучка лучей.
Расположение мелких пятен симметрично и указывает на существование оси симметрии 4-го порядка и четырех плоскостей симметрии.
Вторая иллюстрация (рис. 24) изображает рентгенограмму кристалла кальцита. Снимок сделан в направлении оси симметрии 3-го порядка. Буквами О обозначены концы осей симметрии 2-го порядка.
В настоящее время для исследования структуры кристаллических тел пользуются разными методами. Существенной особенностью метода Лауэ, кратко описанного выше, является применение только крупных кристаллов, точно ориентированных по отношению к проходящему пучку рентгеновских лучей.
При невозможности пользоваться крупными кристаллами обычно применяется «метод порошков» (метод Дебая-Шерера). Громадное преимущество этого метода в том, что для него не требуется крупных кристаллов. Перед исследованием испытуемое вещество в тонко измельченном состоянии обычно спрессовывается в небольшой столбик. Этим методом можно исследовать не только спрессованные порошки, но и вести работу над готовыми образцами металлов в виде проволоки, если кристаллики их достаточно мелки.
При наличии большого количества кристаллов отражение может произойти от любой грани каждого кристалла. Поэтому на рентгенограмме, полученной по «методу порошков», обычно получается ряд линий, дающих характеристику исследуемого вещества.
Благодаря применению рентгеновских лучей для исследования кристаллов, наконец, была получена возможность проникнуть в область действительного расположения молекул, ионов и атомов внутри кристаллов и определить не только форму атомной решетки, но и расстояния между частицами, ее составляющими.
Изучение структуры кристаллов при помощи рентгеновских лучей позволило определить кажущиеся размеры ионов, входящих в состав данного кристалла. Метод определения величины радиуса иона или, как обычно говорят, ионного радиуса будет ясен из следующего примера. Исследование такого рода кристаллов как MgO, MgS и MgSe, с одной стороны, и MnO, MnS и MnSe, с другой, дало следующие межионные расстояния:
Для
MgO -2,10 Å МnО - 2,24 Å
MgS - 2,60 Å и MnS - 2,59 Å
MgSe - 2,73 Å MnSa - 2,73 Å,
где Å-обозначает величину „ангстрем», равную одной десятимиллионной миллиметра.
Сравнение приведенных величин показывает, что для межионного расстояния в соединениях MgO и МnО размеры ионов Mg и Мn Играют некоторую роль. В других же соединениях видно, что расстояния между ионами S и Se не зависит от входя щего в соединения другого иона, и ионы S и Se соприкасаются между собою, создавая плотнейшую упаковку ионов.

Рис. 24. Рентгенограмма кристалла кальцита на оси 3-го порядка
Вычисление дает для S -2 ионный радиус, равный 1,84 Å,
а для Se -2 - 1,93 Å. Зная ионные радиусы S -2 и Se -2 , можно вычислить и ионные радиусы других ионов. Так О 2 имеет ионный
радиус, равный 1,32Å. F -1 - 1,33Å, Na +l -0,98Å, Са+ 2 - 1,06,
К +1 - 1,33, Mg +2 -0,78Å, Аl +3 -0,57Å, Si +4 - 0,39Å и т. д. Величина ионного радиуса играет большую роль в вопросах изоморфизма и полиморфизма, что и будет рассмотрено в соответствующих разделах.
Рентгеноструктурное изучение минералов сильно продвинуло вперед современную минералогию, как в вопросах понимания строения минералов, так и связи их строения и состава с другими важными свойствами, как спайность, показатель преломления и др. Значение исследования минералов рентгеновскими лучами прекрасно выражается следующей фразой: «Если кристаллографы познавали минерал в той мере, в какой можно изучить здание, осматривая его снаружи, а химики пытались познать это здание, разрушив его и затем изучая в отдельности входившие в его состав материалы, то рентгеноструктурный анализ впервые позволил нам войти в здание и обозревать его внутреннее расположение и убранство».
Статья на тему Структура кристаллов
КРИСТАЛЛИЧЕСКАЯ СТРУКТУРА , расположение атомов кристаллич. в-ва в пространстве. наиб. характерное св-во кристаллической структуры - трехмерная периодичность (см. Кристаллическое состояние). Обычно, говоря о кристаллической структуре, подразумевают среднее во времени расположение атомных ядер (т. наз. статич. модель); более полная информация включает сведения об амплитудах и частотах колебаний атомов (динамич. модель), а также о распределении электронной плотности в межъядерном пространстве. Изучение кристаллических структур и их связи со св-вами в-в составляет предмет кристаллохимии . Геом. характеристики кристаллической структуры, данные о распределении электронной плотности , амплитуды колебаний атомов (точнее, среднеквадратичные смещения от положений равновесия) находят с помощью дифракционных методов исследования (рентгеноструктурного анализа, нейтронографии и электронографии кристаллов), частоты колебаний - методами спектроскопии (ИК, комбинац. рассеяния, неупругого рассеяния нейтронов). Моделирование кристаллической структуры. Идеальная кристаллическая структура характеризуется бесконечной пространств. решеткой, т.е. состоит из идентичных элементарных ячеек. Последние имеют форму параллелепипедов со сторонами а, b, с и углами a , b , g (параметры решетки) и соприкасаются целыми гранями. В реальных кристаллах кристаллическая структура всегда искажена дефектами , а также наличием пов-сти кристалла . Иногда вместо термина "кристаллическая структура" употребляют термин "кристаллич. решетка"; предпочтительнее, однако, придавать последнему иное содержание (см. Кристаллы). Чтобы описать статич. модель кристаллической структуры, необходимо указать ее симметрию , выражаемую одной из пространственных (федоровских) групп, параметры решетки и координаты атомных ядер в ячейке; эти данные позволяют вычислить межатомные расстояния и валентные углы . Первичная трактовка такой модели при наличии между атомами ковалентных связей состоит в том, что атомы соединяют валентными штрихами в соответствии с классич. теорией хим. строения. Межатомные расстояния указывают правильный способ проведения валентных штрихов: обычно расстояние А - В, соответствующее ковалентной связи , существенно короче, чем кратчайшее расстояние между валентно не связанными атомами А и В. Если ковалентные связи отсутствуют (превалируют ионные, металлич. или ван-дер-ваальсовы межатомные взаимод.), модель кристаллической структуры представляют в виде плотной упаковки , образованной шарами одинакового размера (простые в-ва) или шарами неск.Рис. 1. Эллипсоиды тепловых колебаний атомов в структуре m -ацетилен-бис(циклопентадиенникеля) при 300 К (а) и 77 К (6). В центре молекула ацетилена , по бокам - молекулы циклопентадиена.
сортов (напр., анионы образуют упаковку, катионы располагаются в ее пустотах). Учет трехмерного распределения электронной плотности р в пространстве декартовых координат х, у, z приводит к модели кристаллической структуры, согласно к-рой атомные ядра "погружены" в непрерывно распределенный с плотностью р электронный заряд. Совр. прецизионный рентгеноструктурный анализ позволяет экспериментально изучать особенности ф-ции r (х, у, z) и определять изменение электронной плотности атомов в кристалле в сравнении с электронной плотностью r 0 валентно не связанных атомов , получаемой в результате квантовохим. расчетов. Эти данные м. б. полезны для установления областей локализации валентных и неподеленных электронных пар , для обнаружения переноса заряда и др. особенностей строения в-в с ковалентными связями , а также в-в, в к-рых направленные межатомные взаимод. отсутствуют. Для отражения динамики атомов в кристаллической структуре в гармонич. приближении атомы изображают в виде "тепловых эллипсоидов", к-рые имеют след. физ. смысл: с фиксир. вероятностью р в любой момент времени атомное ядро находится внутри или на пов-сти такого эллипсоида (рис. 1). Направление наиб. вытянутости эллипсоида соответствует направлению, в к-ром атом совершает максимальные по амплитуде колебания, направление наиб. сжатия соответствует минимальным по размаху колебаниям. Обычно производят нормировку на вероятность р= 1 / 2 . При данной р размеры эллипсоидов зависят от т-ры. Чтобы количественно охарактеризовать форму и ориентацию атомных тепловых эллипсоидов, для каждого атома указывают 6 независимых компонентов симметричного тензора 2-го ранга, значения к-рых определяют по данным рентгеноструктурного исследования. Описанная динамич. модель не дает сведений о мгновенной структуре кристалла и о последоват. смене мгновенных структур. Информацию такого рода можно получить из спектров неупругого рассеяния нейтронов . Классификация кристаллических структур. В принципе каждому кристаллич. в-ву присуща своя структура. Однако часто разные в-ва имеют кристаллические структуры, одинаковые с точностью до подобия (т. наз. изоструктурность). Иногда такие в-ва способны образовывать смешанные кристаллы (см. Изоморфизм). С др. стороны, одно и то же хим. соед. в разных термодинамич. условиях и при разных способах получения может иметь разные кристаллические структуры (см. Полиморфизм). Кристаллические структуры очень многообразны - от простых (напр., у алмаза) до чрезвычайно сложных (напр., у бора). Изучены кристаллические структуры неск. десятков тысяч в-в, включая белки и др. сложные прир. соед. Для неск. сотен кристаллич. в-в (как неорг., так и орг.) изучено распределение электронной плотности в кристаллах . К ристаллические структуры делят нагомодесмические (координационные) и гетеродесмические. В первых все атомы соединены одинаковыми хим. связями, образующими пространств. каркас (напр., алмаз , галогениды щелочных металлов). Для вторых характерно наличие структурных фрагментов, внутри к-рых атомы соединены наиб. прочными (чаще всего ковалентными) связями; атомы , принадлежащие разл. фрагментам, связаны существенно слабее. Фрагменты могут представлять собой конечные группировки атомов ("острова"), цепи, слои, каркасы; соотв. выделяют островные, цепочечные, слоистые и каркасные кристаллические структуры. Островными кристаллическими структурами обладают почти все орг. соед., а также галогены , О 2 , S, (NH 4) 2 SO 4 и др. Роль островов играют молекулы (см. Молекулярные кристаллы) или многоатомные ионы . Цепочечную кристаллическую структуру имеет, напр., одна из модификаций Se, в к-рой атомы связаны в бесконечные спирали . Слоистое строение имеют графит , BN, MoS 2 и др. Пример каркасной кристаллической структуры - кристаллы СаТiO 3: атомы Ti и О, соединенные ковалентными связями , образуют ажурный каркас, в полостях к-рого расположены атомы Са. Известны кристаллические структуры, в к-рых сосуществуют структурные фрагменты разных типов. Так, кристаллы комплексного соед. N(CH 3) 4 построены из "островов" - ионов N(CH 3) 4 и цепей, образованных атомами Мn, связанными мостиковыми атомами Cl. Часто встречаются кристаллические структуры с неполной упорядоченностью, в к-рых отдельные атомы или структурные фрагменты статистически занимают неск. возможных положений (напр., статистич. наложение слоев в CdI 2). В нек-рых кристаллических структурах при достаточно высокой т-ре отдельные группы атомов или даже целые молекулы находятся в состоянии почти свободного или заторможенного вращения. По характеру связи между атомами или структурными фрагментами различают ковалентные кристаллы , ионные кристаллы , металлические кристаллы и ван-дер-ваальсовы кристаллы . Последняя группа включает, в частности, молекулярные кристаллы . Это деление (как и деление хим. связи на типы) условно, однако типичные представители разных групп резко различаются по св-вам, напр. по энергии структуры (энергия, необходимая для разъединения
БРАВЕ РЕШЕТКИ
Схема построения
БРАВЕ́ РЕШЕТКИ, 14 трехмерных геометрических решеток, характеризующих все возможные типы трансляционной симметрии кристаллов. Браве решетки образуются действием операции переноса (трансляции) на любую точку кристалла.
О. Браве в 1848 показал, что все многообразие кристаллических структур можно описать с помощью 14 типов решеток, отличающихся формами элементарных ячеек и симметрией и подразделяющихся на 7 кристаллографических сингоний. Эти решетки были названы решетками Браве.
Решетки Браве различаются симметрией элементарной ячейки, т. е. соотношением между ее ребрами и углами, а также центрированностью.
Для выбора ячейки Браве используют три условия:
Симметрия элементарной ячейки должна соответствовать симметрии кристалла, точнее наиболее высокой симметрии той сингонии, к которой относится кристалл. Ребра элементарной ячейки должны быть трансляциями решетки;
Элементарная ячейка должна содержать максимально возможное число прямых углов или равных углов и равных ребер;
Элементарная ячейка должна иметь минимальный объем.
По характеру взаимного расположения основных трансляций или расположению узлов все кристаллические решетки разбиваются на четыре типа: примитивные (Р ), базоцентрированные (С ), объемно-центрированные (I ), гранецентрированные (F ).
В примитивной Р -ячейке узлы решетки располагаются только по вершинам ячейки, в объемно-центрированной I -ячейке - один узел в центре ячейки, в гранецентрированной F -ячейке - по одному узлу в центре каждой грани, в базоцентрированной С -ячейке - по одному узлу в центрах пары параллельных граней.
Совокупность координат узлов, входящих в элементарную ячейку, называется базисом ячейки. Всю кристаллическую структуру можно получить, повторяя узлы базиса совокупностью трансляций ячейки Браве.
Для некоторых сингоний элементарная ячейка может содержать узлы не только в углах, но и в центре ячейки, всех или некоторых граней. При этом возможен трансляционный перенос не только на периоды элементарной ячейки, но и на половины диагоналей граней ячейки или пространственных диагоналей. Кроме обязательной трансляционной инвариантности, решетка может переходить в себя при других преобразованиях, к которым относятся повороты, отражения и инверсии. Именно эти дополнительные симметрии определяют тип решетки Браве и отличают ее от других.
Типы решеток Браве:
Кубические: примитивная, объемно-центрированная и гранецентрированная;
Гексагональная, тригональная;
Тетрагональные: примитивная и объемно-централизованная;
Ромбические: примитивная, базо-, объемно- и гранецентрированные;
Моноклинные: примитивная и базоцентрированная;
Триклинная.

Сингони́я (от греч. σύν, «согласно, вместе, рядом», и γωνία, «угол» - дословно «сходноугольность») - классификация кристаллографических групп симметрии, кристаллов и кристаллических решёток в зависимости от системы координат (координатного репера). Группы симметрии с единой координатной системой объединяются в одну сингонию.
Кристаллы, принадлежащие к одной и той же сингонии, имеют подобные углы и рёбра элементарных ячеек.
· Триклинная: {\displaystyle a\neq b\neq c}, {\displaystyle \alpha \neq \beta \neq \gamma \neq 90^{\circ }}
· Моноклинная: {\displaystyle a\neq b\neq c}, {\displaystyle \alpha =\gamma =90^{\circ },\beta \neq 90^{\circ }}
· Ромбическая: {\displaystyle a\neq b\neq c}, {\displaystyle \alpha =\beta =\gamma =90^{\circ }}
· Тетрагональная: {\displaystyle a=b\neq c}, {\displaystyle \alpha =\beta =\gamma =90^{\circ }}
· Гексагональная: {\displaystyle a=b\neq c}, {\displaystyle \alpha =\beta =90^{\circ },\gamma =120^{\circ }}
· Кубическая: {\displaystyle a=b=c}, {\displaystyle \alpha =\beta =\gamma =90^{\circ }}

Основные характеристики кристаллических структур
Кристаллические мат-лы характ наличием дальнего порядка, кот характ. тем, что в нем можно выделить некий объем, расположение атома в котором повторяется но всему объему.
В аморфных мат-ах имеет место ближний порядок, кот. характ. тем. что нет повторения объемов.
Крист. структуру удобно описывать с помощью З х мерной сетки прямых липни, которые делят прос-во на параллелепипиды равных размеров. Пересеч линий образ 3 х мерную пространств. решетку. Узлы решетки, как правило, соответствуют расположению атомов в кристалле. Атом колеблется
около этих положений. Если в такой пространственной решетке можно выделить некий объем, перемещением которого в 3 х направ. позволяет выстроив весь кристалл, то гов. Что найдена элемент, ячейка.
Элемент ячейку принято характеризовать 6 параметрами: а, Ь, с - длина ребер параллелепипеда, α, β, γ.
Форма элемент ячейки определяет кристаллографическую систему координат - сингония. В качестве осей выбирают направления ребер -элем, ячейки, а сами ребра являются единицами измерения. Число прямых углов и равных сторон должно быть mах,а объем элем ячейки должен быть min.